Abstract
Dilated cardiomyopathy is a cardiac disease of unknown origin which is characterized by the gradual development of cardiac failure. Apoptosis, i. e. suicidal programmed cell death, may play a role in the development of heart failure. Only few studies have been carried out until now that describe the rate of apoptosis in human hearts with dilated cardiomyopathy. The numbers reported vary widely. This is also true for studies in different other cardiac diseases such as myocardial infarction or hibernating myocardium.
The methods used to identify apoptosis include electron microscopy, labeling of the DNA fragments (TUNEL), staining with the Hoechst dye, annexin V labeling and documentation of DNA fragmentation using gel electrophoresis (laddering). None of these methods are totally reliable in tissue sections in which apoptosis is not a frequent event when they are not combined with another technique, e. g. TUNEL with electron microscopy or laddering. This has, however, only rarely been done. These technical difficulties may be the reason for the wide variation in the rate of apoptosis reported.
From our own data we conclude that apoptosis plays a significant role in acute ischemia and in hibernating myocardium but its significance in the progression to heart failure in dilated cardiomyopathy has still to be established.
Zusammenfassung
Die dilatative Kardiomyopathie ist eine Herzerkrankung unbekannter Genese. Sie zeichnet sich durch einen allmählichen Verlauf in ihrer Entwicklung aus. Es wurden viele verschiedene Ursachen, wie genetische Abnormalitäten, virale Infektionen und autoimmune Erkrankungen, diskutiert, aber eine abschließende Antwort zur Ätiologie fehlt bis heute. Im Endstadium dieser Erkrankung hat das Herz an Gewicht zugenommen und beide Ventrikel und Atria sind dilatiert.
Histologisch sieht man eine generalisierte Fibrose und Hypertrophie, aber auch eine Atrophie von Myozyten. Der augenscheinliche Verlust von Myozyten führt zu der Annahme, daß auch Apoptose eine wichtige Rolle bei der dilatativen Kardiomyopathie spielen könnte. Dieser programmierte Zelltod hat wahrscheinlich einen maßgeblichen Anteil an der Entstehung von verschiedenen Herzerkrankungen.
Apoptose, der suizidale Zelltod, ist morphologisch durch Zellschrumpfung, Kondensation des Chromatins und Bildung von sogenannten „apoptotic bodies” charakterisiert. Ein weiteres typisches Zeichen ist das Vorhandensein von morphologisch normal aussehenden Mitochondrien und einem intakten Plasmalemm (Abbildung 1). Eines der wichtigsten Kennzeichen der Apoptose ist die DNA-Fragmentierung in gleich große Fragmente von 185 bis 200 bp. Im Gegensatz zum nekrotischen Zelltod, bei dem die Zellen durch eine Entzündungsreaktion weggeräumt werden, fehlt diese bei Apoptose, und die Zelltrümmer werden durch Makrophagen phagozytiert.
Es gibt bisher nur einige wenige Veröffentlichungen über die dilatative Kardiomyopathie, welche die Rate von apoptotischen Zellen im menschlichen Herzen beschreiben. Die bisher publizierten Zahlen variieren sehr stark, und es ist wegen technischer Differenzen schwierig, sie zu vergleichen. Dies trifft auch auf Studien zu, die Apoptose bei Herzinfarkt oder im „hibernating myocardium” beschreiben (Tabelle 1).
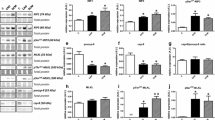
Die verwendeten Methoden sind die TUNEL-Methode, Elektronenmikroskopie, Annexin-V-Markierung, „DNA-Laddering” und die Darstellung von apoptotischen Kernen mit dem Hoechst-Farbstoff. Da Apoptose in menschlichem Herzgewebe nur in geringem Maße vorkommt, ist nur eine Kombination von mindestens zwei dieser Methoden ausreichend, um eine genauere Aussage über das Vorkommen von apoptotischen Zellen im Herzgewebe zu machen. Dies ist leider nur von einigen der Autoren verwirklicht worden. Diese Tatsache ist wahrscheinlich der Grund für die weite Variation der Daten über Apoptose im menschlichen Myokard. Die Suche nach anderen Möglichkeiten, um den Vorgang der Apoptose zu erkennen, muß intensiviert werden. Eine dieser Möglichkeiten könnte zum Beispiel die Spaltung der Polyadenylribosepolymerase (PARP) in die zwei Bruchstücke von 85 und 31 kDa durch die Caspase-3 (CPP 32) (Abbildung 2a) sein. Die Substrate der Caspase-6 sind unter anderem die Lamine A, B1 (Abbildung 2b) und B2. Ihre Abnahme in der Kernmembran ist eine Vorstufe zu der irreversiblen DNA-Fragmentierung. Der Nachweis des Fas-Rezeptors. seines Liganden, von p53, c-myc und den Komponenten der Bcl-2-Gruppe könnte weitere nützliche Informationen bringen.
Zusammenfassend können wir von unseren eigenen Untersuchungen sagen, daß Apoptose eine wichtige Rolle bei der akuten Ischämie und im „hibernating myocardium” spielt. Ihre Rolle bei der dilatativen Kardiomyopathie muß aber noch durch weitere Studien geklärt werden.
Similar content being viewed by others
References
Aerbert H, Cornelius T, Birnbaum D, et al. Induction of early immediate genes and programmed cell death following cardioplegic arrest in human hearts. Eur J Cardiothorac Surg 1997;12:261–7.
Bardales RH, Hailey LS, Xie SS, et al. In situ apoptosis assay for the detection of early acute myocardial infarction. Am J Pathol 1996;149:821–9.
Colucci WS. Apoptosis in the heart [editorial; comment]. N Engl J Med 1996;335:1224–6.
Dimmeler S, Rippmann V, Weiland U, et al. Angiotensin II induces apoptosis of human endothelial cells. Circ Res 1997;81:970–6.
Editorial. Naatural history of dilated cardiomyopathy. Lancet 1986;1:248–9.
Elsässer A, Müller KD, Strasser R, et al. “Hibernating myocardium”: degeneration caused by apoptosis. Circulation 1995; Suppl 1:891.abstract.
Elsässer A, Schlepper M, Klövekorn WP, et al. Hibernating myocardium — an incomplete adaptation to ischemia. Circulation 1997;96:2920–31.
Freude B, Masters TN, Kostin S, et al. Cardiomyocyte apoptosis in acute and chronic conditions. Basic Res Cardiol 1998;93:85–9.
Gavrieli Y, Sherman Y, Ben-Sasson SA. Identification of programmed cell death in situ via specific labeling of nuclear DNA fragmentation. J Cell Biol 1992;119:493–501.
Itoh G, Tamura J, Suzuki M, et al. DNA fragmentation of human infarcted myocardial cells demonstrated by the nick end labeling method and DNA agarose gel electrophoresis. Am J Pathol 1995;146:1325–31.
James T. The variable morphological coexistence of apoptosis and necrosis in human myocardial infarction: Significance for understanding its pathogenesis, clinical course, diagnosis and prognosis. Coron Art Dis 1998;9:291–307.
James TN, Terasaki F, Pavlovich ER, et al. Apoptosis and pleomorphic micromitochondriosis in the sinus nodes surgically excised from five patients with the long QT syndrome. J Lab Clin Med 1993;122:309–23.
Kawano H, Okada R, Kawano Y, et al. Apoptosis in acute and chronic myocarditis. Jpn Heart J 1994;35:745–50.
Lazebnik YA, Kaufmann SH, Desnoyers S, et al. Cleavage of poly(ADP-ribose) polymerase by a proteinase with properties like ICE. Nature 1994;371:346–7.
Majno G, Joris I. Apoptosis, oncosis and necrosis. Am J Pathol 1995;146:3–15.
Mallat Z, Tedgui A, Fontaliran F, et al. Evidence of apoptosis in arrhythmogenic right ventricular dysplasia [see comments]. N Engl J Med 1996;335:1190–6.
Martin S, Reutelingsperger C, McGahon A, et al. Early redistribution of plasma membrane phosphatidylserine is a general feature of apoptosis regardless of the initiating stimulus: Inhibition by overexpression of Bcl-2 and Abl. New York: Rockefeller University Press, 1995;182:1545–56.
Narula J, Haider N, Virmani R, et al. Apoptosis in myocytes in end stage heart failure. N Engl J Med 1996;335:1182–9.
Olivetti G, Abbi R, Quaini F, et al. Apoptosis In the failing human heart. N Engl J Med 1997;336:1131–41.
Olivetti G, Quaini F, Sala R, et al. Acute myocardial infarction in humans is associated with activation of programmed myocyte cell death in the surviving portion of the heart. J Mol Cell Cardiol 1996;28:2005–16.
Piot CA, Padmanaban D, Ursell PC, et al. Ischemic preconditioning decreases apoptosis in rat hearts in vivo. Circulation 1997;96:1598–604.
Rao L, Perez D, White E. Lamin proteolysis facilitates nuclear events during apoptosis. J Cell Biol 1996;135:1441–55.
Saraste A, Pulkki K, Kallajoki M, et al. Apoptosis in human acute myocardial infarction. Circulation 1997;95:320–3.
Schaper J, Froede R, Hein S, et al. Impairment of the myocardial ultrastructure and changes of the cytoskeleton in dilated cardiomyopathy. Circulation 1991;83:504–14.
Schlegel J, Peters I, Orrenius S, et al. CPP32/apopain is a key interleukin 1β converting enzyme-like protease involved in Fas-mediated apoptosis. J Biol Chem 1995;271:1841–4.
Shaddy R. Apoptosis in heart transplantation. Coron Art Dis 1997;8:617–21.
Takahashi A, Alnemeri ES, Lazebnik YA, et al. Cleavage of lamin A by Mch2a but not CPP 32: Multiple interleukin 1β converting enzyme-related proteases with distinct substrate recognition properties are active in apoptosis. Proc Natl Acad Sci USA 1996;93:8395–400.
Tewari M, Quan L, O’Rourke K, et al. Yama/CPP32β, a mammalian homolog of CED-3, is a CrmA-inhibitable protease that cleaves the death substrate poly (ADP-ribose) polymerase. Cell 1995;81:801–9.
Valente M, Calabrese F, Thiene G, et al. In vivo evidence of apoptosis in arrhythmogenic right ventricular cardiomyopathy. Am J Pathol 1998;152:479–84.
Whiteside G, Cougnon N, Hunt SP, et al. An improved method for detection of apoptosis in tissue sections and cell culture, using the Tunel technique combined with Hoechst stain. Brain Res Protocols 1998;2:160–4.
Wyllie A. Glucocorticoide-induced thymocyte apoptosis is associated with endogenous endonuclease activation. Nature 1980; 284:555–6.
Author information
Authors and Affiliations
Corresponding author
Rights and permissions
About this article
Cite this article
Schaper, J., Lorenz-Meyer, S. & Suzuki, K. The role of apoptosis in dilated cardiomyopathy. Herz 24, 219–224 (1999). https://doi.org/10.1007/BF03044964
Issue Date:
DOI: https://doi.org/10.1007/BF03044964