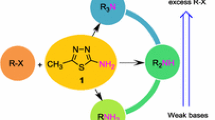
Abstract
A novel one-pot method based on the sequence of the Fisher reaction between nitroacetophenone and phenylhydrazines, the reduction with metallic tin directly in polyphosphoric acid, and acylation has been developed for the synthesis of indoloquinolines. The obtained indolo-[3,2-c]quinolines are precursors of the analogs of isocryptolepine alkaloid.
Similar content being viewed by others
References
T. Robinson, The Biochemistry of Alkaloids, Springer, New York, 1981.
A. N. Tackie, G. L. Boye, M. H. M. Sharaf, P. L. Schi, R. C. Crouch, T. D. Spitzer, R. L. Johnson, J. Dunn, D. Minick, G. E. Martin, J. Nat. Prod., 1993, 56, 653.
A. Paulo, E. T. Gomes, P. J. Houghton, J. Nat. Prod., 1995, 58, 1485.
A. Paulo, E. T. Gomes, J. Steele, D. C. Warhurst, P. J. Houghton, Planta Medica, 2000, 66, 30.
K. Cimanga, T. De Bruyne, A. Lasure, B. Van Poel, L. Pieters, M. Claeys, D. V. Berghe, K. Kambu, L. Tona, A. J. Vlietinck, Planta Medica, 1996, 62, 22.
U. E. Odoh, C. I. Akwuaka, Pharmacognosy J., 2012, 28, 40.
V. E. Kalugin, A. M. Shestopalov, Russ. Chem. Bull., 2018, 67, 1492.
P. Aroonkit, C. Thongsornkleeb, J. Tummatorn, S. Krajangsri, M. Mungthin, S. Ruchirawat, Eur. J. Med. Chem., 2015, 94, 56.
P. E. Murray, K. Mills, J. A. Joule, J. Chem. Res. (S), 1998. 377.
P. T. Parvatkar, P. S. Parameswaran, S. G. Tilve, Current Organic Chemistry, 2011, 15, 1036.
P. S. Mahajan, V. T. Humne, S. D. Tanpure, S. B. Mhaske, Org. Lett., 2016, 18, 3450.
R. N. Kumar, T. Suresh, P. S. Mohan, Tetrahedron Lett., 2002. 43, 3327.
Y. Miki, M. Kuromatsu, H. Miyatake, H. Hamamoto, Tetrahedron Lett., 2007, 48, 9093.
L. R. Whittell, K. T. Batty, R. P. M. Wong, E. M. Bolitho, S. A. Fox, T. M. E. Davis, P. E. Murray, Bioorg. Med. Chem., 2011. 19, 7519.
S. Hostyn, B. U. W. Maes, L. Pieters, G. L. F. Lemière, P. Mátyus, G. Hajós, R. A. Dommisse, Tetrahedron, 2005, 61, 1571.
T. H. M. Jonckers, B. U. W. Maes, G. L. F. Lemière, G. Rombouts, L. Pieters, A. Haemers, R. A. Dommisse, Synlett, 2003, 5, 615.
A. Molina, J. J. Vaquero, J. L. Garcia-Navio, J. Alvarez-Builla, B. de Pascual-Teresa, F. Gago, M. M. Rodrigo, M. Ballesteros, J. Org. Chem., 1996, 61, 5587.
G. Van Baelen, C. Meyers, G. L. F. Lemière, S. Hostyn, R. Dommisse, L. Maes, K. Augustyns, A. Haemers, L. Pieters, B. U. W. Maes, Tetrahedron, 2008, 64, 1180.
C. Meyers, G. Rombouts, K. T. J. Loones, A. Coelho, B. U. W. Maes, Adv. Synth. Catal., 2008, 350, 465.
T. Dhanabal, R. Sangeetha, P. S. Mohan, Tetrahedron, 2006, 62, 6258.
T. Dhanabal, R. Sangeetha, P. S. Mohan, Tetrahedron Lett., 2005. 46, 4509.
A. Molina, J. J. Vaquero, J. L. García-Navio, J. Alvarez-Builla, Tetrahedron Lett., 1993, 34, 2673.
P. M. Fresneda, P. Molina, S. Delgado, Tetrahedron Lett., 1999. 40 7275.
P. M. Fresneda, P. Molina, S. Delgado, Tetrahedron, 2001, 57, 6197.
G. A. Kraus, H. Guo, G. Kumar, G. Pollock, H. Carruthers, D. Chaudhary, J. Beasley, Synthesis, 2010, 8, 1386.
P. K. Agarwal, D. Sawant, S. Sharma, B. Kundu, Eur. J. Org. Chem., 2009, 292.
A. V. Aksenov, D. A. Aksenov, G. D. Griaznov, N. A. Aksenov, L. G. Voskressensky, M. Rubin, Org. Biomol. Chem., 2018, 16, 4325.
A. V. Aksenov, D. A. Aksenov, N. A. Orazova, N. A. Aksenov, G. D. Griaznov, A. De Carvalho, R. Kiss, V. Mathieu, A. Kornienko, M. Rubin, J. Org. Chem., 2017, 82, 3011.
A. V. Aksenov, I. V. Aksenova, Chem. Heterocycl. Compd., 2009. 45, 130.
I. S. Antipin, M. A. Kazymova, M. A. Kuznetsov, A. V. Vasilyev, M. A. Ishchenko, A. A. Kiryushkin, L. M. Kuznetsova, S. V. Makarenko, V. A. Ostrovskii, M. L. Petrov, O. V. Solod, Yu. G. Trishin, I. P. Yakovlev, V. G. Nenaidenko, E. K. Beloglazkina, I. P. Beletskaya, Yu. A. Ustynyuk, P. A. Solov'ev, I. V. Ivanov, E. V. Malina, N. V. Sivova, V. V. Negrebetskii, Yu. I. Baukov, N. A. Pozharskaya, V. F. Traven', A. E. Shekotikhin, A. V. Varlamov, T. N. Borisova, Yu. A. Lesina, E. A. Krasnokutskaya, S. I. Rogozhnikov, S. N. Shurov, T. P. Kustova, M. V. Klyuev, O. G. Khelevina, P. A. Stuzhin, A. Yu. Fedorov, A. V. Gushchin, V. A. Dodonov, A. V. Kolobov, V. V. Plakhtinskii, Yu. V. Orlov, A. P. Kriven'ko, O. V. Fedotova, N. V. Pchelintseva, V. N. Charushin, O. N. Chupakhin, Yu. N. Klimochkin, A. Yu. Klimochkina, V. N. Kuryatnikov, Yu. A. Malinovskaya, A. S. Levin, O. E. Zhuravlev, L. I. Voronchikhina, A. S. Fisyuk, A. V. Aksenov, N. A. Aksenov, I. V. Aksenova, Russ. J. Org. Chem., 2017, 53, 1275.
A. I. Konovalov, I. S. Antipin, V. A. Burilov, T. I. Madzhidov, A. R. Kurbangalieva, A. V. Nemtarev, S. E. Solovieva, I. I. Stoikov, V. A. Mamedov, L. Ya. Zakharova, E. L. Gavrilova, O. G. Sinyashin, I. A. Balova, A. V. Vasilyev, I. G. Zenkevich, M. Yu. Krasavin, M. A. Kuznetsov, A. P. Molchanov, M. S. Novikov, V. A. Nikolaev, L. L. Rodina, A. F. Khlebnikov, I. P. Beletskaya, S. Z. Vatsadze, S. P. Gromov, N. V. Zyk, A. T. Lebedev, D. A. Lemenovskii, V. S. Petrosyan, V. G. Nenaidenko, V. V. Negrebetskii, Yu. I. Baukov, T. A. Shmigol', A. A. Korlyukov, A. S. Tikhomirov, A. E. Shchekotikhin, V. F. Traven', L. G. Voskresenskii, F. I. Zubkov, O. A. Golubchikov, A. S. Semeikin, D. B. Berezin, P. A. Stuzhin, V. D. Filimonov, E. A. Krasnokutskaya, A. Yu. Fedorov, A. V. Nyuchev, V. Yu. Orlov, R. S. Begunov, A. I. Rusakov, A. V. Kolobov, E. R. Kofanov, O. V. Fedotova, A. Yu. Egorova, V. N. Charushin, O. N. Chupakhin, Yu. N. Klimochkin, V. A. Osyanin, A. N. Reznikov, A. S. Fisyuk, G. P. Sagitullina, A. V. Aksenov, N. A. Aksenov, M. K. Grachev, V. I. Maslennikova, M. P. Koroteev, A. K. Brel', S. V. Lisina, S. M. Medvedeva, Kh. S. Shikhaliev, G. A. Suboch, M. S. Tovbis, L. M. Mironovich, S. M. Ivanov, S. V. Kurbatov, M. E. Kletskii, O. N. Burov, K. I. Kobrakov, D. N. Kuznetsov, Russ. J. Org. Chem., 2018, 54, 157.
A. V. Aksenov, N. A. Aksenov, Z. V. Dzhandigova, D. A. Aksenov, L. G. Voskressensky, V. G. Nenajdenko, M. Rubin, RSC Adv., 2016, 6, 9388.
M. G. Uchuskin, A. S. Pilipenko, O. V. Serdyuk, I. V. Trushkov, A. V. Butin, Org. Biomol. Chem., 2012, 10, 7262–7265.
F. Uhlig, Angew. Chem., 1954, 66, 435.
A.-L. Huhti, P. A. Gartaganis, Canadian J. Chem., 1956, 34, 785.
Author information
Authors and Affiliations
Corresponding author
Additional information
Based on the materials of the V All-Russian Organic Chemistry Conference (ROCC-V) (September 10–14, 2018, Vladikavkaz, Russia).
Published in Russian in Izvestiya Akademii Nauk. Seriya Khimicheskaya, No. 4, pp. 0836–0840, April, 2019.
Rights and permissions
About this article
Cite this article
Aksenov, N.A., Gasanova, A.Z., Abakarov, G.M. et al. Novel convenient one-pot method for the synthesis of indoloquinolines. Russ Chem Bull 68, 836–840 (2019). https://doi.org/10.1007/s11172-019-2493-4
Received:
Revised:
Accepted:
Published:
Issue Date:
DOI: https://doi.org/10.1007/s11172-019-2493-4