Abstract
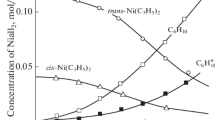
An attempt has been made to apply concepts of complex chemistry in solution to heterogeneous reaction kinetics. A series of solid Ni(II) complexes containing the same anionic ligand and volatile ligands of the same type were investigated under isothermal conditions on the basis of TG curves, and the kinetics of their decompositions were studied. Since the reactions are controlled by the appropriate chemical process, the differences found between the activation energies and the measured values of the standard enthalpies might be explained by substitution processes in the primary coordination sphere. According to the experimental results, the formation of intermediates has to be presumed in all the reactions investigated. A mechanism could be proposed for their formation. No dependence could be detected between the geometrical configuration of the coordination sphere and the stoichiometry of the decomposition process.
Résumé
On a étudié la cinétique de la décomposition d'une série de composés solides du Ni(II) avec le mÊme ligand anionique et avec des ligands volatils du mÊme type en utilisant les résultats de la thermogravimétrie isotherme. Comme les réactions sont contrÔlées par leur processus chimique propre, les différences qui ont été observées entre l'énergie d'activation et les valeurs mesurées des enthalpies standard peuvent s'expliquer par des processus de substitution dans la sphère de coordination primaire. Les résultats expérimentaux laissent présumer l'existence d'étapes intermédiaires pour toutes les réactions étudiées. Le mécanisme de leur formation a pu Être proposé. On n'a pas pu déceler de rapport entre la configuration géométrique de la sphère de coordination et la stoechiométrie du processus de décomposition.
Zusammenfassung
Es wurde ein Versuch gemacht, komplexchemische Vorstellungen in Lösungen auf die Kinetik heterogener Reaktionen zu übertragen. Eine Reihe fester Ni(II)-Komplexe mit demselben anionischen Liganden und mit flüchtigen Liganden desselben Typs wurde aufgrund der TG-Kurve unter isothermen Bedingungen untersucht und die Kinetik ihrer Zersetzung studiert. Da die Reaktionen durch den entsprechenden chemischen Vorgang gesteuert werden, können die zwischen den Aktivierungsenergien und den gemessenen Werten der Standardenthalpien gefundenen Unterschiede durch Substitutionsvorgänge in der primären Koordinationssphäre erklärt werden. Den Versuchsergebnissen gemäß muß bei sämtlichen untersuchten Reaktionen die Bildung von Zwischenprodukten angenommen werden. Eine Erklärung ihres Bildungsmechanismus wird vorgeschlagen. Es wurde kein Zusammenhang zwischen der geometrischen Konfiguration der Koordinationssphären und der Stöchiometrie des Zersetzungsvorganges gefunden.
РЕжУМЕ
сДЕлАНА пОпыткА пРИл ОжИть пОНьтИь хИМИИ кОМплЕксОВ В РОстВОР Ох к кИНЕтИкЕ гЕтЕРОгЕННых РЕАкцИ И. ИсслЕДОВАН В ИжОтoРМ ИЧЕскИх УслОВИьх НА ОсНОВАНИ И кРИВых тг РьД тВЕРДых кОМплЕксОВ Ni(II), сОДЕРжАЩИх ОДИНАкОВ ыИ АНИОННыИ лИгАНД И лЕт УЧИЕ лИгАНДы ОДНОгО тИпА, И ИжУЧЕНА кИНЕтИкА Их РАспАДА. В сВьжИ с тЕМ, ЧтО РЕАкцИИ кОНтР ОлИРУУтсь сООтВЕтстВУУЩИМ хИМ ИЧЕскИМ пРОцЕссОМ, ОБ НАРУжЕННАь РАжНИцА МЕжДУ ЁНЕРгИ ьМИ АктИВАцИИ И ИжМЕРЕННыМИ ВЕлИЧИ НАМИ стАНДАРтНых ЁНт АльпИИ МОжЕт Быть ОБЩьсНЕНА пРОцЕ ссАМИ жАМЕЩЕНИь В пЕРВИЧНО И кООРДИНАцИОННОИ сФ ЕРЕ. сОглАсНО РЕжУльтАтА М ЁкспЕРИМЕНтА ВО ВсЕх ИсслЕДОВАННы х РЕАкцИьх пРЕДпОлАг АЕтсь ОБРАжОВАНИЕ пРОМЕжУ тОЧНых пРОДУктОВ. пРЕДлОжЕН МЕхАНИжМ И х ОБРАжОВАНИь. жАВИсИ МОсть МЕжДУ гЕОМЕтРИЧЕскОИ кОНФ ИгУРАцИЕИ кООРДИНАцИОННОИ сФЕ Ры И стЕхИОМЕтРИЕИ пР ОцЕссА РАспАДА УстАНОВИть Н Е УДАлОсь.
Similar content being viewed by others
References
W. W. Wendlandt andJ. P. Smith, The Thermal Properties of Transition Metal Amino-complexes, Elsevier, Amsterdam, 1967.
F. Basolo andF. G. Pearson, Mechanism of Inorganic Reactions, 2nd edition. Wiley, New York, London, 1967.
C. H. Langford andH. B. Gray, Ligand Substitution Processes, Benjamin, New York, Amsterdam, 1965.
T.šramko, E.Jóna and A.Sirota, Proceedings of the 2nd Conference on Coordination Chemistry. Smolenice, Bratislava, čSSR, 1969, p. 239.
J. Kohout, M. Kohutovà andE. Jona, Z. Naturforsch., 25 (1970) 1054.
E. Jóna, T. šramko, J. Kohout, A. Sirota andJ. GaŽo, Chem. Zvesti 25 (1971) 241.
H. C. A.King, E.Körös and S. M.Nelson, J. Chem. Soc. (1963) 5449.
S. M. Nelson andT. M. Shepherd, Inorg. Chem., 4 (1965) 813.
E. Jóna, T. šramko andJ. Gazo, J. Thermal. Anal. 4 (1972) 61.
E. Jona, V. Jesenák andT. šramko, Chem. Zvesti, 23 (1969) 420.
D. Young, Decomposition of Solids. Russian translation “Kinetika razlozhenija tvjerdych veshchestv”. Izdat. “Mir” Moscow, 1969., p. 97.
S. škramovský, R. Forster andG. F. Hüttig, Z. Phys. Chem., 25 (1934) 1.
G. F. Hüttig, Mh. Chem., 85 (1954) 376.
I. Proks, Chem. Zvesti, 20 (1966) 697.
R. G. Pearson, C. R. Boston andF. Basolo, J. Amer. Chem. Soc., 75 (1953) 3089.
E. Jóna, T. šramko, P. Ambrovic andJ. Gazo, J. Thermal Anal., 4 (1972) 153.
Author information
Authors and Affiliations
Rights and permissions
About this article
Cite this article
Jóna, E., šramko, T. & Jesenàk, V. The mechanism of thermal decomposition of solid complexes of the type Ni(NCS)2L2 . Journal of Thermal Analysis 5, 315–318 (1973). https://doi.org/10.1007/BF01950379
Issue Date:
DOI: https://doi.org/10.1007/BF01950379