Abstract
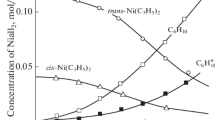
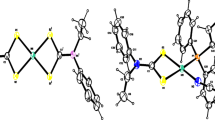
Thermal analysis of mono-, bis- and trisethylenediamine (en) complexes of Ni(II) chloride was carried out using TG, DTG and DTA techniques. The kinetic parameters were estimated from dynamic TG studies using the Coats and Redfern equation. The thermal stability of the metal-ligand (Ni-N) bond in, the complex was found to decrease with increasing Ni∶en ratio. The DTA studies showed that the loss of en was initially endothermic but became increasingly exothermic with the progress of the decomposition. The final step in the case of all the three complexes was always composite in nature causing the loss of both Cl atoms with simultaneous oxidation of Ni to NiO. The dissociation of the Ni-en bonds appears to be regulated by the “nucleation and growth” mechanism. Kinetic parameters corresponding to various steps of decomposition of all the three complexes were evaluated.
Zusammenfassung
Mittels TG-, DTG- und DTA-Verfahren wurde eine Thermountersuchung des mono-, bis- und tris-Äthylendiammin (en) komplexes von Ni(II)-chlorid durchgeführt. Unter Zuhilfenahme der Gleichung von Coats und Redfern wurden die kinetischen Parameter anhand der Daten aus dynamischen TG-Untersuchungen abgeschätzt. Es wurde gefunden, daß die thermische Stabilität der Metall-Ligand Bindung (Ni-N) der Komplexe mit anwachsendem Ni:en Verhältnis absinkt. Aufgrund der DTA Untersuchungen erwies sich die Abgabe von en anfänglich als endotherm, mit fortschreitender Zersetzung jedoch als zunehmend exotherm. Bei allen drei Komplexen war der letzte Schritt immer komplexer Natur und beinhaltete die Abgabe beider Chloratome verbunden mit einer gleichzeitigen Oxidation von Ni zu NiO. Die Dissoziation der Ni-en Bindung scheint durch einen „Keimbildungs- und Wachstums”-mechanismus bestimmt zu werden. Die kinetischen Parameter für die einzelnen Zersetzungsschritte aller drei Komplexe wurden ermittelt.
Резюме
Методами ТГ, ДТГ и ДТА проведен термически й анализ монр-, бис- и три этилендиаминовых комплексов хлорида никеля. Исходя из дан ных динамической ТГ и используя уравнени е Коутса-Редферна, бы ли определены кинетические пара метры. Найдено, что термоустойчив ость связи металл-л иганд в комплексах уменьша ется с увеличением соотношения никель: зтилендиамнн. ДТА ис следования показали, что потеря лиганда носила первоначально эндо термический характ ер, но по мере дальнейшего разлож ения процесс становился все боле е экзотермическим. К онечная стадия разложения в сех трех комплексов носила сложный хара ктер, обусловленный потерей обоих атомов хлора и одно временым окислением никеля до его оксида. Разры в связей никель-этилендиам ин свидетельствует о механизме «образо вания и роста центров кристаллизации». Оп ределены кинетичес кие параметры различных стадий ра зложения всех трех к омплексов.
Similar content being viewed by others
References
Stability Constants of Metal-Ion Complexes, compiled by L. G. Sillen and A. E. Martell. The Chemical Society, London Special Publication No. 17, 1964, p. 372 and Special Publication No. 25, 1971, p. 261.
R. H. Lee, E. Grinswold and J. Kleinberg, Inorg. Chem., 3 (1964) 1278.
T. D. George and W. W. Wendlandt, J. Inorg. Nucl. Chem., 25 (1963) 395.
A. I. Vogel, A Textbook of Quantitative Inorganic Analysis, Ed. 3, ELBS and Longman, London 1975, p. 269.
A. I. Vogel, A Textbook of Quantitative Inorganic Analysis, Ed. 3, ELBS and Longman, London 1975, p. 708.
K. Nakamoto, Infrared and Raman Spectra of Inorganic and Coordination Compounds, Ed. 3, Wiley Interscience, N.Y., 1977, Part III.
D. B. Powell and N. Shepperd, Spectrochim. Acta, 17 (1961) 68.
A. B. P. Lever, Inorganic Electronic Spectroscopy, Elsevier, 1984, p. 507.
A. W. Coats and J. P. Redfern, Nature, 201 (1964) 68.
H. Tanaka, J. Thermal Anal., 32 (1987) 521.
Author information
Authors and Affiliations
Additional information
A research grant to LSP from the C.S.I.R. (India) and a JRF to SRN are thankfully acknowledged.
Rights and permissions
About this article
Cite this article
Probhumirashi, L.S., Natu, G.N. & Nayak, S.R. Thermal analysis of ethylenediamine complexes of Ni(II) chloride. Journal of Thermal Analysis 35, 1105–1110 (1989). https://doi.org/10.1007/BF01913027
Issue Date:
DOI: https://doi.org/10.1007/BF01913027