Summary
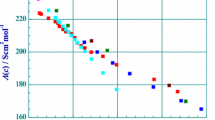
Conductivities of the aqueous solutions of nearly thirty samples of Graham's salt having different molecular weights have been observed. Plots of equivalent conductivity (Λ) against square root of equivalent concentration (C 1/2) show a strong curvature at lower concentration reminiscent of the behaviour of weak electrolytes. It has been explained as being due to the association of counter-ions with poly-ions because of a high charge density around the latter. The rise in equivalent conductance with decrease in concentration is more pronounced in the case of low-molecular-weight samples. In high molecular-weight compounds the molecular weight dependance is less conspicuous. On plotting equivalent conductance against weight-average molecular weight for any particular concentration of Graham's salt, curves have been obtained which show that with an increase in molecular weight conductivity falls first sharply and then slowly. The effect of the weight-average molecular weight on conductivity is much more pronounced than that of the corresponding endgroup molecular weight, although the values of the latter also affect the conductance.
The highly curved plots of Λ vs. C 1/2 can be reduced to linear ones on a log-log scale. A plot of specific conductivity against the equivalent concentration is also invariably linear.
The values of ‘apparent basicity’ calculated for various samples of Graham's salt with the help of Ostwald's rule lie between 2 and 3; they have a tendency to decrease with increase in weight-average molecular weight.
Zusammenfassung
Die Leitfähigkeit wäßriger Lösungen von nahezu 30 Proben aus Graham-Salz, die verschiedenes Molekulargewicht hatten, wird betrachtet. Die Auftragung der Äquivalentleitfähigkeit gegen die Quadratwurzel aus der Äquivalentkonzentration zeigt starke Krümmungen bei niedrigen Konzentrationen, die an das Verhalten schwacher Elektrolyte erinnern. Sie wird erklärt durch Assoziationen der Gegenionen mit den Polyionen infolge der hohen Ladungsdichte um letztere. Der Anstieg der Äquivalentleitfähigkeit mit sinkender Konzentration ist für die niedermolekularen Proben stärker ausgeprägt. Bei den hochmolekularen Verbindungen ist die Molekulargewichtsabhängigkeit weniger auffällig. Trägt man die Äquivalentleitfähigkeit gegen das Gewichtsmittel des Molekulargewichts für irgend eine Konzentration des Graham-Salzes auf, so ergeben sich Kurven, die mit steigendem Molekulargewicht erst einen scharfen und später einen langsamen Leitfähigkeitsabfall zeigen. Der Effekt des Gewichtsmittels des Molekulargewichts auf die Leitfähigkeit ist viel ausgeprägter als der des entsprechenden Endgruppenmolekulargewichts, obgleich der Betrag des letzteren die Leitfähigkeit ebenfalls beeinflußt.
Die stark gekrümmten Kurven von Λ gegen √C können in einer doppelt-logarithmischen Skala zu linearen reduziert werden. Die Auftragung der spezifischen Leitfähigkeit gegen die Äquivalentkonzentration ist ebenfalls invariabel linear.
Die Werte der scheinbaren Basizität, berechnet mit Hilfe der Ostwald-Regel für verschiedene Graham-Salzproben, liegen zwischen 2 und 3. Sie haben die Tendenz, mit Zunahme des Gewichtsmittels der Molekulargewichte abzunehmen.
Similar content being viewed by others
References
Hartley, G. S., Quart. Revs. 2, 152 (1948).
Meyer, K. H., Natural and Synthetic High Polymers (New York 1950).
Jirgensons, B., Organic Colloids (Amsterdam 1958).
Kern, W., Z. phys. chem. A 181, 249 (1938).
Briggs, D. R., J. Phys. and Colloid Chem. 52, 76 (1948).
Fuoss, R. M. and G. I. Cathers, J. Polymer Sci. 2, 12 (1947).
Edelson, D. and R. M. Fuoss, J. Amer. Chem. Soc. 70, 2832 (1948); ibid. 72, 306 (1950).
Fuoss, R. M. and U. P. Strauss, J. Polymer Sci. 3, 246 (1948).
Cathers, G. I. and R. M. Fuoss, ibid. 4, 121 (1949).
Fuoss, R. M. and D. Edelson, ibid. 6, 523 (1951).
Fuoss, R. M., Disc. Faraday Soc. 11, 125 (1951).
Fuoss, R. M., J. Polymer Sci. 12, 185 (1954).
McFarlane, R. jr. and R. M. Fuoss, ibid. 23, 403 (1957).
Huizenga, J. R., P. F. Grieger and F. T. Wall, J. Amer. Chem. Soc. 72, 2936, 4228 (1950).
Wall, F. T. and R. H. Doremus, ibid. 76, 1557 (1954).
Tammann, G., J. pr. chem. 45, 463 (1892).
Davies, C. W. and C. B. Monk, J. Chem. Soc. 1949, 413.
Monk, C. B., ibid. 1949, 423, 427.
Schindewolf, U., Z. phys. Chem. (Frankfurt) N. F. 1, 134 (1954).
Wall, F. T. and R. H. Doremus, J. Amer. Chem. Soc. 76, 868 (1954).
Teichert, W. and K. Rinman, Acta Chem. Scand. 2, 225 (1948).
Chatterji, A. C. and H. N. Bhargava, J. Polymer Sci. 35, 235 (1959).
Newman, F. H., Electrolytic Conduction, p. 324 (London 1930).
Bonneman-Bemia, P., Ann. Chim. (Paris) 16, 395 (1941).
Basu, S. and P. C. DasGupta, J. Colloid Sci. 7, 53 (1952).
Robinson, C. and H. E. Garrett, Trans. Faraday Soc. 35, 771 (1939).
Smoluchowski, M. von, Kolloid-Z. 18, 190 (1916).
Chatterji, A. C. and H. N. Bhargava, ibid. 160, 35 (1958).
Fuoss, R. M., A. Katchalsky and S. Lifson, Natl. Acad. Sci. (U.S.) 37, 579 (1951).
Strauss, U. P. and T. R. Treitler, J. Amer. Chem. Soc. 77, 1473 (1955).
Chatterji, A. C., H. N. Bhargava, K. K. Tewari and P. S. Krishnan, Arch. Biochem. Biophys. 85, 19 (1959).
Chatterji, A. C. and H. N. Bhargava, J. Polymer Sci. 39, 543 (1959).
Stearn, A., J. Amer. Chem. Soc. 44, 670 (1922).
Pascal, P., Compt. Rend. 179, 966 (1924).
Mme. Salih, R., Bull. soc. chim. belges 5, 4, 1724 (1937).
Wiesler, A., Z. anorg. Chem. 28, 177 (1901).
Fitzgerald, E. B. and R. M. Fuoss, J. Polymer Sci. 14, 329 (1954).
Author information
Authors and Affiliations
Rights and permissions
About this article
Cite this article
Chatterji, A.C., Bhargava, H.N. Studies in inorganic polyelectrolytes. Part III. Kolloid-Zeitschrift 170, 116–123 (1960). https://doi.org/10.1007/BF01525170
Received:
Issue Date:
DOI: https://doi.org/10.1007/BF01525170