Abstract
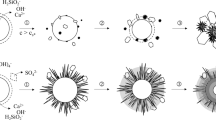
The effect of Mg2+, citrate3−, F− and SO 2−4 on the exchange of45Ca2+ and32PO 3−4 with the mineral phase of bone (ethylenediamine-extracted) was determined under physiological conditions. Mg2+ substituted for Ca2+ at the adherent liquid film (hydration shell), while citrate3− displaced PO 3−4 from both the adherent liquid film and the crystal surface. These bone-seeking elements thus increased the apparent solubility of bone mineral. In contrast, F− markedly reduced the concentration of Ca2+ and PO 3−4 in both the ambient solution and the adherent liquid film, probably by inducing the formation of a CaF2 boundary layer at the crystal surface. There was a net uptake of Ca2+ and PO 3−4 by the solids phase in the presence of Mg2+ and F−, but not in citrate3− solutions. SO 2−4 did not significantly affect the solubility, dissolution, or growth of bone mineral.
Résumé
L'action du Mg2+, du citrate3−, du F− et du SO 2−4 sur les45Ca2+ et32PO 3−4 avec la phase minérale osseuse (extraite de l'éthylènediamine) est déterminée dans des conditions physiologiques. Le Mg2+ se substitue au Ca2+ au niveau de la pellicule liquide adhérente (enveloppe d'hydratation), alors que le citrate3− déplace PO 3−4 , à la fois, de la pellicule liquide adhérente et de la surface cristalline. Ces éléments à affinité pour l'os augmente ainsi la solubilité apparente du minéral osseux. A l'inverse, le F− diminue netterment la concentration de Ca2+ et du PO 3−4 dans la solution environante et dans la pellicule liquide adhérente, en formant probablement une couche de liaison de CaF2 à la surface cristalline. Il y a une absorption nette de Ca2+ et PO 3−4 par la phase solide en présence de Mg2+ et F−, qui ne s'observe pas dans les solutions de citrate. Le SO 2−4 n'affecte pas de façon significative la solubilité, la dissolution ou la croissance du minéral osseux.
Zusammenfassung
Die Wirkung von Mg2+, Citrat3−, F− und SO 2−4 auf den Austausch von45Ca2+ und32PO 3−4 mit dem Mineralanteil von Knochen (Ethylendiaminextraktion) wurde unter physiologischen Verhältnissen verfolgt. Mg2+ substituierte das Ca2+ des anhaftenden Flüssigkeitsfilms (Hydratationsschicht), während Citrat3− das PO 3−4 sowohl vom anhaftenden Flüssigkeitsfilm als auch von der Kristalloberfläche ersetzte. Diese vom Knochen angezogenen Elemente erhöhten demzufolge die scheinbare Löslichkeit des Knochenminerals. Dagegen reduzierte F− die Konzentration von Ca2+ und PO 3−4 wesentlich, sowohl in der umgebenden Lösung als auch im anhaftenden Flüssigkeitsfilm, vermutlich durch Bildung einer CaF2-bindenden Schicht auf der Oberfläche des Kristalls. In Gegenwart von Mg2+ und F− nahm diefeste Phase eindeutig Ca2+ und PO 3−4 auf, was bei Citrat3−-haltigen Lösungen nicht der Fall war. SO 2−4 veränderte weder die Löslichkeit noch die Auflösung oder das Wachstum des Knochenminerals significkant.
Similar content being viewed by others
References
Armstrong, W. D., andL. Singer: Composition and constitution of the mineral phase of bone. Clin. Orthop.38, 179–190 (1967).
Barker, E. S., J. R. Elkington andJ. K. Clark: Studies of the renal excretion of magnesium in man. J. clin. Invest.38, 1733–1745 (1959).
Berman, M.: Computers in biochemical research (R. Stacy, andB. Waxman, eds.), vol. 2, chap. 7. New York: Acad. Press 1965.
—, andE. Shahn: Some formal approaches to the analysis of kinetic data in forms of linear compartmental systems, Biophys. J.2, 290–316 (1962).
Bernstein, D. S., N. Sadowsky, D. M. Hegsted, C. D. Guri, andF. J. Stare: Prevalence of osteoporosis in high-and-low fluoride areas in North Dakota. J. Amer. med. Ass.198, 85–90 (1966).
Chakmakjian, andJ. E. Bethune: Sodium sulfate treatment of hypercalcemia. New Engl. J. Med.275, 862–869 (1966).
Duckworth, J., W. Godden, andG. M. Warnock: The effect of acute magnesium deficiency on bone formation in rats. Biochem. J.34, 97–108 (1940).
Fiske, C. H., andM. A. Logan: Determination of calcium by alkalimetric titration: II. The precipitation of calcium in the presence of magnesium, phosphate and sulfate, with application to the analysis of urine. J. biol. Chem.93, 211–226 (1931).
—, andY. Subba Row: The colorimetric determination of phosphorus. J. biol. Chem.66, 375–400 (1925).
Gill, J. R., Jr., N. H. Bell, andF. C. Bartter: Effect of parathyroid extract on magnesium excretion in man. J. appl. Physiol.22, 136–138 (1967).
Griffithh, G. C., G. Nichols, J. D. Asher andB. Flanagan: Heparin osteoporosis. J. Amer. med. Ass.193, 91–94 (1965).
Jones, K. H., andP. Fourman: Effects of infusions of magnesium and of calcium in parathyroid insufficiency. Clin. Sci.30, 139–150 (1966).
Jowsey, J., R. K. Schenk, andF. W. Reutter: Some results on the effect of fluoride on bone tissue in osteoporosis. J. clin. Endocr.28, 869–874 (1968).
McIntyre, I., S. Hanna, C. C. Booth, andA. E. Read: Intracellular magnesium deficiency in man. Clin. Sci.20, 297–305 (1961).
Neuman, W. F., andM. W. Neuman: The chemical dynamics of bone mineral. Chicago, Ill.: University of Chicago Press 1958.
Pak, C. Y. C., andF. C. Bartter: Ionic interaction with bone mineral. I. Evidence for an isoionic calcium exchange with hydroxyapatite. Biochim. biophys. Acta (Amst.)141, 401–409 (1967a).
——: Ionic interaction with bone mineral. II. The control of Ca2+ and PO 3−4 exchange by univalent cation — Ca2+ substitution at the hydroxyapatite crystal surface. Biochim. biophys. Acta (Amst.)141, 410–420 (1967b).
—, andH. C. W. Skinner: Ionic interaction with bone mineral IV. Varying affinity of synthetic calcium phosphates for Ca2+. Biochem. biophys. Acta (Amst.)165, 274–282 (1968).
Rich, C., J. Ensinck, andP. Ivanovich: The effect of sodium fluoride on calcium metabolism of subjects with metabolic bone diseases. J. clin. Invest.43, 545–556 (1964).
Samiy, A. H. E., J. L. Brown, D. L. Globus, R. H. Kessler, andD. D. Thompson: Interrelation between renal transport systems of magnesium and calcium. Amer. J. Physiol.198, 599–602 (1960).
Author information
Authors and Affiliations
Rights and permissions
About this article
Cite this article
Pak, C.Y.C., Diller, E.C. Ionic interaction with bone mineral. Calc. Tis Res. 4, 69–77 (1969). https://doi.org/10.1007/BF02279107
Received:
Issue Date:
DOI: https://doi.org/10.1007/BF02279107