Summary
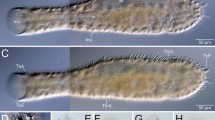
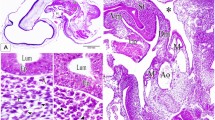
A two-layered glandular tissue occurs on tergites V to X and on the cerci of juvenile specimens of both sexes and of adult females of Blatta orientalis, in place of the usual monolayer of epidermal cells. This gland tissue contains two cell types and secretes a viscous product of water, free amino acids (+ glutamine), oligo- and several polypeptides onto the tergal surface. The structural differentiation of the gland is correlated with secretory activity, both in different molting stages and in different tergites of an individual; maximal values are found in tergites VI und VII on last instar females. Applying quantitative radioautography on the electron microscope level, we found, that although the most common gland cell type contained an abundantly developed rough endoplasmic reticulum and Golgi-apparatus, characteristic of protein secreting cells, not all of them incorporated equally the injected amino acids. This is consistent with an asynchronous secretory cycle, also suggested by biochemical studies. Of great significance is the demonstration that the fine structural elaboration of the cellular organelles involved in protein synthesis cannot be used as a criterion for their ongoing activity. The secretion is discharged into an end-apparatus consisting of a tortuous canal with a brushborder that penetrates the whole gland cell. One unbranched chitinous duct, formed by a “duct carrying cell”, is inserted into the end-apparatus of each gland cell. Occasionally, cell processes exhibiting the typical morphological characteristics of neurosecretory cells are seen in direct contact with gland cells. A defensive function of the secretion which acts by mechanically impairing smaller predatory arthropods was ascertained. To achieve this effect and to allow the preyanimal to escape, the secretion has to be adjusted to a proper viscosity by an adequate dilution. This might be achieved by the second gland cell type, which was not selectively labelled by injected amino acids; this cell type contains an endapparatus, abundant mitochondria, Golgi-apparatuses and small vesicles, but only few profiles of rough endoplasmic reticulum.
Zusammenfassung
Im Bereich der abdominalen Tergite V-X und oberseits and den Zerzi liegt bei Nymphen beider Geschlechter und bei adulten Weibchen von Blatta orientalis statt des einschichtigen Epithels ein zweischichtiges Drüsengewebe vor, welches ein visköses Sekret aus Wasser, freien Aminosäuren (+ Glutamin), Oligo- und zahlreichen Polypeptiden auf die Tergitenoberfläche sezerniert. Die strukturelle Differenzierung des Drüsengewebes ist mit der Sekretionsaktivität korreliert, sowohl während der Ontogenese als auch im Bereich verschiedener Tergite (Maxima: weibliche Subimagines, Tergite VI und VII). Untersuchungen mittels hochauflösender quantitativer Autoradiographie ergaben, daß injizierte Aminosäuren im größten Teil der Drüsenzellen angereichert werden: Markierte Zellen zeigen Radioaktivität im reichlich ausgebildeten rauhen endoplasmatischen Retikulum, Golgi-Apparat, in Sekretgranula und in ihrem Endapparat. Dieser durchsetzt die Drüsenzelle als langer gewundener Kanal mit Bürstensaum, in welchen je eine darüberliegende Gangzelle einen chitinösen Ausführgang inseriert. Die gleichzeitige Anwesenheit von markierten und nicht markierten Zellen mit praktisch gleich stark entwickeltem endoplasmatischem Retikulum und Golgi-Apparat zeigt, daß die morphologische Ausbildung dieser mit der Proteinsekretion befaßten Organellen nicht unbedingt deren Aktivität reflektiert. Vereinzelt stehen Zellfortsätze mit den morphologischen Charakteristika neurosekretorischer Tätigkeit in direktem Kontakt mit Drüsenzellen. Eine Abwehrfunktion des viskösen Sekrets durch bloße mechanische Behinderung kleiner räuberischer Arthropoden wurde sichergestellt, wobei es dem Beutetier gelingt, zu flüchten. Weiters wurde ein zweiter Drüsenzelltyp beobachtet, der mit injizierten Aminosäuren nur schwach markierbar ist, ebenfalls einen Endapparat besitzt, jedoch arm an rauhem endoplasmatischem Retikulum und gleichzeitig reich an Mitochondrien, Golgi-Apparaten und kleinen Vesikeln ist. Die Funktion dieses zweiten Zelltyps ist zwar nicht sichergestellt, möglicherweise reguliert er jedoch die funktionell wichtige Viskosität des Sekretes.
Similar content being viewed by others
Literatur
Akai, H.: Electron microscopical observation on the fibroin formation in the silk gland of the silkworm, Bombyx mori L. Bull. Sericult. Exp. Stn. (Tokyo) 18, 271–282 (1963).
— Micromorphological changes of the glandular cell in the posterior division of the silk gland during the 5th larval instar of the silkworm, Bombyx mori. Bull. Sericult. Exp. Stn. (Tokyo) 18, 475–511 (1964).
— Kobayashi, M.: Sites of fibroin formation in the silk gland in Bombyx mori. Nature (Lond.) 206, 529 (1965).
Alexander, A. J.: Notes on onychophoran behavior. Ann. Natal Museum 14, 35–43 (1957).
Bachmann, L., Salpeter, M. M.: Absolute sensitivity of electron microscope radioautography. J. Cell Biol. 33, 299–305 (1967).
Barbier, R.: Mise en évidence de sphérules et de “vacuoles” cytoplasmiques dans l'hypoderme de Dysdercus fasciatus Sgn. (Hétéroptère Pyrrhocoridae). Étude histologique et cytochimique de ces formations et observation de leur évolution, au cours du cycle cuticulaire, par le microscope électronique. C. R. Acad. Sci. (Paris), Ser. D 266, 2486–2488 (1968).
Beams, H. W., Anderson, E.: Fine structure of “intracellular ductules” in certain glands of the carabid beetle. J. Morph. 109, 159–171 (1961).
— Sekhon, S. S.: Morphological studies on secretion in the silk glands of the caddis fly larvae, Platyphylax designatus Walker. Z. Zellforsch. 72, 408–414 (1966).
Bell, A. L., Peakall, D. B.: Changes in fine structure during silk protein production in the ampullate gland of the spider Araneus sericatus. J. Cell Biol. 42, 284–295 (1969).
Berry, S. J.: The fine structure of the colleterial glands of Hyalophora cecropia (Lepidoptera). J. Morph. 125, 259–280 (1968).
Bristowe, W. S.: The world of spiders. In: New naturalist. London: Collins 1958.
Caro, L. G., Palade, G. E.: Protein synthesis, storage and discharge in the pancreatic exocrine cell. J. Cell Biol. 20, 473–495 (1964).
Couch, E. F., Mills, R. R.: The midgut epithelium of the american cockroach: Acid phosphomonoesterase activity during the formation of autophagic vacuoles. J. Insect Physiol. 14, 55–62 (1968).
Crossley, A. C., Waterhouse, D. F.: The ultrastructure of a pheromonesecreting gland in the male scorpion-fly Harpobittacus australis (Bittacidae, Mecoptera). Tissue & Cell 1, 273–294 (1969a).
— The ultrastructure of the osmeterium and the nature of its secretion in Papilio larvae (Lepidoptera). Tissue & Cell 1, 525–554 (1969b).
Cuénot, L.: Les onychophores. Traité Zool. 6, 3–37 (1949).
Dalton, A. J.: A chrome-osmium fixative for electron microscopy. Anat. Rec. 121, 281 (1955).
Eisner, T.: Chemical defense against predation in arthropods. In: Chemical ecology. New York and London: Academic Press 1970.
— McHenry, F., Salpeter, M. M.: Defense mechanisms of arthropods. XV. Morphology of the quinone-producing glands of a tenebrionid beetle (Eleodes longicollis Lec.) J. Morph. 115, 355–399 (1964).
Faeder, I. R., O'Brien, R. D., Salpeter, M. M.: A re-investigation of evidence for cholinergic neuromuscular transmission in insects. J. exp. Zool. 173, 187–202 (1970).
Fain-Maurel, M. A.: Grains de sécrétion à microtubules dans les glandes salivaires de Limnea stagnalis L. (Gastéropode pulmoné). J. Microscopie 8, 427–430 (1969).
Filshie, B. K., Waterhouse, D. F.: The fine structure of the lateral scent glands of the green vegetable bug, Nezara viridula (Hemiptera, Pentatomidae). J. Microscopie 7, 231–244 (1968).
Forsyth, D. J.: The ultrastructure of the pygidial defense glands of the carabid Pterostichus madidus F. J. Morph. 131, 397–416 (1970).
Gurr, E.: Staining. Practical and theoretical, 1st ed., Baltimore: Williams & Wilkins Co. 1962.
Happ, G. M.: Quinone and hydrocarbon production in the defensive glands of Eleodes longicollis and Tribolium castaneum (Coleoptera, Tenebrionidae). J. Insect Physiol. 14, 1821–1837 (1968).
— Strandberg, J. D., Happ, Ch. M.: The terpene-producing glands of a phasmid insect. Cell morphology and histochemistry. J. Morph. 119, 143–160 (1966).
Jamieson, J. D., Palade, G. E.: Intracellular transport of secretory proteins in the pancreatic exocrine cell. I. The role of the peripheral elements of the Golgi complex. J. Cell Biol. 34, 577–596 (1967a).
— Intracellular transport of secretory proteins in the pancreatic exocrine cell. II. Transport to condensing vacuoles and zymogen granules. J. Cell Biol. 34, 597–615 (1967b).
Kendall, M. D.: The fine structure of the salivary glands of the desert locust Schistocerca gregaria Forskål. Z. Zellforsch. 98, 399–420 (1969).
Kessel, R. G., Beams, H. W.: Electron microscope observations on the salivary gland of the cockroach, Periplaneta americana. Z. Zellforsch. 59, 857–877 (1963).
Kloetzel, J. A., Laufer, H.: Developmental changes in fine structure associated with secretion in larval salivary glands of Chironomus. Exp. Cell Res. 60, 327–337 (1970).
Lawrence, D. F.: Peripatus: a living museum of antiquites. Afr. Wild Life 4, 112–120 (1950).
Locke, M.: The structure and formation of the cuticulin layer in the epicuticle of an insect, Calpodes ethlius (Lepidoptera, Hesperiidae). J. Morph. 118, 461–494 (1966).
— The structure of an epidermal cell during the development of the protein epicuticle and the uptake of molting fluid in an insect. J. Morph. 127, 7–40 (1969).
Manton, S. M., Heatley, N. G.: Studies on the Onychophora. II. The feeding, digestion, excretion, and food storage of Peripatopsis. Phil. Trans. B 227, 411–464 (1937).
Matsuura, S., Motimoto, T., Nagata, S., Tashiro, Y.: Studies on the posterior silk gland of the silkworm, Bombyx mori. II. Cytolytic processes in posterior silk gland cells during metamorphosis from larva to pupa. J. Cell Biol. 38, 589–603 (1968).
McAlister, W. H.: The spitting habit in the spider Scytodes intricata Banks (Family Scytodidae). Texas J. Sci. 12, 17–20 (1960).
Mercer, E. H., Brunet, P. C. J.: The electron microscopy of the left colleterial gland of the cockroach. J. biophys. biochem. Cytol. 5, 257–261 (1959).
Miller, T., Jefferson, R. N., Thompson, W. W.: Sex pheromones of noctuid moths. XI. The ultrastructure of the apical region of cells of the female sex pheromone gland of Trichoplusia ni. Ann. entomol. Soc. Amer. 60, 707–708 (1967).
Moericke, V., Wohlfarth-Bottermann, K. E.: Zur funktionellen Morphologie der Speicheldrüsen von Homopteren. I. Mitt.: Die Hauptzellen der Hauptdrüse von Myzus persicae (Sulz.) Aphididae. Z. Zellforsch. 51, 157–184 (1960).
Morimoto, T., Matsuura, S., Nagata, S., Tashiro, Y.: Studies on the posterior silk gland of the silkworm, Bombyx mori. III. Ultrastructural changes of posterior silk gland cells in the fourth larval instar. J. Cell Biol. 38, 604–614 (1968).
Nayler, L. S.: The structure and function of the posterior abdominal glands of the cockroach Pseudoderopeltis bicolor (Thunb.). J. entomol. Soc. S. Afr. 27, 62–66 (1964).
Noirot, C., Noirot-Timothée, C.: Organisation de la glande sternale chez Calotermes flavicollis F. (Insecta, Isoptera). Étude au microscope électronique. C. R. Acad. Sci. (Paris), Ser. D 260, 6202–6204 (1965).
Palade, G. E.: Intracisternal granules in the exocrine cells of the pancreas. J. biophys. biochem. Cytol. 2, 417–422 (1956).
Perotti, M. E.: Filamentous structures in the male accessory glands of Drosophila. 7ème Int. Congr. Electron Micr. (Grenoble), Proc. III, 213–214 (1970).
Plattner, H.: Funktionelle Organisation eines Protein-sezernierenden Insektenepithels. Naturwissenschaften 58, 325–326 (1970).
Rau, P.: The biology of the roach, Blatta orientalis Linn. Trans. Acad. Sci. St. Louis 25, 57–79 (1924).
Rinterknecht, E., Lévi, P.: Étude au microscope électronique du cycle cuticulaire au cours du 4ème stade larvaire chez Locusta migratoria. Z. Zellforsch. 72, 390–407 (1966).
Ross, R., Benditt, E. P.: Wound healing and collagen formation V. Quantitative electron microscope radioautographic observations of proline-3H utilization by fibroblasts. J. Cell Biol. 27, 83–106 (1965).
Roth, L. M., Stahl, W. H.: Tergal and cercal secretion of Blatta orientalis L. Science 123, 798–799 (1956).
— Wills, E. R.: A study of cockroach behavior. Amer. Midland Naturalist 47, 66–129 (1952).
Salpeter, M. M.: H3-proline incorporation into cartilage: Electron microscope autoradiographic observations. J. Morph. 124, 387–422 (1968).
— Bachmann, L.: Autoradiography with the electron microscope. A procedure for improving resolution, sensitivity and contrast. J. Cell Biol. 22, 469–477 (1964).
Schnepf, E., Wenneis, W., Schildknecht, H.: Über Arthropoden-Abwehrstoffe XLI. Zur Explosionschemie der Bombardierkäfer (Coleoptera, Carabidae). IV. Zur Feinstruktur der Pygidialwehrdrüsen des Bombardierkäfers (Brachynus crepitans L.). Z. Zellforsch. 96, 582–599 (1969).
Sjöstrand, F. S., Hanzon, V.: Ultrastructure of Golgi apparatus of exocrine cells of mouse pancreas. Exp. Cell Res. 7, 415–429 (1954a).
— Electron microscopy of the Golgi apparatus of the exocrine pancreas cells. Experientia (Basel) 10, 367–369 (1954b).
Slifer, E. H.: The structure of arthropod chemoreceptors. Ann. Rev. Entomol. 15, 121–142 (1970).
Smith, D. S.: Insect cells. Their structure and function, 1st ed., Edinburgh: Oliver & Boyd 1968.
Stein, G.: Über den Feinbau der Mandibeldrüse von Hummelmännchen. Z. Zellforsch. 57, 719–736 (1962).
— Über den Feinbau der Duftdrüsen von Feuerwanzen (Pyrrhocoris apterus L., Geocorisae). I. Zur funktionellen Morphologie der Drüsenzelle. Z. Zellforsch. 74, 271–290 (1966).
— Über den Feinbau der Duftdrüsen von Feuerwanzen (Pyrrhocoris apterus L., Geocorisae). Die zweite larvale Abdominaldrüse. Z. Zellforsch. 79, 49–63 (1967).
— Schumacher, R.: Über den Feinbau der Duftdrüsen von Baumwollwanzen (Dysdercus intermedius Dist., Pyrrhocoridae). Z. Naturforsch. 24b, 148–149 (1969).
— Walker, S.: Über den Feinbau der Duftdrüsen des Rückenschwimmers Notonecta glauca L. (Notonectidae). Z. Naturforsch. 25b, 562–563 (1970).
Steinbrecht, R. A.: Feinstruktur und Histochemie der Sexualduftdrüse des Seidenspinners Bombyx mori L. Z. Zellforsch. 64, 227–261 (1964).
— Op-art-bodies. A new class of periodically layered cell inclusions observed in crayfish epidermis cells. 4th Reg. Conf. El. Micr. (Rom) Proc. II, 221–222 (1968).
Stock, A., O'Farrell, A. F.: Cercal spinning glands in the cockroach, Blattella germanica. Aust. J. Sci. 17, 64 (1954).
Stuart, A. M., Satir, P.: Morphological and functional aspects of an insect epidermal gland. J. Cell Biol. 36, 527–549 (1968).
Tashiro, Y., Morimoto, T., Matsuura, S., Nagata, S.: Studies on the posterior silk gland of the silkworm, Bombyx mori. I. Growth of posterior silk gland cells and biosynthesis of fibroin during the fifth larval instar. J. Cell Biol. 38, 574–588 (1968).
Tulloch, G. S., Shapiro, J. E., Hershenov, B.: The ultrastructure of the metasternal glands of ants. Bull. Brooklyn entomol. Soc. 57, 91–101 (1962).
Venable, J. H., Coggeshall, R.: A simplified lead citrate stain for use in electron microscopy. J. Cell Biol. 25, 407–408 (1965).
Verhoeff, K. W.: Chilopoda. In: Klassen und Ordnungen des Tierreiches (H. G. Bronn, ed.), Bd. 5, S. 351–365. Leipzig: Akademische Verlagsgesellschaft 1925.
Voigt, W. H.: Zur funktionellen Morphologie der Fibroin- und Sericin-Sekretion der Seidendrüse von Bombyx mori L. I. Mitteilung: Der proximale Abschnitt der Seidendrüse. Z. Zellforsch. 66, 548–570 (1965a).
— Zur funktionellen Morphologie der Fibroin- und Sericin-Sekretion der Seidendrüse von Bombyx mori L. II. Mitt. Der mediale Abschnitt der Seidendrüse. Z. Zellforsch. 66, 571–582 (1965b).
Wohlfarth-Bottermann, K. E.: Die Kontrastierung tierischer Zellen und Gewebe im Rahmen ihrer elektronenmikroskopischen Untersuchung an ultradünnen Schnitten. Naturwissenschaften 44, 287–288 (1957).
— Moericke, V.: Zur funktionellen Morphologie der Speicheldrüsen von Homopteren. III. Mitt. Die Nebendrüsen von Myzus persicae (Sulz.), Aphididae. Z. Zellforsch. 52, 346–361 (1960).
Author information
Authors and Affiliations
Rights and permissions
About this article
Cite this article
Plattner, H., Salpeter, M., Carrel, J.E. et al. Struktur und Funktion des Drüsenepithels der postabdominalen Tergite von Blatta orientalis . Z.Zellforsch 125, 45–87 (1972). https://doi.org/10.1007/BF00306841
Received:
Issue Date:
DOI: https://doi.org/10.1007/BF00306841