Abstract
This study seeks to provide evidence for deciding whether or not a new preparation for the treatment of diabetes should be included in the benefit list of social health insurance. A discrete-choice experiment (DCE) was conducted in Germany to measure preferences for modern insulin therapy using long-acting insulin analogue “insulin detemir” in comparison to NPH insulin. The DCE contains two price attributes, co-payment and increased contributions to health insurance, as well as four properties of the insulin, i.e. risk of hypoglycemia, weight gain, need for preparing the insulin before injection, and flexibility in time of the injection. Of the 1,110 individuals interviewed in 2007, 202 suffered from type 1, 154 from insulin-treated type 2, and 152 from insulin-naive type 2 diabetes. This allows to compare ex-ante and ex-post willingness-to-pay (WTP). Non-diabetics and insulin-naive diabetics exhibit higher WTP values through co-payment, while affected type 1 and insulin-treated type 2 diabetics have higher WTP through increased contributions. However, WTP values exceed the extra treatment cost in both financing alternatives, justifying inclusion of the new drug in the benefit list from a cost-benefit point of view.
Similar content being viewed by others
Avoid common mistakes on your manuscript.
1 Einleitung
Die Gesundheitsausgaben (und insbesondere die Arzneimittelausgaben) nehmen in fast allen Industrieländern zu. So stieg der Anteil der Arzneimittel an den Ausgaben allein der deutschen Gesetzlichen Krankenversicherung (GKV) zwischen 2007 und 2012 von € 27 Mrd. auf € 29 Mrd. (dies entspricht jeweils ca. 1,1 % des Bruttoinlandsprodukts) [1]. In den USA wuchs dieser Anteil von 9 % der Gesundheitsausgaben insgesamt im Jahre 1996 auf 12 % im Jahre 2009 [2]. Um diesen Anstieg zu dämpfen, führten mehrere Länder zusätzlich das Kosten-Wirksamkeits-Kriterium für neue Arzneimittel ein. An ihm orientieren sich nicht nur das Institut für Qualitätssicherung und Wirtschaftlichkeit im Gesundheitswesen (IQWIG), sondern auch z. B. die australische Medicare Payment Advisory Commission (MEOPAC) und das britische National Institute for Clinical Excellence (NICE). Entsprechend müssen seit 2007 neue Arzneimittel für die Aufnahme in den Leistungskatalog der GKV nicht nur Anforderungen bezüglich Sicherheit und Wirksamkeit, sondern auch der Kostenwirksamkeit erfüllen.
Der vorliegende Beitrag hat zum Ziel, Entscheidungsgrundlagen für die Aufnahme eines neuen Arzneimittels in den Leistungskatalog der GKV bereitzustellen. Der konkrete Fall betrifft ein langwirksames Insulinanalogon; das bisherige Standardpräparat ist das Neutral Protamine Hagedorn (NPH) Insulin, ein Humaninsulin. Das neue Arzneimittel verspricht eine Reihe von medizinischen Vorteilen, insbesondere ein geringeres Unterzuckerungsrisiko, das Ausbleiben einer Gewichtszunahme (oder sogar eine Gewichtsabnahme), eine einfachere Aufbereitung und mehr Flexibilität in Bezug auf den Zeitpunkt der Injektion (auf die einschlägigen klinischen Studien wird im Abschn. 3 verwiesen). Diese potenziellen Vorteile sind mit zusätzlichen Kosten von € 226 pro Jahr und Diabetiker verbunden. Studien zur Kosteneffektivität von Insulinanalogon im Vergleich zur Alternative Humaninsulin NPH kamen zu unterschiedlichen, mehrheitlich jedoch positiven Ergebnissen. Nur gerade eine Studie [3] kommt zum Schluss, das Arzneimittel sei nicht kostenwirksam, während es z. B. in [4] als kostenwirksam für Diabetiker vom Typ 2Footnote 1 in den USA eingestuft wird.
Das vorliegende Präparat ist aus zwei Gründen von besonderem Interesse. Zum einen ist die Prävalenz von Diabetes in den Industrieländern höher als je zuvor und nimmt weiterhin rasch zu. So sagt die Weltgesundheitsorganisation (WHO) für den Zeitraum zwischen 2000 und 2030 eine Zunahme der Diabetikerzahl von 170 auf 360 Mio. Menschen voraus [6, 7]. In den USA allein wird 2034 mit 44,1 Mio. Patienten gerechnet – gegenüber 23,7 Mio. im Jahre 2009 [8], verbunden mit einer Zunahme der Behandlungskosten von USD 113 Mrd. auf USD 336 Mrd. Die Diabetes-Prävalenz liegt in Deutschland zwischen 6 und 10 % in der Altersgruppe 40–59 und 18 bis 28 % in der Altersgruppe der über 60-Jährigen [9]. Zweitens empfahl das IQWIG in mehreren Fällen, sowohl kurz- wie langwirksame Insulinanaloga vom Leistungskatalog der GKV wegen mangelnder Kostenwirksamkeit auszuschließen [10, 11]. Doch diese Empfehlungen missachten die Präferenzen der (potenziellen) Patienten. Mehrere Eigenschaften des Arzneimittels, die aus der Sicht der Patienten innovativ sein könnten, werden vernachlässigt oder als therapeutisch irrelevant beurteilt. Doch mit dem Instrument der sog. Wahlexperimente (Discrete-Choice-Experiments, DCE) lassen sich die Präferenzen der (potenziellen) Patienten durchaus ermitteln. Enthält das Experiment ein Preisattribut, kann man zudem die Zahlungsbereitschaft für positiv gewertet und Kompensationsforderungen für negativ bewertete Eigenschaften des Präparats ermitteln. Für das Präparat als Ganzes ergibt dies eine Schätzung des (Dis)Nutzens in Geldeinheiten und eröffnet damit die Möglichkeit, mit einer echten Kosten-Nutzen-Analyse den Goldstandard der Gesundheitsökonomie umzusetzen. Aus der Sicht der GKV-Versicherten (sowohl der potenziellen wie auch der aktuellen Patienten) ist die Aufnahme des neuen Präparats dann gerechtfertigt, wenn die ermittelte Zahlungsbereitschaft die zusätzlichen Kosten der Behandlung übertrifft.
Die vorliegende Studie präsentiert ein Wahlexperiment vom DCE-Typ, bei dem ein Insulinanalogon dem herkömmlichen NPH Insulin gegenübergestellt wird. An diesem im Herbst 2007 durchgeführten DCE nahmen 1.110 Mitglieder der deutschen GKV teil, davon sind 602 Teilnehmer Nicht-Diabetiker, 202 leiden an Diabetes vom Typ 1, 154 an Diabetes vom Typ 2 und werden mit Insulin behandelt, und 152 Teilnehmer gehören zur Gruppe der Insulin-naiven Diabetiker vom Typ 2. So lässt sich die ex-ante Zahlungsbereitschaft von Nichtbetroffenen (Nicht-Diabetiker sowie Insulin-naive Diabetiker) von der ex-post Zahlungsbereitschaft der Betroffenen (Diabetiker vom Typ 1 und Insulin-abhängige vom Typ 2) unterscheiden.
Die Auswertung von klinischen Studien ergab vier Attribute zur Beschreibung der Therapie mit dem Insulinanalogon im Vergleich mit dem NPH Insulin: Risiko der Unterzuckerung, Gewichtszunahme während der ersten sechs Monate der Behandlung, Notwendigkeit der Aufbereitung durch Schwenken (nicht Schütteln) des Insulins vor der InjektionFootnote 2 und Flexibilität bezüglich des Zeitpunkts der Injektion. Zwei weitere Attribute definieren die Finanzierung der Therapie, nämlich durch die Patienten selbst (Zuzahlung) und über einen erhöhten eigenen GKV-Beitrag. Auf diese Weise lässt sich prüfen, ob das neue Präparat ein günstiges Nutzen-Kosten-Verhältnis aufweist unabhängig davon, ob der Versicherungsschutz die Zahlungsbereitschaft verstärkt oder nicht.
Die vier zentralen Fragestellungen und die jeweiligen Hypothesen lauten: (1) Gibt es eine positive Zahlungsbereitschaft für langwirksames Insulinanalogon unter den Mitgliedern der GKV? Die zu testende Hypothese H1 besagt, dass die Zahlungsbereitschaft für Insulinanalogon im Vergleich zum herkömmlichen Humaninsulin positiv ausfällt. (2) Falls H1 bestätigt werden kann, welche Attribute tragen zur Zahlungsbereitschaft in welchem Maße bei? Hypothese H2 besagt, dass eine Senkung des Unterzuckerungsrisikos die höchste Zahlungsbereitschaft aufweist, gefolgt von einer geringeren Gewichtszunahme und mehr Flexibilität bezüglich des Injektionszeitpunktes. Die Zahlungsbereitschaft dafür, dass das Präparat vor der Injektion nicht geschwenkt werden muss, wird als gering und nichtsignifikant eingestuft. (3) Besteht eine Heterogenität der Präferenzen zwischen den Nichtbetroffenen (Nicht-Diabetiker und Insulin-naive Diabetiker vom Typ 2) und den Betroffenen (Diabetiker vom Typ 1 und Insulin-Abhängige vom Typ 2)? Hypothese H3 besagt, dass diese Heterogenitäten signifikant sind. (4) Ergibt sich ein günstiges Nutzen-Kosten-Verhältnis für das neue Arzneimittel unabhängig davon, ob seine Kosten allgemein durch einen erhöhten GKV-Beitrag oder durch eine Zuzahlung der Patienten gedeckt werden? H4 bejaht dies, wobei Nichtbetroffene und Diabetiker, die nicht mit Insulin behandelt werden eine höhere Zahlungsbereitschaft aufweisen, falls die Finanzierung durch die Patienten selbst mittels Zuzahlung erfolgt, wogegen die Zahlungsbereitschaft von mit Insulin behandelten Patienten höher ist bei einer Finanzierung durch einen erhöhten GKV-Beitrag.
2 Literaturübersicht
2.1 Studien zur Kostenwirksamkeit
Die verfügbaren Kostenwirksamkeitsstudien von Insulinanalogon verwenden die Quality-Adjusted Life Years (QALYs) als Nutzenmaß und die Incremental Cost Effectiveness Ratio (ICER) als Evaluationskriterium. Im Folgenden geben wird eine Übersicht zu Kostenwirksamkeitsstudien bez. Insulinanaloga. Zwei Untersuchungen [12, 13] konzentrieren sich auf britische Diabetiker vom Typ 1. Sie kommen auf 0,09 und 0,66 zusätzliche QALYs und damit auf ICER-Werte von GBP 19.285 und GBP 2.500, die dem Schwellenwert des NICE von maximal £ 30.000 vollauf genügen. Diese Schätzungen wurden für Dänemark bestätigt [14], mit einer ICER von DRK 55.867 bzw. GBP 6.600. Die international vergleichende Studie [15] kommt zum Schluss, dass Insulinanalogon wahrscheinlich die dominante Behandlungsalternative für Patienten vom Typ 1 in Belgien, Deutschland und Spanien darstellt und immer noch hoch kostenwirksam in Frankreich und Italien abschneidet, mit einer ICER von € 415 und € 2.604 pro QALY. Eine weitere international vergleichende Studie [15] bestätigt Insulinanalogon als kostenwirksame Behandlungsmethode für Dänemark, Schweden, Finnland und die Niederlande. Im Falle der USA erwies sich das Arzneimittel ebenfalls als kostenwirksam [16] dank einer gesenkten Inzidenz akuter Unterzuckerung und kostspieliger chronischer Komplikationen wie z. B. diabetische Nephropathie. Eine weitere Studie [17] kommt zum gleichen Schluss auf Grund einer ICER von USD 14.974. Nicht ganz so günstig war das Ergebnis einer kanadischen Studie [18] mit einer ICER von CAD 24.389 je QALY.
In Bezug auf Patienten vom Typ 2 sind die Schätzungen nicht ganz so eindeutig. Die Autoren von Valentine et al. [4] kommen auf eine ICER von USD 6.269 und Tunis et al. [18] auf CAD 18.677. Mit einem extremen Wert von USD 387.729 kommt [3] sogar zum Schluss, dass langwirksame Insulinanaloga zumindest für die USA keine effiziente Verwendung der Mittel darstellen.
2.2 Untersuchungen der Zahlungsbereitschaft
Trotz ihrer großen Beliebtheit stellt die Kostenwirksamkeit aus ökonomischer Sicht kein zufriedenstellendes Kriterium dar, und dies aus zwei Gründen. Zum einen messen QALYs nur gerade den resultierenden Gesundheitszustand und vernachlässigen damit Eigenschaften des Behandlungsprozesses wie Angst, Schmerzen, Isolation und Trennung von den Angehörigen. Zweitens kann man die Mittel, die man zu Gunsten der Gesundheit aufwendet, keinen anderen konkurrierenden Verwendungszwecken gegenüberstellen. Drittens gibt das Maß der Kostenwirksamkeit lediglich darüber Auskunft, wie im Umfang vorgegebene (meist öffentliche) Mittel für das Gesundheitswesen für konkurrierende Zwecke verwendet werden sollen. Es liefert jedoch kein Kriterium für die Beantwortung der Frage, ob dem Gesundheitswesen mehr oder weniger Mittel zu Lasten bzw. zu Gunsten beispielsweise der Ausbildung zukommen sollen. Konkret werden durch QALYs die Präferenzen von BürgerInnen nicht abgebildet, die eine Ausweitung der Gesundheitsausgaben befürworten, mit der Folge, dass der geforderte ICER-Schwellenwert (z. B. die GBP 30.000/QALY des NICE) zu niedrig angesetzt ist. Demgegenüber ermöglicht die Messung der Zahlungsbereitschaft das Abwägen des zusätzlichen Nutzens einer neuen Therapie (Grenznutzen) gegen ihre zusätzlichen Kosten (Grenzkosten), wobei beide Größen in Geld ausgedrückt werden.
Die erste Zahlungsbereitschafts-Studie über eine Insulintherapie bezieht sich auf Australien [19]. Sie vergleicht Insulin lispro, das erste kurzwirksame Insulinanalogon, mit neutralem (herkömmlichem) Insulin, wobei der Ansatz der bedingten Bewertung (sog. Contingent Valuation) zur Anwendung kam. Die Teilnehmer am Experiment erhielten zuerst eine Beschreibung der beiden Insulinarten und mussten eine davon auswählen. Dann wurden sie mit immer höheren zu bezahlenden Preisen konfrontiert, um so ihre maximale Zahlungsbereitschaft für die gewählte Alternative zu bestimmen. Die Stichprobe enthält Diabetiker vom Typ 1 und mit Insulin Behandelte vom Typ 2. Dasselbe Verfahren wurde verwendet, um die Zahlungsbereitschaft für das schnellwirksame Insulinanalogon Humalog Mix 25 zu schätzen [20]. Diesmal enthält die Stichprobe nicht nur Diabetiker, sondern auch die Steuerzahler aus der allgemeinen Bevölkerung. Schließlich wird in [21] die Zahlungsbereitschaft von Diabetikern vom Typ 1 und Typ 2 (sowohl Insulin-naive wie auch Insulin-abhängige) für inhaliertes Insulin analysiert, wiederum unter Verwendung der Contingent Valuation in Kombination mit immer höheren Preisen.
Im Gegensatz zur Contingent Valuation dürfen in einem DCE sämtliche Eigenschaften („Attribute“ der Vergleichsalternative) immer wieder neue Werte annehmen, wenn die Teilnehmer jeweils zwischen dem Status quo und der Alternative wählen. Beim ersten DCE bezüglich einer Insulintherapie wurde das Insulinanalogon Humalog Mix 25 mit dem kurzwirksamen Humaninsulin Humulin 30/70 verglichen [22]. In fünf europäischen Ländern ergab sich eine statistisch signifikante (zusätzliche) Zahlungsbereitschaft für das neue Präparat. Die Präferenzen für Diabetesbehandlung von Patienten vom Typ 2 war Gegenstand eines anderen, diesmal Internet-basierten DCE [23], mit besonderer Betonung der Faktoren, welche die Therapietreue beeinflussen. Schließlich gibt es Wahlexperimente [24, 25], welche die orale Einnahme der Injektion durch den Patienten gegenüberstellen. Den Autoren [25] zufolge stuften die Teilnehmer am Experiment die Injektion als akzeptabel ein, sobald sie im Zuge der Gewöhnung eine psychologische Barriere überwunden hatten. Die erste und bisher einzige DCE-Studie zu langwirksamem Insulinanalogon untersucht Präferenzen von Typ-1 und mit Insulin behandelten Typ-2-Diabetikern im Vereinigten Königreich [26].
3 Das Experiment
3.1 Entwicklung des Fragebogens, Prätest und Design
Zur Entwicklung des Fragebogens wurde einerseits auf die Erfahrung der Autoren aus früheren DCE-Studien, andererseits auf das Fachwissen von Diabetologen zurückgegriffen. Der Fragebogen besteht aus vier Teilen.
- Teil 1::
-
Das Interview beginnt mit Fragen zur Gesundheit (allgemeiner Gesundheitszustand, regelmäßige Einnahme von Arzneimitteln, chronische Krankheiten, Diabetes, Body-Mass-Index BMI) sowie zur Krankenversicherung (jährlicher eigener GKV-Beitrag, Zusatzversicherungen). Diese Fragen sind für alle Teilnehmer identisch.
- Teil 2::
-
Der Rest des Interviews unterscheidet zwischen Nicht-Diabetikern, Insulin-behandelten Diabetikern und Insulin-naiven Diabetikern. Den Nicht-Diabetikern werden detaillierte Informationen über Diabetes und seine Behandlung vermittelt, damit sie sich in die Lage eines Patienten versetzen konnten. Sie wurden auch mit Hilfe einer visuellen Analogskala nach ihrer (subjektiven) Wahrscheinlichkeit befragt, im Verlauf ihres Lebens selbst Insulin-abhängig zu werden (mit Werten von 0 % „Ich werde nie zu einem Insulin-abhängigen Diabetiker“ bis 100 % „Ich werde dies mit Sicherheit“). Mit Insulin behandelte Patienten wurden gebeten, über den Verlauf ihrer Krankheit, ihre Insulinbehandlung sowie allfällige Nebenwirkungen Auskunft zu geben. Die Insulin-naiven Patienten erhielten ebenfalls Informationen zum Diabetes und seiner Behandlung und machten Angaben zur Dauer ihrer Krankheit, zu ihrer Behandlung sowie allfälligen Nebenwirkungen. Sie trugen auch (wiederum auf einer visuellen Analogskala) ihre subjektiv geschätzte Wahrscheinlichkeit ein, im Verlauf ihres Lebens von Insulin abhängig zu werden.
- Teil 3::
-
Dieser Teil ist wiederum identisch für alle Befragten. Um sie auf das DCE vorzubereiten, erhielten sie ausführliche Erklärungen der verwendeten Attribute, mit besonderer Betonung der beiden Finanzierungsmodalitäten „Zuzahlung“ und „Erhöhter GKV-Beitrag“. Dank des Direktkontaktes mit den Interviewern hatten sie die Möglichkeit, Fragen zu stellen und zusätzliche Erklärungen zu verlangen, was zugegebenermaßen zum Risiko einer Rekodierung führt, indem manche Teilnehmer ihre Angaben unter dem Einfluss des Interviewers anpassen. Darauf wurde das in der herkömmlichen Therapie verwendete Insulin beschrieben (mittels der Status-quo-Karte). Die Teilnehmer am Experiment wurden schließlich achtmal (s. u.) gebeten, zwischen dem Status quo und einem Insulin mit veränderten Ausprägungen der Attribute (dargestellt auf Alternativen-Karten) zu wählen.
- Teil 4::
-
Zum Schluss werden die Befragten um Angaben zu sozioökonomischen Eigenschaften (Alter, Geschlecht, Ausbildung, Wohnort) gebeten. Um das Risiko eines Ausscheidens aus dem Experiment möglichst gering zu halten, wurde die Frage zum monatlichen Netto-Haushaltseinkommen an den Schluss gestellt; die Angaben waren auf Anraten des Befragungsinstituts in eine visuelle Analogskala einzutragen, um jeden Bezug zu einer steuerlichen Erhebung zu vermeiden.
3.2 Attribute
Obwohl für die Therapie sowohl kurz- als auch langwirksames Insulin nötig ist, beschränkt sich diese Untersuchung auf langwirksames Insulin. Die geltenden Behandlungsrichtlinien sehen langwirksames NPH Insulin für die Grundversorgung mit Insulin vor. Diese Art der Therapie definiert den konstant gehaltenen Status quo, der durch eine spezifische Kombination von Ausprägungen der vier Attribute charakterisiert ist. Veränderungen in den Ausprägungen der vier Attribute dienen dazu, das Insulinanalogon vom herkömmlichen langwirksamen NPH Insulin zu unterscheiden:
Das Hypoglykämie- bzw. Unterzuckerungsrisiko (Zucker, vgl. Tab. 1) ist eine zentrale Nebenwirkung der Insulintherapie. Seine Inzidenz hängt vom Individuum, der nötigen Insulindosis, den individuellen Gewohnheiten und der Aufbereitung des Insulins ab. Die mittlere Anzahl von Unterzuckerungen wird auf 1 bis 2 pro Woche geschätzt (auf Grund von [27] und Gesprächen mit Diabetologen). Bei einem Zeithorizont von bis zu sechs Monaten (vgl. das Attribut Gewicht) ergibt dies ein Risiko von 100 % im Status quo [1−(1−q)24≈1, bei einer Wahrscheinlichkeit von q>0,5 pro Woche mindestens eine Unterzuckerung zu erleiden]. Die Mehrzahl der Untersuchungen [28–37] und Meta-Analysen [18, 38–45] lassen eine niedrigere Inzidenz mit einem Insulinanalogon als mit NPH Insulin vermuten. Eine Untersuchung [46] ergab keinen erkennbaren Unterschied in der Häufigkeit der Unterzuckerung, während die Resultate einer weiteren Studie nicht eindeutig ausfallen [47]. Eine Cochrane-Studie [48] kommt zum Schluss, dass die Behandlung mit Insulinanalogon mit weniger Unterzuckerungen (auch während der Nacht) verbunden ist als jene mit NPH Insulin. Das Ausmaß der Reduktion unterscheidet sich allerdings je nach Studie und wird auf über 50 % [43], 22 % [32] und 18 % [29] geschätzt. Das IQWIG hält in seinem Schlussbericht [49] fest, dass Insulinanalogon das Risiko schwerer Unterzuckerungen für Diabetiker vom Typ 2 beseitigt (0,0 % gegenüber NPH: 2,1 %), und das Risiko leichter Unterzuckerung signifikant senkt [57,0 % gegenüber NPH: 78,2 %, OR (Odds Ratio) = 0,37] ebenso das Risiko von Unterzuckerung in der Nacht [26,2 % gegenüber NPH: 44,1 %, OR = 0,45]. Bezüglich Patienten vom Typ 1 hält der Abschlussbericht des IQWIG [10] fest, dass bei gemeinsamer Betrachtung der Blutzuckersenkung und der schweren nächtlichen Hypoglykämien ein Hinweis auf einen Unterschied zugunsten von Insulin Detemir besteht:
„Für den Vergleich von Insulin Detemir gegenüber NPH-Insulin, jeweils einmal (zu Studienbeginn) oder zweimal täglich (ggf. im Studienverlauf), zeigte sich bei gemeinsamer Betrachtung der Blutzuckersenkung und der schweren nächtlichen Hypoglykämien ein Hinweis auf einen Unterschied zugunsten von Insulin Detemir. Bei der Interpretation der Ergebnisse ist allerdings die durch die Anwendungsmodalitäten des Basalinsulins bedingte fehlende Übertragbarkeit auf die deutsche Behandlungssituation zu beachten. Bezüglich nicht schwerer (nächtlicher) Hypoglykämien zeigte sich ein solcher Hinweis nicht.“ [IQWIG (2010), „Langwirksame Insulinanaloga zur Behandlung des Diabetes mellitus Typ 1“, Abschlussbericht A05–10, S. vii].
Deshalb wird im Weiteren ein konservativer Wert von 30 % (im Vergleich zu NPH Insulin) für die Risikosenkung durch das Insulinanalogon unterstellt. Da die statistische Inferenz eine genügend große Spanne der Ausprägungen verlangt, gibt das DCE auch Reduktionen von 75 und 50 % im Vergleich zu NPH Insulin vor. Diese Vorgaben sind zugegebenermaßen unrealistisch und könnten die Teilnehmer bewegen, aus dem Experiment auszuscheiden. Andererseits sind große Spannweiten in den Ausprägungen der Attribute nötig, um die Teilnehmer zu veranlassen, zwischen dem Status quo und der Alternative mehrfach hin- und herzuwechseln. Würden sie hingegen überwiegend im Status quo verharren (bzw. fast immer die Alternative wählen), wäre der Informationsgewinn vergleichsweise klein. Schwere Fälle von Unterzuckerung können zum Verlust des Bewusstseins und sogar zum Tode führen. Entsprechend kommen die Studien [23] und [25] zum Schluss, dass Patienten vom Typ 1 und 2 die höchste Zahlungsbereitschaft für die Vermeidung der Unterzuckerung haben, gefolgt von der Vermeidung der Gewichtszunahme (vgl. Hypothese H2.1 in Abschn. 5).
Die Gewichtszunahme (Gewicht) bedeutet für Diabetiker vom Typ 2 ein großes Problem, denn 80 % von ihnen leiden unter Übergewicht [50]. Entsprechend ist ihr BMI signifikant höher als in der deutschen Bevölkerung allgemein [51]. Die herkömmliche Insulintherapie macht die Sache noch schlimmer, denn besonders während der ersten paar Monate nehmen die Patienten zu. Es ist mit einer mittleren Gewichtszunahme von 2,5 kg in sechs Monaten zu rechnen [52], dieser Wert beschreibt den Status quo. Insulinanalogon verringert diese Gewichtszunahme [36, 37, 40–42, 44, 53–57]. Es kann sogar eine Abnahme von bis zu 1 kg herbeiführen [27, 34, 38, 43, 45, 58–61]. Diese Ergebnisse begründen die Vorgabe einer Gewichtszunahme von 0 kg für das Insulinanalogon, verglichen mit Alternativwerten von +2,5 (Status quo), 0 und −1 kg. Eine verringerte Gewichtszunahme dürfte mit einer höheren Zahlungsbereitschaft verbunden sein als das Attribut Flexibilität (s. u.), dessen Wertung gemäß [22] vergleichsweise niedrig (doch signifikant positiv) ausfällt (vgl. Hypothese H2.2 in Abschn. 5).
Die Art der Aufbereitung des Insulinpräparats (Schwenken) ist das dritte Attribut. Vor jeder Injektion muss NPH Humaninsulin geschwenkt (nicht geschüttelt!) werden, um eine gleichmäßige Auflösung und damit die richtige Menge Insulin bei der Injektion zu gewährleisten. Dies definiert den Status quo (vgl. Tab. 1). Ungenügendes Schwenken bringt die Gefahr mit sich, dass eine suboptimale Menge Insulin injiziert wird, mit der Folge einer ungenügenden Stabilisierung der Blutzucker-Konzentration [62]. Das Insulinanalogon kann sofort, ohne Schwenken, gespritzt werden [63]. Der Vorbericht des IQWIG [49] anerkennt dieses Attribut nicht als Innovation, weil es die medizinisch definierten Endpunkte nur indirekt berührt. Aus Patientensicht hingegen könnte es aber durchaus von Bedeutung sein, denn unter Zeitdruck kann es zu ungenügendem Schwenken kommen, was Auswirkungen auf die Wirksamkeit des Präparats haben würde. Das DCE enthält die ,Ausprägungen „1“ (Alternative, Schwenken unnötig) und „0“ (Status quo Schwenken nötig). Die entsprechenden Ausprägungen („1“ kein Schwenken „0“ sonst) werden im DCE und in der Schätzung der Gleichung (9) verwendet. Da es zu diesem Attribut keine Untersuchungen der Zahlungsbereitschaft gibt und das IQWIG in seinem Vorbericht [49] keinen innovativen Gehalt erkennt, wird eine Zahlungsbereitschaft von Null erwartet (vgl. Hypothese H2.3 in Abschn. 5).
Die Flexibilität (Flexibilität) in Bezug auf den Zeitpunkt der Injektion (vgl. wiederum Tab. 1) ist ein weiterer Unterschied zwischen den beiden Arten von Insulin. Das Humaninsulin erreicht seine maximale Wirkung meist nach wenigen Stunden [64]. Dies bedingt, dass die Injektion beim Zubettgehen ziemlich genau um 22 Uhr erfolgen muss, um eine Insulin-Insuffizienz am frühen Morgen danach zu vermeiden (Status quo). Das Insulinanalogon hat ein anderes Zeitprofil, indem seine höchste Wirksamkeit erst später eintritt [40, 65]. Dies ermöglicht den Patienten, das Insulin auch vor 22 Uhr zu spritzen, insbesondere zwischen dem Abendessen und dem Zubettgehen. Allerdings sollte der einmal gewählte Zeitpunkt beibehalten werden. Das Insulinanalogon wird im DCE sowie in der Gleichung (9) mit den Ausprägungen „1“ (Flexibilität) und „0“ (sonst) beschrieben. Für dieses Attribut wird eine geringe positive Zahlungsbereitschaft erwartet (vgl. Hypothese H2.2 in Abschn. 5).
Die letzten beiden in der Tab. 1 aufgeführten Attribute beziehen sich auf die Art der Finanzierung, entweder individuell mittels Zuzahlung durch die Diabetiker selbst oder kollektiv durch erhöhte GKV-Beiträge, die von der Gesamtheit der Versicherten zu tragen wäre. Die Verwendung von zwei Preisattributen macht aus mindestens drei Gründen Sinn. Erstens führt das Referenzpreis-System in Deutschland zunehmend zu Zuzahlungen für Arzneimittel, die damit zu einer immer wichtigeren Finanzierungsquelle werden. Zweitens hat die Bevölkerung vermutlich auch Präferenzen bezüglich der Finanzierung von Gesundheitsleistungen, wie für den Fall von Dänemark nachgewiesen [66]. Und schließlich lassen ökonomische Überlegungen vermuten, dass die Patienten der Finanzierung durch erhöhte GKV-Beiträge (die von allen geleistet würde) den Vorzug geben vor der Finanzierung durch Zuzahlung (die nur die Betroffenen belasten würde). Diese Hypothese wird weiter unten geprüft (vgl. H4 in Abschn. 5).
Was das Attribut Zuzahlung betrifft, so gibt es für die Diabetespatienten keine Zuzahlung im Status quo (vgl. Tab. 1). In der Alternative kommen die Ausprägungen € 50, 150 und 300 jährlich vor, während die Kosten des Präparats € 226 betragen (vgl. Einleitung). Solche Vorgaben bergen stets die Gefahr eines Recoding; doch wenigstens ist hier seine Richtung nicht vorgegeben, da einige Teilnehmer € 50 als „unerwartet niedrig“, andere dagegen € 300 als „unerwartet hoch“ einschätzen dürften. Außerdem wird ja in einem DCE nie direkt nach der Zahlungsbereitschaft, sondern nur nach der Wahl zwischen dem Status quo und der Alternative gefragt, was den Einfluss eines Recoding von vornherein beschränkt. Im Zusammenhang mit dem Attribut GVK-Beitrag wurden die Teilnehmer am DCE gebeten, den von ihnen selbst bezahlten Anteil am GKV-Beitrag nachzuschlagen, um in diesem Punkt ihren individuellen Status quo zu fixieren. Die durch die Vergütung des Insulinanalogons verursachte Beitragserhöhung beläuft sich auf geschätzte € 8,54 je Jahr und GKV-Mitglied.Footnote 3 Dies entspricht im Mittel einer Beitragserhöhung um 0,5 % (also z. B. von 13,000 % auf 13,065 % im Beitragssatz). Im DCE werden die Erhöhungen auf 0,5, 1 und 2 % festgesetzt – im Interesse einer genügend großen Spanne zwischen den Ausprägungen (s. u.).
3.3 Design
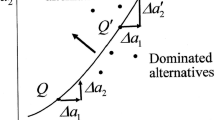
Für das Experiment wurde ein D-optimales Design mit Hilfe der Software GOSSET gewählt [69–73]. Die Zahl der 576 möglichen Kombinationen wurde so auf 30 reduziert und diese 30 zu Beginn zufällig in vier Kartensätze unterteilt, wobei die Wiederholung von Kombinationen vermieden wurde. Jeder Satz bestand aus acht bis zehn Entscheidungen zwischen dem herkömmlichen Insulin (Status quo) und dem neuartigen Insulin (Alternative). Ein Konsistenztest bestand darin, dass die Teilnehmer eine schwach dominierte Alternative vorgelegt erhielten, auf die jedoch nur sehr wenige „hereinfielen“. Da Entscheidungsfehler alltäglich sind, wurden diese Teilnehmer nicht ausgeschlossen, um eine falsche Genauigkeit der in Abschn. 7 präsentierten Schätzergebnisse zu vermeiden. Zudem wurden kostenträchtigere Alternativen signifikant weniger häufig gewählt als kostengünstigere. Insgesamt fiel die Wahl auf das Analoginsulin in 40 % der Fälle, auf das herkömmliche in 60 %. Nur gerade 27 Teilnehmer wechselten nie zwischen den beiden Insulinarten; da ihr Verhalten nicht auf Fehlentscheidungen hinweist, wurden sie in der Stichprobe behalten. Die Entscheidungsfindung wurde von der Hälfte der Teilnehmer als „leicht“, von 30 % als „schwierig“ und nur von 11 % als „sehr schwierig“ beurteilt.
3.4 Prätest
Die Verständlichkeit des Fragebogens (für die Befrager sowie für die Teilnehmer), die Wahrnehmung sowie die Relevanz und Vollständigkeit der Attribute wurden in einem Prätest geprüft. Der Prätest fand im Sommer 2007 statt und wurde durch ein auf das Gesundheitswesen spezialisiertes Marktforschungsinstitut durchgeführt. Es nahmen 30 Personen aus dem Großraum Leipzig teil, die Interviews wurden im Direktkontakt durchgeführt (17 Nicht-Diabetiker, vier Insulin-abhängige vom Typ 2, vier Insulin-naive vom Typ 2 und fünf Patienten vom Typ 1, 23 Frauen und sieben Männer, Durchschnittsalter 52 Jahre). Ein Drittel der Interviews konnten von den Autoren dieses Beitrags beobachtet werden. Die Teilnehmer verstanden die Fragen im Allgemeinen gut; 25 von ihnen stuften die DCE-Entscheidungen als „leicht“, fünf als „schwierig“ und überhaupt niemand als „sehr schwierig“ ein. Das Insulinanalogon wurde im Durchschnitt 3,8-mal aus einem Total von 10 Entscheidungen gewählt. Ökonometrische Schätzungen bestätigten die Relevanz der Attribute und der gewählten Ausprägungen, mit einer Ausnahme. Die Erhöhung der GKV-Beiträge um ursprünglich 0,25, 0,5 und 1 % genügte nicht, um die Entscheidungen zu beeinflussen; sie wurde deshalb auf 0,5, 1 und 2 % vergrößert. Auch wenn diese neuen Werte noch in einem „realistischen Bereich“ liegen mögen, beeinflussen sie potenziell die Präferenzäußerungen. Doch es geht gemäß Gleichung (5) darum, das Verhältnis der Grenznutzen und damit die Zahlungsbereitschaft für eine marginale Zunahme eines Attributs zu schätzen; dieser Parameter dürfte durch diese Verschiebung wenig berührt werden. Umgekehrt ist für die Schätzung der marginalen Zahlungsbereitschaft von entscheidender Bedeutung, dass der Koeffizient der Preisvariablen möglichst präzise geschätzt wird, was Wechsel zwischen Status quo und Alternative in genügender Anzahl verlangt. Eine ausgewählte Entscheidung wird in Abb. 1 illustriert.
3.5 Aufbau von Stichprobe und Hauptbefragung
Das DCE fand im Herbst 2007 in Deutschland statt. Da eine der Fragestellungen die Finanzierung eines Insulinanalogons durch einen erhöhten GKV-Beitrag im Vergleich zu einer Zuzahlung lautete, wurden nur erwachsene GKV-Versicherte (dies sind rd. 90 % der deutschen Bevölkerung) zur Teilnahme eingeladen. Dasselbe Marktforschungsinstitut wie beim Prätest übernahm die Rekrutierung sowie die Erhebung der Präferenzdaten. Die ausgebildeten Interviewer hatten meist bereits Erfahrungen mit gesundheitsbezogenen Befragungen. Die Interviews wurden im Direktkontakt durchgeführt. Von den insgesamt 1.110 Befragten leiden 602 nicht an Diabetes, 202 sind Diabetiker vom Typ 1 und 306 vom Typ 2. Die Gruppe vom Typ 2 umfasst 152 Insulin-naive und 154 mit Insulin behandelte Patienten. Weil auch die Heterogenität von Patientenpräferenzen erfasst werden soll, sind die Diabetiker überrepräsentiert, liegt doch die Diabetes-Prävalenz in Deutschland zwischen 6 und 10 % in der Altersgruppe 40–59 und 18 bis 28 % in der Altersgruppe der über 60-Jährigen [9].
Die Stichprobe der Nicht-Diabetiker ist repräsentativ bezüglich der 16 Bundesländer sowie Alter und Geschlecht. Dies war bei den Diabetikern vom Typ 2 nicht möglich. Da die Krankheit fast immer ab Alter 45 einsetzt, wurden drei gleich große Altersgruppen (46–55, 56–65, und über 65) gebildet. Die minimale Behandlungsdauer (Injektionen oder oral) für die Aufnahme in die Stichprobe beträgt sechs Monate. Weil sich schließlich die Rekrutierung von Diabetikern vom Typ 1 als sehr schwierig erwies, beschränkte sich bei ihnen die Repräsentativität auf die 16 Bundesländer.
4 Ex-ante vs. ex-post Zahlungsbereitschaft
Die DCE wenden die Zufallsnutzentheorie (sog. Random Utility Theory [74–78]) an, um die individuellen Präferenzen für Güter und Leistungen zu ermitteln, die (noch) nicht auf Märkten gehandelt werden. Die Teilnehmer werden gebeten, wiederholt zwischen einem (hier konstant gehaltenen) Status quo und einer Alternative mit immer wieder wechselnden Ausprägungen der Attribute zu wählen. Bei diesem Abwägen wird ein rationales Individuum stets jene Alternative bevorzugen, welchen den Erwartungswert des Nutzens maximiert. Zur Vereinfachung wird der Erwartungswert-Operator im Folgenden vernachlässigt, so dass die Entscheidungsfindung auf den Vergleich von Nutzenwerten hinausläuft, die gegeben sind durch
wobei U ij für den sog. indirekten, vom Individuum i erreichten Nutzen im Falle der Alternative j steht. Dieser Nutzen hängt ab vom Vektor der Attribute a j , dem zu bezahlenden Preis p j , dem Einkommen y i sowie den sozioökonomischen Eigenschaften s i des Individuums. Der Störterm ε ij variiert zwischen den Alternativen und Individuen; er rührt daher, dass die Experimentatoren nie alle Faktoren beobachten können, die in den subjektiven Nutzen eines Menschen eingehen. Unter der Annahme eines additiven Störterms zieht das Individuum die Alternative k der Alternative l vor, falls
wobei u( ⋅ ) die deterministische Komponente der Nutzenfunktion v( ⋅ ) bedeutet. Im Gegensatz zu ε ij kann von den beobachteten Wahlhandlungen auf diese Komponente und ihre Bestimmungsgründe zurückgeschlossen werden. Dazu geht man von der einleuchtenden Annahme aus, dass die Wahrscheinlichkeit P ik , mit welcher die Alternative k den Vorzug vor l erhält, der Wahrscheinlichkeit Prob entspricht, dass die Ungleichung (2) erfüllt ist. Die Auflösung nach der Differenz der Störterme ergibt dann
Damit eine statistische Inferenz bezüglich der rechten Seite von (3) möglich wird, muss ein Verteilungsgesetz für ω=(ε il −ε ik ) unterstellt werden. In Frage kommen die logistische und die Normalverteilung; die letztere kommt hier zur Anwendung. Das entsprechende Verfahren ist die Probit-Schätzung, wobei die Störterme als unkorreliert zwischen den Individuen, jedoch als korreliert (mit Autokorrelation erster Ordnung) über die bis zu 10 Entscheidungen angenommen werden (sog. Random-Effects-Spezifikation). Bei einer linearen Nutzenfunktion (begründet in [79]) erhält man für den Nutzenunterschied
mit ω ik =μ i +ν ik . Die βs sind die zu schätzenden Parameter, die zu den Attributen a 1k ,…,a Lk der betrachteten Alternative gehören, zu denen von jetzt an auch der zu bezahlende Preis gehört. Da nur die Nutzenunterschiede relevant sind [3], fallen die gleich bleibenden Eigenschaften der Teilnehmer weg.
Die marginale Rate der Substitution zwischen den Attributen m und n ergibt sich aus dem Verhältnis ihrer Grenz-nutzen und somit aus dem Verhältnis der partiellen Ableitungen der indirekten Nutzenfunktion in Bezug auf die beiden Attribute [80],
Definiert man n als Preisattribut, so wird dessen Grenznutzen zum (negativen) Grenznutzen des Einkommens, so dass sich die MRS im Absolutwert als marginale Zahlungsbereitschaft für das Attribut m interpretieren lässt.
Eine Besonderheit dieses Beitrags besteht darin, dass er einen Vergleich der Zahlungsbereitschaften ermöglicht von Individuen, die nicht an Diabetes leiden oder noch kein Insulin brauchen (ex-ante), und solchen, die Insulin-abhängig sind (ex-post). Während der Nutzengewinn (bzw. -verlust) für Insulin-behandelte Diabetiker unmittelbar anfällt, handelt es sich im Falle der Nicht-Diabetiker und Insulin-naiven Diabetiker um einen Erwartungsnutzen der Form
wobei π i die Individuum-spezifische (subjektive) Wahrscheinlichkeit darstellt, zum mit Insulin behandelten Diabetiker zu werden. Für Insulin-abhängige Patienten ist π i gleich 1, so dass der zweite Summand von (6) für sie Null beträgt. In diesem Fall wird (6) zum festen Wert U ij , dem vom Individuum erreichten Nutzen in Alternative j. Wenn man die oben beschriebenen Attribute in (1) einsetzt, erhält man für den Nutzen der Insulin-abhängigen DiabetikerFootnote 4:
Bei den Nicht-Diabetikern und Insulin-naiven Diabetikern liegt π i zwischen Null und Eins, so dass für sie die Differenz ihres Erwartungsnutzens gilt
Man beachte, dass die Variablen ab Gleichung (7) für Differenzen in den Ausprägungen des herkömmlichen und des neuartigen Insulins stehen. Beispielsweise bedeutet Zucker ij die Wahrscheinlichkeit einer Unterzuckerung bei Behandlung mit herkömmlichem (NPH) Insulin minus dieselbe Wahrscheinlichkeit bei Behandlung mit dem neuartigen Insulin. Entsprechend nehmen die Werte von Zucker, Gewicht, Schwenken, Flexibilität und Zuzahlung alle den Wert Null an, falls es sich um Nicht-Diabetiker und Insulin-naive Patienten handelt, bei denen es in Bezug auf diese Attribute von der Anlage des DCE her keinen Unterschied zwischen dem Status quo und den Alternativen gibt. Der GKV-Beitrag variiert hingegen, weil sich bei einer Aufnahme des Arzneimittels in den Leistungskatalog alle Mitglieder und nicht nur die Patienten an seiner Finanzierung beteiligen.
Es gibt zwei Gründe dafür, dass auch ein Nicht-Diabetiker einen Nutzen aus der Diabetesbehandlung hat und damit eine positive Zahlungsbereitschaft aufweist: Altruismus und/oder die Option einer verbesserten Behandlung für den Fall, dass die Krankheit in Zukunft eintritt. Im zweitgenannten Fall gibt der erste Summand in Gleichung (8) die Veränderung des Erwartungsnutzens ΔEU einer Person an, die sich die Möglichkeit vorstellt, in Zukunft Insulin-abhängig zu sein und deshalb eine positive Zahlungsbereitschaft für die verbesserte Behandlungsoption hat. Je höher ihre Wahrscheinlichkeit π i , desto höher ist die Wahrscheinlichkeit, diese Option auszuüben und desto höher ist die Zahlungsbereitschaft. Im Falle des Altruismus steht der zweite Summand von (8) für die Veränderung des Erwartungsnutzens einer Person, die damit rechnet, gesund zu bleiben. Dann ist β 0 als Zahlungsbereitschaft aus Altruismus zu interpretieren. Schließlich lässt sich (8) wie folgt umschreiben:
Diese Gleichung gilt sowohl für Nicht-Diabetiker als auch Diabetiker. Im Falle eines Patienten der zweiten Gruppe ist π i gleich 1, falls er oder sie mit Insulin behandelt wird, so dass (9) und (7) identisch sind. Die Berechnung der Zahlungsbereitschaft hängt ebenfalls von der Situation ab. Falls das Preisattribut (n) für die Zuzahlung steht, gilt (5). Falls es dagegen für den erhöhten GKV-Beitrag steht, ist die Zahlungsbereitschaft mit der Wahrscheinlichkeit zu gewichten, zum Diabetiker zu werden:
5 Zu prüfende Hypothesen
Dieser Abschnitt enthält die Hypothesen mit Bezug auf die Zahlungsbereitschafts-Werte, die im Zuge der ökonometrischen Auswertung des DCE geprüft werden sollen.
Hypothese H1
Aus der Sicht der GKV-Mitglieder hat das Insulinanalogon einen Zusatznutzen im Vergleich zum herkömmlichen Humaninsulin.
Ein erhöhter GKV-Beitrag bzw. eine Zuzahlung ist immer mit einem Nutzenverlust verbunden, der aber dieser Hypothese zufolge durch die Vorteile aus einer Behandlung mit dem Insulinanalogon statt mit Humaninsulin mehr als aufgewogen wird.
Hypothese H2
Die Zahlungsbereitschafts-Werte der Attribute weisen die folgende Rangordnung aufw.
-
H2.1:
Zucker > Gewicht.
-
H2.2:
Gewicht ≫ Flexibilität.
-
H2.3:
Schwenken = 0.
Diese Rangfolge lässt sich durch die Ausführungen im Abschn. 3.2 begründen.
Hypothese H3
Die Zahlungsbereitschaft der Diabetiker für Insulinanalogon unterscheidet sich von derjenigen der Nicht-Diabetiker; sie ist zudem innerhalb der Diabetiker-untergruppen unterschiedlich.
Unterschiedliche Erfahrungen in der Verwendung von Insulin führen vermutlich zu einer Heterogenität der Patientenpräferenzen (wie in [25] gefunden). Während Diabetiker vom Typ 1 und Insulin-behandelte Diabetiker vom Typ 2 das Insulin kennen, ist dies bei Nicht-Diabetikern und Insulin-naiven Diabetikern vom Typ 2 nicht der Fall. Insbesondere können sie nicht wissen, was eine Unterzuckerung für sie bedeutet und wie sie ihr begegnen können.
Hypothese H4
Nichtbetroffene Personen und Insulin-naive Diabetiker weisen eine höhere Zahlungsbereitschaft auf, falls die Finanzierung durch die Patienten selbst mittels Zuzahlung erfolgt, wogegen die Zahlungsbereitschaft von Insulin-behandelten Patienten höher ist, falls die Finanzierung durch einen erhöhten GKV-Beitrag erfolgt.
Sowohl für Diabetiker als auch Nicht-Diabetiker wird eine positive Zahlungsbereitschaft für Insulinanalogon vorausgesagt (H1). Allerdings ist bei Nicht-Diabetikern und Insulin-naiven Diabetikern eine höhere Zahlungsbereitschaft zu erwarten, falls das neue Präparat durch eine Zuzahlung der Patienten finanziert wird, als wenn sie sich an der Finanzierung über die GKV beteiligen müssen. Diese Voraussage ist jedoch nicht mit maximal ausgeprägtem Altruismus vereinbar, der unter den Nichtbetroffenen eine beträchtliche Zahlungsbereitschaft zur Folge hätte dafür, dass die Betroffenen finanziell nicht belastet werden. Umgekehrt müssten (bei wenig ausgeprägtem Altruismus diesmal der Betroffenen) die Zahlungsbereitschafts-Werte der Diabetiker vom Typ 1 sowie der Insulin-abhängigen Patienten vom Typ 2 dann besonders hoch sein, wenn alle GKV-Mitglieder über erhöhte Beiträge zur Finanzierung herangezogen würden.
6 Daten und deskriptive Statistik
Die Tab. 2 vermittelt einen Überblick über die Stichprobe. Ungefähr 50 % der Befragten sind Frauen. Das mittlere Alter der Diabetiker vom Typ 2 ist höher als dasjenige der übrigen Diabetiker in der Stichprobe, weil diese Krankheit vor allem in höherem Alter vorkommt (obschon die Zahl der Kinder mit Diabetes vom Typ 2 rasch zunimmt). Die Teilnehmer am DCE wurden gebeten, ihren subjektiven Gesundheitszustand auf einer visuellen Analogskala mit Werten von 0 (sehr schlechte Gesundheit) bis 100 (ausgezeichnete Gesundheit) zu markieren. Die Nicht-Diabetiker kommen auf den höchsten Durchschnittswert (73), Insulin-behandelte Patienten vom Typ 2 auf den niedrigsten (53). Im Durchschnitt haben die Diabetiker vom Typ 2 den höchsten BMI von 28 (falls Insulin-behandelt) und 27 (falls Insulin-naiv). Der Unterschied zu den Nicht-Diabetikern ist statistisch signifikant. Er stimmt mit den Ergebnissen von [52] überein, wonach Obesität unter Diabetikern vom Typ 2 weit verbreitet ist.
Das mittlere Haushaltseinkommen liegt bei € 1.900 monatlich. Insulin-naive Diabetiker vom Typ 2 liegen darunter (€ 1.783), Nicht-Diabetiker darüber (€ 1.975). Dieser Unterschied wird in [51] durch eine negative Korrelation zwischen Prävalenz des Diabetes vom Typ 2 und dem Einkommen bestätigt. Weil die GKV-Beiträge in Prozenten des Arbeitseinkommens erhoben werden, leisten die Bezieher höhere absolute Beiträge, wobei der Zusammenhang mit dem Einkommen wegen regional unterschiedlicher Beitragssätze nichtlinear ausfällt. Dennoch bezahlen die Nicht-Diabetiker der Stichprobe im Mittel einen höheren Beitrag als die anderen. Überdies haben 41 % von ihnen mindestens eine Zusatzversicherung, verglichen mit zu nur 30 % der Diabetiker vom Typ 1 und 31 % der Insulin-behandelten Diabetiker. Dies spiegelt die Tatsache wider, dass Insulin-abhängige Diabetiker für die privaten Anbieter von Zusatzversicherungen (PKV) ungünstige Risiken darstellen, von denen sie hohe Prämien verlangen oder die sie überhaupt ausschließen.
Der untere Teil der Tab. 2 enthält Angaben zur Dauer der Erkrankung und zur Inzidenz von Komplikationen im Zusammenhang mit Diabetes. Zur Zeit des Experiments leiden Diabetiker vom Typ 1 im Durchschnitt seit 17 Jahren an ihrer Krankheit; jene vom Typ 2 seit 8 bis 9 Jahren. Nur gerade 18 % der Insulin-abhängigen Diabetiker vom Typ 2 sind frei von Komplikationen; bei den Insulin-naiven Diabetikern sind es 23 %, und 27 % bei den Diabetikern vom Typ 1. Die häufigste Komplikation ist hoher Blutdruck, gefolgt von diabetischer Neuropathie, diabetischem Fuß und diabetischer Retinopathie (Augenleiden). Schlaganfälle und Herz-Kreislauf-Störungen sowie Amputationen kommen am häufigsten bei den Diabetikern mit Insulintherapie vor.
7 Ergebnisse der ökonometrischen Analyse
7.1 Zahlungsbereitschaft
Die Tab. 3 präsentiert die Schätzergebnisse zur Gleichung (9). Im Einklang mit der Erwartungsnutzentheorie entspricht der Beobachtung „Teilnehmer wählt die Alternative“, die mit „1“ codiert wird („0“ sonst). Da die zugrundeliegende Variable eine Wahlwahrscheinlichkeit ist, kommt das Probit-Verfahren für die statistische Inferenz zur Anwendung. Der Koeffizient des Attributs Zucker beispielsweise beträgt 0,0065, was darauf hinweist, dass eine Senkung des Unterzuckerungsrisikos (wie erwartet) positiv gewertet wird. Der z-Wert gibt an, dass dieser an sich kleine Koeffizient seinen Standardfehler um das 14,07-fache übertrifft; unter der Annahme der Normalverteilung für den Störterm ist es damit höchst unwahrscheinlich, dass er in Tat und Wahrheit Null beträgt. Die Nullhypothese „Eine Senkung des Unterzuckerungsrisikos hat keinen Einfluss auf den Nutzen der Teilnehmer am Experiment“ kann deshalb mit einer Irrtumswahrscheinlichkeit von weniger als 1 % verworfen werden. Auch die übrigen Koeffizienten sind hoch signifikant und weisen das erwartete Vorzeichen auf. Der positive Wert der Konstanten ist von besonderem Interesse und kann wie folgt interpretiert werden. Wenn die Spezifikation der Nutzenfunktion perfekt wäre, müsste eine Nutzendifferenz zwischen der Alternative und dem Status quo ausschließlich auf die Unterschiede in den Attributen zurückzuführen sein. Es gäbe keinen Grund, eine Konstante verschieden von Null zu erwarten. Es ist jedoch mit individuellen Eigenschaften der Befragten zu rechnen, die eine grundsätzliche Ablehnung (oder Befürwortung) des Status quo bewirken (status quo bias [81]). Im vorliegenden Fall lässt die positive Konstante auf eine Präferenz für die Alternative und damit eine Ablehnung des Status quo schließen.
Auf Grund von (5) und (10) kann man Werte der marginalen Zahlungsbereitschaft je nach Finanzierungsart (Zuzahlung bzw. erhöhter GKV-Beitrag) schätzen. Der obere Teil der Tab. 4 enthält die Ergebnisse für die Diabetiker im Falle der Zuzahlung, der untere Teil für die Diabetiker im Falle der Beitragserhöhung. Gemäß (10) müssen die Zahlungsbereitschafts-Werte für den Fall der Beitragserhöhung (die ja von allen geleistet werden müsste) gewichtet werden mit der Wahrscheinlichkeit zum Diabetiker zu werden, um die Zahlungsbereitschafts-Werte auch für die Nichtbetroffenen unter den GKV-Mitgliedern zu berechnen. In der letzten Spalte der Tab. 4 wird diese Gewichtung mit \(\bar{\pi}\), der durchschnittlichen subjektiven Wahrscheinlichkeit (π i ) der Befragten, Insulin-abhängig zu werden, vorgenommen. Sie wurde im Fragebogen mit einer visuellen Analogskala (mit Werten von 0 % „Ich werde nie zu einem Insulin-abhängigen Diabetiker“ bis 100 % „Ich werde dies mit Sicherheit“) erfasst. Für Diabetiker, die bereits mit Insulin behandelt werden, ist π i gleich Eins. Der geschätzte Durchschnittswert über alle Befragten beträgt \((\bar{\pi} =)\) 53 %.
Unabhängig von der Finanzierungsart weisen die Teilnehmer an diesem DCE eine ausgeprägte Präferenz für die Alternative auf, nämlich eine Zahlungsbereitschaft von € 262 bzw. € 162 pro Jahr. Demgegenüber findet man sonst meist einen Hang zum Status quo (negative Konstante [82, 83]). Im Falle der Diabetesbehandlung scheinen die Befragten jedoch eine positive Zahlungsbereitschaft für ein Abgehen vom Status quo aufzuweisen.
Was das Risiko einer Unterzuckerung betrifft, so sind die Befragten gemäß der Schätzung bereit, mittels Zuzahlung € 1,19 pro Jahr und Diabetiker für eine Senkung um 1 Prozentpunkt zu bezahlen; mittels einer Beitragserhöhung sogar € 1,39. Der letztgenannte Betrag ist allerdings noch mit der durchschnittlichen Wahrscheinlichkeit \(\bar{\pi}\) zu gewichten, so dass die marginale Zahlungsbereitschaft auf € 0,74 jährlich zurückgeht (vgl. den unteren Teil der Tab. 4). Zum Vergleich: Für die Vermeidung einer Gewichtszunahme um 1 kg sind die Befragten bereit, € 25 mittels Zuzahlung bzw. € 16 mittels erhöhter GKV-Beiträge zu bezahlen.
Dieser direkte Vergleich ist jedoch irreführend; die Veränderung muss standardisiert werden. Im Folgenden wird eine Veränderung des Attributs um jeweils 100 % vorgegeben. Dies ist im Falle des Unterzuckerungsrisikos zugegebenermaßen unrealistisch, doch lassen sich so die Zahlungsbereitschafts-Werte unmittelbar mit denjenigen von (0,1)-skalierten Attributen vergleichen. Die Zahlungsbereitschaft für eine 100 %ige Senkung des Unterzuckerungsrisikos beträgt ungefähr € 119 (Zuzahlung) bzw. € 139 (Beitragserhöhung). Die vollständige Vermeidung der Gewichtszunahme von maximal 2,5 kg (vgl. Abschn. 3) kommt ebenfalls einer Veränderung von 100 % gleich. Die Zahlungsbereitschaft dafür beträgt rd. € 63 (=2,5⋅25,15; Zuzahlung) bzw. € 39 (=2,5⋅15,55; Beitragserhöhung). Somit werten die Befragten unabhängig von der Finanzierungsart die Senkung des Unterzuckerungsrisikos zweimal höher als die Vermeidung der Gewichtszunahme, was die Hypothese H2.1 bestätigt. Die geschätzte Zahlungsbereitschaft für ein Mehr an Flexibilität bezüglich des Injektionszeitpunkts beläuft sich auf € 31 (Zuzahlung) bzw. € 19 (Beitragserhöhung). Dies sind deutlich niedrigere Werte als die € 63 bzw. € 39 für die Vermeidung der Gewichtszunahme, in Übereinstimmung mit H2.2.
Die Möglichkeit, Insulin ohne Schwenken zu injizieren, ist den Befragten jährlich € 54 wert (Zuzahlung) bzw. € 33 (erhöhter Beitrag). Da sich beide Schätzungen signifikant von Null unterscheiden, sprechen sie gegen H2.3. Offenbar findet eine scheinbar geringfügige Innovation (zumindest aus medizinischer Sicht) eine positive Zahlungsbereitschaft bei den GKV-Mitgliedern. Allerdings wird sie weniger hoch bewertet als die Vermeidung von Unterzuckerung oder Gewichtszunahme. So ist der Unterschied z. B. zwischen € 119 (Zahlungsbereitschaft für eine hundertprozentige Senkung des Unterzuckerungsrisikos im Falle der Zuzahlung) und € 54 (kein Schwenken, Zuzahlung) statistisch signifikant; dies geht aus den kleinen Standardfehlern in der Tab. 4 hervor.
Eine Prüfung von H1 (positive Zahlungsbereitschaft für das neuartige Arzneimittel) verlangt die Berechnung der Zahlungsbereitschaft für das Produkt insgesamt. Wie in Abschn. 3 dargelegt, senkt es das Unterzuckerungsrisiko um 30 % gegenüber der Behandlung mit NPH Humaninsulin. Während die Patienten bei dieser Behandlung im Durchschnitt 2,5 kg zunehmen, lässt sich eine Gewichtszunahme mit dem Insulinanalogon vermeiden. Der Injektionszeitpunkt ist flexibler, und das Präparat muss nicht geschwenkt werden. Die mit diesen nicht-marginalen Veränderungen verbundene Zahlungsbereitschaft lässt sich näherungsweise berechnen als die marginale Zahlungsbereitschaft multipliziert mit der Veränderung in der Ausprägung des Attributs [80]. Diese Teilwerte sind dann zu summieren, um die Zahlungsbereitschaft für das Produkt insgesamt zu erhalten [86]. Die Ergebnisse dieser Berechnung sind in der Tab. 5 aufgeführt. Die Zahlungsbereitschaft insgesamt beläuft sich auf geschätzte € 445 pro Jahr im Falle der Finanzierung mittels Zuzahlung und € 275 (nach Gewichtung mit der Wahrscheinlichkeit) im Falle eines erhöhten GKV-Beitrags. Ungefähr 60 % dieser Zahlungsbereitschaft stammt von der grundsätzlichen Präferenz für die Alternative. Doch sogar wenn diese Komponente vernachlässigt wird, sind die verbleibenden Zahlungsbereitschafts-Werte von € 183 bzw. € 114 immer noch signifikant von Null verschieden (vgl. die kleinen Standardfehler in der Tab. 5). Damit wird H1 bestätigt: Das Produkt stiftet den GKV-Mitgliedern einen Nutzen, der sich in einer positiven geschätzten Zahlungsbereitschaft niederschlägt.
7.2 Zahlungsbereitschaft nach Untergruppen
Um Gruppen-spezifische Zahlungsbereitschafts-Werte zu erhalten, wird (9) separat für Nicht-Diabetiker, Diabetiker vom Typ 1, Insulin-naive Diabetiker vom Typ 2 sowie Insulin-behandelte Diabetiker vom Typ 2 geschätzt. Die Gruppen-spezifischen marginalen Zahlungsbereitschafts-Werte (nicht ausgewiesen) werden wie im Abschn. 7.1 und in Analogie zur Tab. 5 mit den Veränderungen in den Ausprägungen der Attribute multipliziert und summiert. Die subjektive Wahrscheinlichkeit, zum Insulin-abhängigen Diabetiker zu werden, beträgt im Durchschnitt 26,2 % für Nicht-Diabetiker und 56,4 % für Insulin-naive Patienten. Die errechneten nicht-marginalen Zahlungsbereitschafts-Werte nach Untergruppen erscheinen in der Tab. 6. Die Summe I umfasst sämtliche Teilwerte der Zahlungsbereitschaft, Summe II dagegen nur die statistisch signifikanten. Die hohen z-Werte bedeuten kleine Standardfehler, so dass man auf eine Heterogenität der Präferenzen schließen kann, wie von H3 vorausgesagt.
Der Vergleich zwischen dem oberen und dem unteren Teil der Tab. 6 zeigt einmal mehr, dass die Finanzierungsart von Bedeutung ist, allerdings nicht ganz so, wie in H4 formuliert. Dieser Hypothese zufolge müssten die Zahlungsbereitschafts-Werte der Betroffenen höher ausfallen, wenn das neuartige Arzneimittel mittels erhöhter GKV-Beiträge statt mittels Zuzahlung finanziert wird, während es bei den Nichtbetroffenen genau umgekehrt sein sollte. Zwar weisen die Nicht-Diabetiker tatsächlich eine höhere Zahlungsbereitschaft für das Produkt insgesamt auf, wenn die Finanzierung durch Zuzahlung erfolgen würde. Dasselbe gilt für die Insulin-naiven Diabetiker, die sich offenbar als Nichtbetroffene fühlen. Aber die Diabetiker vom Typ 1 haben die höhere Zahlungsbereitschaft, wenn die Finanzierung durch eine Beitragserhöhung erfolgt (allerdings ist der Unterschied statistisch nicht signifikant). Bei den Insulin-behandelten Diabetikern vom Typ 2 scheint die Rangordnung wieder den Erwartungen zu entsprechen, indem ihre Zahlungsbereitschaft außerordentlich hoch ausfällt, wenn die Finanzierung mittels erhöhter GKV-Beiträge erfolgen würde (vgl. Summe I). Doch keiner der Zahlungsbereitschafts-Teilwerte erweist sich als statistisch signifikant von Null verschieden, so dass die Summe II ebenfalls Null wird. Offenbar sind die Einschätzungen bezüglich Insulinanalogon unter diesen Patienten sehr geteilt, sobald das Präparat durch eine Erhöhung des GKV-Beitrags zu finanzieren wäre. Möglicherweise ist Altruismus auf Seiten einiger Patienten am Werk, der sie zögern lässt, die Mehrkosten ihrer Behandlung auf die Allgemeinheit abzuwälzen.
Die hohen Zahlungsbereitschafts-Werte der Nicht-Diabetiker im Falle der Zuzahlung durch die Patienten stützen einmal mehr H4. Zur Hauptsache gehen sie auf eine grundsätzliche Präferenz für die Alternative zurück, wie durch die hohe positive Konstante angezeigt. Aber dies gilt eben nur so lange, als die Diabetiker für die Kosten selbst aufkommen. Im Falle einer Finanzierung durch erhöhte GKV-Beiträge sind die (mit der Wahrscheinlichkeit gewichteten) Zahlungsbereitschafts-Werte sehr viel geringer, so wie von H4 vorausgesagt. Immerhin bleiben sie signifikant positiv, was auf ein gewisses Maß von Altruismus schließen lässt.
Zusammenfassend können die Eintragungen der Tab. 6 wie folgt interpretiert werden. Die hohen Zahlungsbereitschafts-Werte nicht betroffener Diabetiker und Insulin-naiven Diabetiker bei Finanzierung durch Zuzahlung weisen darauf hin, dass sie einer Finanzierung durch die Patienten selbst den Vorzug geben. Umgekehrt lassen die hohen Zahlungsbereitschafts-Werte bei Finanzierung durch erhöhte GKV-Beiträge darauf schließen, dass mit Insulin behandelte Patienten lieber die gemeinsame Finanzierung über die Krankenversicherung hätten. Doch unabhängig von der betrachteten Untergruppe und unabhängig von der Finanzierungsart ergibt sich, dass die mit der Summe I gemessene Zahlungsbereitschaft für das neuartige Insulinanalogon seine Kosten von jährlich € 226 übersteigt. Diese Aussage gilt auch, falls die Summe II als Maß (unter Ausschluss der nichtsignifikanten Teilwerte) verwendet wird, mit der einzigen Ausnahme der Insulin-abhängigen Patienten vom Typ 2, deren Präferenzen offenbar zu heterogen sind, um die übliche Signifikanzschwelle für ihre Zahlungsbereitschaft für das Produkt insgesamt zu erreichen. Nach dem Nutzen-Kosten-Kriterium spricht demnach nichts dagegen, das neuartige Arzneimittel in den Leistungskatalog der deutschen GKV aufzunehmen.
8 Schlussfolgerungen
Dieser Beitrag hat die Frage zum Thema, ob ein neues Arzneimittel für die Diabetesbehandlung in den Leistungskatalog der deutschen Gesetzlichen Krankenversicherung (GKV) aufgenommen werden soll oder nicht. Vom Standpunkt der Kosten-Nutzen-Analyse und unter Vernachlässigung von Verteilungs-Gesichtspunkten ist eine Aufnahme dann gerechtfertigt, wenn die GKV-Mitglieder eine mittlere Zahlungsbereitschaft aufweisen, welche die Kosten der Behandlung mit dem neuen Präparat übersteigt. Im konkreten Fall handelt es sich um das Präparat „Insulin Detemir“, ein langwirksames Insulinanalogon für die Behandlung von Diabetes. Die Präferenzen der GKV-Mitglieder für dieses Arzneimittel im Vergleich zur konventionellen Therapie (mit NPH Humaninsulin) werden mit Hilfe eines sog. Discrete-Choice-Experiments im Jahre 2007 ermittelt. Am Experiment nahmen 1.110 Versicherte teil, von denen 202 Diabetes vom Typ 1 haben, 154 sind vom Typ 2 mit Insulinbehandlung, 152 Insulin-naive Diabetiker vom Typ 2 und 602 Nicht-Diabetiker.
Das Besondere an diesem Experiment liegt in zwei Aspekten. Zum einen erlaubt die Unterscheidung von Untergruppen die Schätzung sowohl der ex-ante Zahlungsbereitschaft von Nicht-Diabetikern wie auch der ex-post Zahlungsbereitschaft von Diabetespatienten. Zum anderen kann man dank der Vorgabe von zwei Finanzierungsarten (Zuzahlung bzw. Erhöhung der GKV-Beiträge) prüfen, ob das neuartige Arzneimittel ein günstiges Nutzen-Kosten-Verhältnis aufweist, unabhängig davon, wie es finanziert wird. Auf Grund der Ergebnisse lassen sich die vier in der Einleitung genannten Fragestellungen wie folgt beantworten.
-
(1)
Weisen die Mitglieder der deutschen GKV eine positive Zahlungsbereitschaft für das Insulinanalogon auf?
Die ökonometrische Evidenz lässt vermuten, dass eine positive Zahlungsbereitschaft im Vergleich zur herkömmlichen Therapie mit langwirksamem Humaninsulin NPH besteht (Tab. 5). Sie setzt sich zusammen aus einer Zahlungsbereitschaft für die Reduktion des Unterzuckerungsrisikos um 30 %, der Vermeidung einer Gewichtszunahme von 2,5 kg während der ersten sechs Monate der Behandlung, der Entbindung von der Notwendigkeit, das Präparat vor jeder Injektion zu schwenken sowie einem Mehr an Flexibilität bezüglich des Zeitpunkts der Injektion.
-
(2)
Welche Attribute des Produkts tragen zur Zahlungsbereitschaft bei?
Den Schätzungen zufolge weisen alle Attribute eine signifikant positive Zahlungsbereitschaft auf. Um die Vergleichbarkeit mit den (0,1)-skalierten Attributen zu gewährleisten, wird eine hypothetische Senkung des Unterzuckerungsrisikos um 100 % und eine vollständige Vermeidung der Gewichtszunahme unterstellt. Erwartungsgemäß stammt die größte Zahlungsbereitschaft von der Senkung des Unterzuckerungsrisikos, gefolgt von der Vermeidung der Gewichtszunahme. Die übrigen Attribute werden durch die Teilnehmer am Experiment weniger hoch bewertet, wie vorausgesagt.
-
(3)
Besteht Heterogenität der Präferenzen zwischen den verschiedenen Untergruppen, nämlich den Nicht-Diabetikern, Diabetikern vom Typ 1, Insulin-abhängigen Diabetikern vom Typ 2 sowie Insulin-naiven Diabetikern vom Typ 2?
Tatsächlich weisen die ökonometrischen Schätzungen auf Präferenzheterogenität hin, indem sich die Werte der Zahlungsbereitschaft für das Präparat als Ganzes statistisch signifikant zwischen den Untergruppen unterscheiden. Die Nichtbetroffenen, d. h. Nicht-Diabetiker sowie Insulin-naive Diabetiker vom Typ 2, haben ähnliche Präferenzen, die von denjenigen der Betroffenen, nämlich den Diabetikern vom Typ 1 und den Insulin-abhängigen (die unter sich ähnlich sind) systematisch abweichen.
-
(4)
Ist das Nutzen-Kosten-Verhältnis des neuartigen Arzneimittels günstig, unabhängig davon, ob es individuell durch Zuzahlung der Patienten selbst oder kollektiv durch eine Erhöhung der GKV-Beiträge finanziert wird?
Diese Frage kann im Lichte der Ergebnisse bejaht werden, mit der einen Ausnahme der Insulin-behandelten Diabetiker vom Typ 2 im Falle der Beitragserhöhung. Die geschätzten Zahlungsbereitschaft-Werte sind zwar außerordentlich hoch, doch wegen der großen Streuung statistisch nicht signifikant. Zudem weisen Nicht-Diabetiker und Insulin-naive Diabetiker eine höhere Zahlungsbereitschaft auf, falls die Finanzierung durch Zuzahlung erfolgen würde, Insulin-behandelte Diabetiker dagegen haben höhere Zahlungsbereitschafts-Werte, wenn erhöhte GKV-Beiträge zur Finanzierung herangezogen würden. Dies lässt sich als eine Präferenz der Nichtbetroffenen für die Finanzierung mittels Zuzahlung und der Betroffenen für eine Finanzierung mittels erhöhter GKV-Beiträge interpretieren. Da jedoch die Zahlungsbereitschaft sogar der Nicht-Diabetiker die zusätzlichen Behandlungskosten bei Verwendung des Insulinanalogons übertrifft, und zwar unabhängig von der Finanzierungsart, steht aus Sicht der ökonomischen Nutzen-Kosten-Analyse der Aufnahme dieses Arzneimittels in den Leistungskatalog der GKV nichts entgegen.
Diese Schlussfolgerungen unterliegen einer Reihe von Einschränkungen. Vorab könnten die geschätzten Zahlungsbereitschafts-Werte nach oben verzerrt sein, weil die Teilnehmer am Experiment möglicherweise nicht repräsentativ für die Gesamtheit der GKV-Mitglieder sind. Tatsächlich liegt das durchschnittliche Einkommen in der Stichprobe unter dem Mittelwert Deutschlands, was mit einer allgemeinen Unzufriedenheit einhergehen mag, die zu einer grundsätzlichen Ablehnung des Status quo führen könnte. Die mögliche Folge wäre eine grundsätzliche Ablehnung auch der herkömmlichen Diabetestherapie bzw. eine grundsätzliche Zahlungsbereitschaft für eine alternative Therapie. Zweitens könnte es trotz der Unterscheidung von Untergruppen immer noch eine versteckte Heterogenität geben, die mit dem Störterm korreliert ist und die Schätzwerte verzerrt. Hingegen dürfte Skalenheterogenität kaum ein Problem darstellen, denn die unterschiedenen Untergruppen haben mindestens vom Szenario her den gleichen (stets konstant gehaltenen) Status-quo-Punkt. Im Gegensatz etwa zum Best-Worst-Scaling kann es deshalb nicht dazu kommen, dass sich die erhobenen Präferenzen der Untergruppen nur deshalb unterscheiden, weil der Nutzen der einen anders skaliert ist als der anderen. Zudem wird ja die marginale Grenzrate der Substitution geschätzt [vgl. (5)], die bekannterweise gegenüber einer ordnungserhaltenden Skalierung des Nutzens (bzw. der Ausprägungen der Attribute) invariant ist. Drittens wurden für das Attribut des Unterzuckerungsrisikos Reduktionen auf 75 % und 50 % gewählt, aufgrund der statistischen Inferenz. Die Werte könnten von einzelnen Teilnehmern als nicht realistisch beurteilt worden sein. Es sei darauf hingewiesen, dass die Gruppe der Diabetiker bei der Schätzung, welche Tab. 4 zu Grunde liegt, überrepräsentiert sind. Dies könnte einen Einfluss auf die Resultate haben. Es bleibt offen, ob die Zahlungsbereitschaft für die sofortige Anwendbarkeit des Präparates auf der einfacheren Anwendung selbst oder dem verminderten Risiko, nicht die optimale Menge an Insulin zu injizieren, beruht. Schließlich steht die Verwendung einer linearisierten Nutzenfunktion im Widerspruch zur mikroökonomischen Theorie (die Indifferenzkurven sind keine Geraden) und hat zur Folge, dass die geschätzten Zahlungsbereitschaften nur in der Umgebung des Status quo Gültigkeit haben [87]. Schließlich mag man die Verwendung des Nutzen-Kosten-Kriteriums als unzulässig kritisieren. Manche Autoren argumentieren, es seien die Quality-adjusted Life Years (QALYs) und nicht Geldeinheiten als Nutzenmaß zu verwenden [69, 88–90]. Andere weisen darauf hin, dass durchschnittliche Zahlungsbereitschafts-Werte die Verteilung der Nutzen über die Mitglieder der Gesellschaft vernachlässigt.
Diese Einwände haben ihre Berechtigung. Sie werden jedoch die zentralen Ergebnisse der vorliegenden Untersuchung kaum über den Haufen werfen. Erstens besteht eindeutige Evidenz dahingehend, dass nicht nur die Senkung des Unterzuckerungsrisikos und die Vermeidung der Gewichtszunahme Nutzen stiften, sondern auch Attribute, die üblicherweise als medizinisch irrelevant eingestuft werden, so die Entbindung von der Notwendigkeit, das Präparat vor der Injektion zu schwenken und die erhöhte Flexibilität bezüglich des Injektionszeitpunkts. Diese „irrelevanten“ Attribute werden zudem nicht nur von den aktuellen Diabetespatienten, sondern auch von den potenziellen Patienten und damit der Gesamtheit der erfassten GKV-Versicherten mit einer positiven Zahlungsbereitschaft belegt. Zweitens summieren sich diese Bewertungen zu Beträgen, die durchwegs die zusätzlichen Behandlungskosten bei Verwendung des neuen Arzneimittels übersteigen, mit der einzigen Ausnahme der Insulin-abhängigen Diabetiker vom Typ 2 und für den Fall der Finanzierung durch erhöhte GKV-Beiträge. Hier fallen die geschätzten Zahlungsbereitschafts-Werte zwar sehr hoch aus, doch sie streuen so stark, dass sich ihr Mittelwert statistisch nicht von Null unterscheiden lässt. Offenbar gehen die Meinungen in dieser Untergruppe weit auseinander, insbesondere darüber, ob den übrigen GKV-Mitgliedern die höheren Beiträge zugemutet werden können. Schließlich kann man sich nur schwer allgemein akzeptierte Gewichtungen bei der Verteilung der Nutzen vorstellen, die so einseitig Arme oder Reiche begünstigen würden, dass die entscheidende Schlussfolgerung umgestoßen wird: Nach Maßgabe des Nutzen-Kosten-Kriteriums und beim jetzigen Stand der Erkenntnis lässt sich ein Ausschluss dieses neuartigen Arzneimittels aus dem Leistungskatalog der deutschen Gesetzlichen Krankenversicherung kaum rechtfertigen.
9 Hinweis
Diese Studie wurde von Novo Nordisk Pharma GmbH finanziert. Doch die Autoren bedingten sich für die Planung, Durchführung und ökonometrische Analyse des Experiments vollumfängliche Unabhängigkeit aus. Insbesondere wählten sie das Marktforschungsinstitut nach eigenem Gutdünken und ließen sich die Daten direkt, ohne Dazwischenschalten des Sponsors, übermitteln.
Notes
Diabetiker vom Typ 1 produzieren kein Insulin; dieser Typ wird in der Regel bei Kindern und jungen Erwachsenen diagnostiziert und verlangt von Anfang an eine Insulinbehandlung. Im Falle von Diabetes vom Typ 2 stellt der Körper nicht genügend Insulin her, oder die Zellen nehmen es nicht auf; er kommt überwiegend bei älteren Menschen vor. Diabetiker vom Typ 2 heißen „Insulin-naiv“, falls sie (noch) nicht mit Insulin, sondern mit einem oralen Diabetespräparat behandelt werden. Im Verlaufe der Zeit brauchen sie jedoch ebenfalls Insulin für ihre Behandlung [5].
Siehe Fachinformation zu Insulin Detemir bzw. zum Präparat „Levemir“.
Die Attribute wurden für die ökonometrischen Schätzungen wie folgt codiert. Für das Attribut Zucker wurden die drei Ausprägungen 100, 75 und 50 verwendet, für Gewicht die Ausprägungen +2,5, 0 und −1. Für die Attribute Schwenken und Flexibilität wurde ein Dummy-Coding verwendet. Für Zuzahlung gingen die Ausprägungen 0, 50, 150 und 300 in die Schätzung ein, für GKV-Beitrag jeweils die effektiven Beträge, je nach Einkommen der befragten Person. Die drei Attribute mit drei Ausprägungen wurden zuerst als Satz von Dummyvariablen dargestellt, z. B. Zucker50=1, = 0 sonst; Zucker25=1, = 0 sonst, mit Zucker100 als Basiskategorie. Die Abstufung der Probit-Koeffizienten war mit der Proportionalitätsannahme der Variablen Zucker vereinbar; dies gilt auch für die beiden anderen Attribute.
Literatur
GKV Spitzenverband. Website. 2013.
Statistical Offices of the Länder. Volkswirtschaftliche Gesamtrechnung der Länder VGRdL (National Accounts at the level of the Länder). Website. 2011.
Caermon CG, Bennett HA. Cost-effectiveness of insulin analogues for diabetes mellitus. CMAJ, Can Med Assoc J. 2009;180(4):400–7.
Valentine WJ, Erny-Albrecht K, Ray J, Roze S, Cobden D, Palmer A. Therapy conversion to insulin detemir among patients with type 2 diabetes treated with oral agents: a modeling study of cost-effectiveness in the United States. Curr Med Res Opin. 2007;23(4):895–901.
American Diabetes Association. Diabetes basics. Website. 2011.
World Health Organization. Diabetes facts. Website. 2007.
Wild S, Roglic G, Green A, Sicref R, King H. Global prevalence of diabetes: estimates for the year 2000 and projections for 2030. Diabetes Care. 2004;27:1047–53.
Huang ES, Basu A, O’Grady M, Capretta JC. Projecting the future diabetes population size and related costs for the U.S. Diabetes Care. 2009;32(12):2225–9.
Hauner H. Diabetesepidemiologie und Dunkelziffer (Epidemiology and iceberg phenomenon in diabetes). In Nuder, G. Hrsg. Deutscher Gesundheitsbericht Diabetes. Deutsche Diabetes Union DDU; 2008. S. 7–11.
IQWIG. Kurzwirksame Insulinanaloga zur Behandlung des Diabetes mellitus Typ 1 – Abschlussbericht. Version 1.1 A05-02. Institute for Quality and Efficiency in Health Care. 2009.
IQWIG. Langwirksame Insulinanaloga zur Behandlung des Diabetes mellitus Typ 1 – Vorbericht (vorläufige Nutzenbewertung). Version 1.0 A05-01. Institute for Quality and Efficiency in Health Care. 2009.
Palmer AJ, Roze S, Valentine WJ, Smith I, Wittrup-Jensen KU. Cost-effectiveness of detemir-based basal/bolus therapy versus NPH-based basal/bolus therapy for type 1 diabetes in a UK setting: an economic analysis based on metaanalysis results of four clinical trials. Curr Med Res Opin. 2004;20(11):1729–46.
Palmer AJ, Valentine WJ, Ray JA, Foos V, Lurati F, Smith I, Lammert M, Roze S. An economic assessment of analogue basal bolus insulin versus human basal-bolus insulin in subjects with type 1 diabetes in the UK. Curr Med Res Opin. 2007;23(4):895–901.
Palmer AJ, Lammert M, Hermansen K. Health economic consequences of insulin analogues in the treatment of type 1 diabetes in Denmark. Ugeskr Læger. 2008;170(15):1250–4.
Gschwend MH, Aagren M, Valentine WJ. Cost-effectiveness of insulin detemir compared with neutral protamine hagedorn insulin in patients with type 1 diabetes using a basal-bolus regimen in five European countries. J Med Econ. 2009;12(2):114–23.
Leichter S. Is the use of insulin analogue cost-effective? Adv Ther. 2008;25(4):285–99.
Valentine WJ, Palmer AJ, Erny-Albrecht KM, Ray JA, Cobden D, Foos V, Lurati FM, Roze S. Cost-effectiveness of basal insulin from a US health system perspective: comparative analyses of detemir, glargine, and NPH. Adv Ther. 2006;23(2):191–207.
Tunis SL, Minshall ME, Conner C, McCormick JI, Kapor J, Yale J-F, Groleau D. Cost-effectiveness of insulin detemir compared to NPH insulin for type 1 and type 2 diabetes mellitus in the Canadian payer setting: modeling analysis. Curr Med Res Opin. 2009;25(5):1273–84.
Davey P, Grainger D, MacMillan J, Rajan N, Aristides M, Dobson M. Economic evaluation of insulin lispro versus neutral (regular) insulin therapy using a willingness-to-pay approach. Pharmacoeconomics. 1998;13(3):347–58.
Dranitsaris G, Longo CJ, Grossman LD. The economic value of a new insulin preparation, humalog mix 25: measured by a willingness-to-pay approach. Pharmacoeconomics. 2000;18(3): 275–87.
Sadri H, MacKeigan LD, Leiter LA, Einarson TR. Willingness to pay for inhaled insulin: a contingent valuation approach. Pharmacoeconomics. 2005;23(12):1215–27.
Aristides M, Weston AR, FitzGerald P, Le Reun C, Maniadakis N. Patient preference and willingness-to-pay for humalog mix25 relative to humulin 30/70: a multicountry application of a discrete choice experiment. Value Health. 2004;7(4):442–54.
Hauber AB, Mohamed AF, Johnson FR, Falvey H. Treatment preferences and medication adherence of people with type 2 diabetes using oral glucose-lowering agents. Diabet Med. 2009;26(4):416–24.
Guimaraes C, Marra CA, Colley L, Gill S, Simpson S, Meneilly G, Queiroz RHC, Lynd LD. Socioeconomic differences in preferences and willingness-to-pay for insulin delivery systems in type 1 and type 2 diabetes. Diabetes Technol Ther. 2009;11(9):567–73.
Guimaraes C, Marra CA, Colley L, Gill S, Simpson SH, Meneilly GS, Queiroz RHC, Lynd LD. A valuation of patients’ willingness-to-pay for insulin delivery in diabetes. Int. J Technol Assess Health Care. 2009;25(3):359–66.
Jendle J, Torffvit O, Ridderstrale M, Lammert M, Ericsson A, Bogelund M. Willingness to pay for health improvements associated with anti-diabetes treatments for people with type 2 diabetes. Curr Med Res Opin. 2010;26(4):917–23.
Sreenan S, Virkamaki A, Zhang K, Hansen JB. Switching from NPH insulin to once-daily insulin detemir in basal-bolus-treated patients with diabetes mellitus: data from the European cohort of the predictive study. Int J Clin Pract. 2008;62(12):1971–80.
Russell-Jones D, Boliner J, Simpson R. Lower and more predictable fasting glucose and reduced risk of nocturnal hypoglycaemia with once daily insulin detemir versus NPH in subjects with type 1 diabetes. Diabetologia. 2004;45(Suppl. 2): A51.
Vague P, Selam JL, Skeie S. Insulin detemir is associated with more predictable glycemic control and lower risk of hypoglycemia compared to NPH insulin in subjects with type 1 diabetes on a basal-bolus regimen with premeal insulin aspart. Diabetes Care. 2002;26:590–6.
Hermansen K, Fontaine P, Kukolja KK. Insulin analogues (insulin detemir and insulin aspart) versus traditional human insulins (NPH insulin and regular human insulin) in basal-bolus therapy for patients with type 1 diabetes. Diabetologia. 2004;47:622–9.
Home P, Bartley P, Russell-Jones D. Insulin detemir offers improved glycemic control compared to NPH insulin in people with type 1 diabetes: a randomized clinical trial. Diabetes Care. 2004;27:1081–7.
Kolendorf K, Pavlic-Renar I, Santeusanio F, Philotheou A, Gall M, Heller S. Insulin detemir is associated with lower risk of hypoglycemia compared to NPH insulin in people with type 1 diabetes. In: Program of the American Diabetes Association’s 64th annual scientific sessions. 2004. S. A551-P.
Robertson K, Schonle E, Gucev Z. Benefits of insulin detemir over NPH insulin in children and adolescents with type 1 diabetes: lower and more predictable fasting plasma glucose and lower risk of nocturnal hypoglycemia. In: Program of the American Diabetes Association’s 64th annual scientific sessions. 2004. S. A606-P.
Russell-Jones D. Insulin detemir and basal insulin therapy. Endocrinol Metab Clin N Am. 2007;36(Suppl.):6–52.
Bartley PC, Bogoev M, Larsen J, Philotheou A. Long-term efficacy and safety of insulin detemir compared to neutral protamine hagedorn insulin in patients with type 1 diabetes using a treat-to-target basal-bolus regimen with insulin aspart at meals: a 2-year, randomized, controlled trial. Diabet Med. 2008;25(4):442–9.
Dornhorst A, Lüddeke H-J, Honka M, Ackermann RW, Merilainen M, Gallwitz B, Sreenan S. Safety and efficacy of insulin detemir basal-bolus therapy in type 1 diabetes patients: 14-week data from the European cohort of the predictive study. Curr Med Res Opin. 2008;24(2):369–76.
Marre M, Pinget M, Gin H, Thivolet C, Hanaire H, Robert J, Fontaine P. Insulin detemir improves glycaemic control with less hypoglycaemia and no weight gain: 52-week data from the predictive study in a cohort of French patients with type 1 or type 2 diabetes. Diabetes Metab. 2009;35(6):469–75.
Raskin P. Efficacy and safety of insulin detemir. Endocrinol Metab Clin N Am. 2007;36(Suppl. 1):21–32.
Satish KG, Ramachandra GN. Long-acting insulin analogs versus human insulins. Diabetes Technol Ther. 2008;10(5):331–2.
Demssie YN, Younis N, Soran H. The role of insulin detemir in overweight type 2 diabetes management. Vasc Health Risk Manag. 2009;5:553–60.
Dundar BN, Dundar N, Eren E. Comparison of the efficacy and safety of insulin glargine and insulin detemir with NPH insulin in children and adolescents with type 1 diabetes mellitus receiving intensive insulin therapy. J Clin Res Pediatr Endocrinol. 2009;1(4):181–7.
Freeman JS. Insulin analog therapy: improving the match with physiologic insulin secretion. J Am Osteopath Assoc. 2009;109(1):26–36.
Hermansen K, Dornhorst A, Sreenan S. Observational, open-label study of type 1 and type 2 diabetes patients switching from human insulin to insulin analogue basal bolus regimens: insights from the predictive study. Curr Med Res Opin. 2009;25(11):2601–8.
Monami M, Marchionni N, Mannucci E. Long-acting insulin analogues vs. NPH human insulin in type 1 diabetics. A meta-analysis. Diabetes Obes Metab. 2009;11(4):372–8.
Waugh N, Cummins E, Royle P, Clar C, Marien M, Richter B, Philip S. Newer agents for blood glucose control in type 2 diabetes: systematic review and economic evaluation. Health Technol Assess. 2010;14(36):1–248.
Umpierrez GE, Hor T, Smiley D, Temponi A, Umpierrez D, Ceron M, Munoz C, Peng L, Baldwin D. Comparison of inpatient insulin regimes with detemir plus aspart versus neutral protamine hagedorn plus regular in medical patients with type 2 diabetes. J Clin Endocrinol Metab. 2009;94(2):564–9.
Singh SR, Ahmad F, Lal A, Yu C, Bai Z, Bennett H. Efficacy and safety of insulin analogues for the management of diabetes mellitus: a meta-analysis. CMAJ, Can Med Assoc J. 2009;180(4):385–97.
Horvath K, Jeitler K, Berghold A, Ebrahim SH, Gratzer TW, Plank J, Kaiser T, Pieber TR, Siebenhofer A. Long-acting insulin analogues versus NPH insulin (human isophane insulin) for type 2 diabetes mellitus. Cochrane Database Syst Rev.. 2007;2:CD005613.
IQWIG. Langwirksame Insulinanaloga zur Behandlung des Diabetes mellitus Typ 2 – Vorbericht (vorläufige Nutzenbewertung). Version 1.0 A05-03. Institute for Quality and Efficiency in Health Care. 2009.
Russell-Jones D, Khan R. Insulin-associated weight gain in diabetes—causes effects and coping strategies. Diabetes Obes Metab. 2007;9:799–812.
Häussler B, Berger U, Mast O, Thefeld W. Risk and potential risk reduction in diabetes type 2 patients in Germany. Eur J Health Econ. 2005;6(2):152–8.
UK Prospective Diabetes Study (UKPDS) Group. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). Lancet. 1998;352:837–53.
Haak T, Tiengo A, Waldhäusl W, Draeger E. Treatment with insulin detemir is associated with predictable fasting blood glucose levels and favourable weight development in subjects with type 2 diabetes. Diabetes. 2003;52(Suppl. 1): A120.
Haak T, Tiengo A, Draeger E, Suntum M, Waldhäusl W. Lower within-subject variability of fasting blood glucose and reduced weight gain with insulin detemir compared to NPH insulin in patients with type 2 diabetes. Diabetes Obes Metab. 2005;7:56–64.
Hermansen K, Davies M. Does insulin detemir have a role in reducing risk of insulin associated weight gain? Diabetes Obes Metab. 2007;9:209–17.
Raslova K, Tamer SC, Clauson P, Karl D. Insulin detemir results in less weight gain than NPH insulin when used in basal-bolus therapy for type 2 diabetes mellitus, and this advantage increases with baseline body mass index. Clin Drug Investig. 2007;27(4):279–85.
Mandosi E, Fallarino M, Rossetti M, Gatti A, Morano S. Waist circumference reduction after insulin detemir therapy in type 2 diabetes patients previously treated with NPH. Diabetes Res Clin Pract. 2009;84(2). e18–e20.
Hallschmid M, Jauch-Chara K, Korn O, Molle M, Rasch B, Born J, Schultes B, Kern W. Euglycemic infusion of insulin detemir compared with human insulin appears to increase direct current brain potential response and reduces food intake while inducing similar systemic effects. Diabetes. 2010;59(4):1101–7.
Raslova K. An update on the treatment of type 1 and type 2 diabetes mellitus: focus on insulin detemir, a long-acting human insulin analog. Vasc Health Risk Manag. 2010;6:399–410.
Zachariah S, Sheldon B, Shojaee-Moradie F, Jackson NC, Backhouse K, Johnsen S, Jones RH, Umpley AM, Russell-Jones DL. Insulin detemir reduces weight gain as a result of reduced food intake in patients with type 1 diabetes. Diabetes Care. 2011;34(7): 1487–91.
Bush MA. Intensive diabetes therapy and body weight: focus on insulin detemir. Endocrinol Metab Clin N Am. 2007;36(Suppl. 1):33–44.
Schleser-Mohr S. Einfach gut leben – mit Insulin! (Simply have a good life—using insulin). Website. 2007.
Schmeisl G-W. Schulungsbuch für Diabetiker (Book of instructions for diabetics). 6. Aufl. Munich: Urban & Fischer; 2009.
Soran H, Younis N. Insulin detemir: a new insulin analogue. Diabetes Obes Metab. 2006;8:26–30.
Kurtzhals P. Pharmacology of insulin detemir. Endocrinol Metab Clin N Am. 2007;36(Suppl.):6–52.
Slothuus Skjoldborg U, Gyrd-Hansen D. Conjoint analysis. The cost variable: an Achilles’ heel? Health Econ. 2003;12:479–91.
Giani G, Janka HU, Hauner H, Standl E, Schiel R, Neu A, Rathmann W, Rosenbauer J. Epidemiologie und Verlauf des Diabetes mellitus in Deutschland (Epidemiology and development of diabetes in Germany). 2004.
BMG. Institut für Qualitätssicherung und Wirtschaftlichkeit im Gesundheitswesen. 2007.
Street D, Bunch DS, Moore B. Optimal designs for 2k paired comparison experiments. Commun Stat, Theory Methods. 2001;30:2149–71.
Burgess L, Street D. Optimal designs for 2k choice experiments. Commun Stat, Theory Methods. 2003;32:2185–206.
Carlsson F, Martinsson P. Design techniques for stated preference methods in health economics. Health Econ. 2003;12:281–94.
Kuhfeld WF, Tobias RD, Garratt M. Efficient experimental design with marketing research applications. J Mark Res. 1994;XXXI:545–57.
Sloane N, Hardin R. Gosset: A general-purpose program for designing experiments. Website, 2007.
Luce DR. Individual choice behavior. New York: Wiley; 1959.
Manski C, Lerman SR. The estimation of choice probabilities from choice based samples. Econometrica. 1977;45(8):1977–88.
McFadden D. Conditional logit analysis of qualitative choice behavior. In: Zarembka P, Hrsg. Frontiers of econometrics. New York: Academic Press; 1974. p. 105–42.
McFadden D. Econometric models of probabilistic choice. In: Manski CF, McFadden D, Hrsg. Structural analysis of discrete data with econometric applications. Cambridge: The MIT Press; 1981. p. 198–272.
McFadden D. Economic choices. Am Econ Rev. 2001;91(3):351–78.
Louviere JJ, Hensher DA, Swait JD. Stated choice methods—analysis and application. Cambridge: Cambridge University Press; 2000.
Hanemann MW. Marginal welfare measures for discrete choice models. Econ Lett. 1983;13:129–36.
Salkeld G, Ryan M, Short L. The veil of experience: do consumers prefer what they know best? Health Econ. 2000;9(3):267–70.
Zweifel P, Telser H, Vaterlaus S. Consumer resistance against regulation: the case of health care. J Regul Econ. 2007;29(3):319–32.
Telser H, Zweifel P. Measuring willingness-to-pay for risk reduction—an application of conjoint analysis. Health Econ. 2002;11:129–39.
Mullahy J, Manning WG. Statistical issues in cost-effectiveness analysis. In: Sloan FA, Hrsg. Valuing health care—costs, benefits, and effectiveness of pharmaceuticals and other medical technologies. New York: Cambridge University Press; 1996. S. 149–84.
Efron B, Tibshirani R. An introduction to the bootstrap. New York: Chapman & Hall; 1993.
Johnson FR, Desvousges WH. Estimating stated preferences with rated-pair data: environmental, health, and employment effects of energy programs. J Environ Econ Manag. 1997;34:79–99.
Sennhauser M. Why the linear utility function is a risky choice in discrete-choice experiments. Working Papers 1014, Department of Economics University of Zurich. 2009.
Williams A, Cookson R. Equity in health. In: Culyer A, Newhouse J, Hrsg. Handbook of health economics. Bd. 1B. Amsterdam: Elsevier; 2000. S. 1863–910.
Culyer A. Commodities, characteristics of commodities, characteristics of people, utilities, and quality of life. In: Baldwin S, Godfrey C, Propper C, Hrsg. Quality of life: perspectives and policies. London: Routledge; 1990. S. 9–27.
Drummond M, Sculpher M, Torrance G, O’Brien B, Stoddart G. Methods for the economic evaluation of health.
Danksagung
Die Autoren bedanken sich bei zwei anonymen GutachterInnen sowie insbesondere Prof. Axel Mühlbacher (Potsdam) für eine äußerst genaue Lektüre des Textes, die zur Klärung einer ganzen Reihe von Punkten geführt hat.
Open Access
Dieser Artikel unterliegt den Bedingungen der Creative Commons Attribution License. Dadurch sind die Nutzung, Verteilung und Reproduktion erlaubt, sofern der/die Originalautor/en und die Quelle angegeben sind.
Author information
Authors and Affiliations
Corresponding author
Rights and permissions
Open Access This article is distributed under the terms of the Creative Commons Attribution 4.0 International License (https://creativecommons.org/licenses/by/4.0), which permits use, duplication, adaptation, distribution, and reproduction in any medium or format, as long as you give appropriate credit to the original author(s) and the source, provide a link to the Creative Commons license, and indicate if changes were made.
About this article
Cite this article
Sennhauser, M., Zweifel, P. Ist ein neues Arzneimittel sein Geld wert? Wessen Geld? – Bewertung eines neuen Diabetes-Präparats mit Hilfe eines Discrete-Choice-Experiments. PharmacoEcon. Ger. Res. Artic. 11, 45–63 (2013). https://doi.org/10.1007/s40275-014-0010-9
Published:
Issue Date:
DOI: https://doi.org/10.1007/s40275-014-0010-9