Abstract
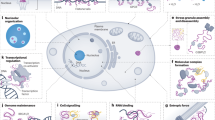
In contrast to folded proteins, intrinsically disordered proteins (IDPs) exert their functions in the absence of a stable three-dimensional structure. They are active in many important cellular mechanisms, for example cell signaling and transcriptional regulation and thus very important cellular players. Their dynamics make them extremely difficult to study, but recent advances in solution based structural biology techniques have increased the understanding of IDPs’ functions on a molecular level.
Article PDF
Similar content being viewed by others
Avoid common mistakes on your manuscript.
Literatur
Uversky VN (2013) Disorder in the lifetime of a protein. Intrinsically Disord Proteins 1: e26782
Jumper J, Evans R, Pritzel A et al. (2021) Highly accurate protein structure prediction with AlphaFold. Nature 596: 583–589
Cordeiro TN, Herranz-Trillo F, Urbanek A et al. (2017) Structural Characterization of Highly Flexible Proteins by Small-Angle Scattering. Adv Exp Med Biol 1009: 107–129
Schuler B, Soranno A, Hofmann H, Nettels D (2016) Single-Molecule FRET Spectroscopy and the Polymer Physics of Unfolded and Intrinsically Disordered Proteins. Annu Rev Biophys 45: 207–231
Milles S, Salvi N, Blackledge M, Jensen MR (2018) Characterization of intrinsically disordered proteins and their dynamic complexes: From in vitro to cell-like environments. Prog Nucl Magn Reson Spectrosc 109: 79–100
Necci M, Piovesan D, CAID Predictors et al. (2021) Critical assessment of protein intrinsic disorder prediction. Nat Methods 18: 472–481
Naudi-Fabra S, Tengo M, Jensen MR et al. (2021) Quantitative Description of Intrinsically Disordered Proteins Using Single-Molecule FRET, NMR, and SAXS. J Am Chem Soc 143: 20109–20121
Guseva S, Milles S, Jensen MR et al. (2020) Measles virus nucleo- and phosphoproteins form liquid-like phase-separated compartments that promote nucleocapsid assembly. Sci Adv 6: eaaz7095
Funding
Open Access funding enabled and organized by Projekt DEAL.Open Access funding enabled and organized by Projekt DEAL.
Author information
Authors and Affiliations
Corresponding author
Additional information
Danksagung
Für dieses Projekt wurden Fördermittel des Europäischen Forschungsrats (ERC) im Rahmen des Programms der Europäischen Union für Forschung und Innovation „Horizont 2020“ bereitgestellt (Finanzhilfevereinbarung Nr. 802209).
Sigrid Milles 2004–2009 Studium der Biophysik an der HU Berlin und der Universität Paris VII, Frankreich. 2013 Promotion am European Molecular Biology Laboratory (EMBL) und der Universität Heidelberg. 2014–2022 Postdoc und CNRS-Wissenschaftlerin am Institut de Biologie Structurale in Grenoble, Frankreich. 2021 Habilitation im Fach Biologie an der Université Grenoble Alpes. Seit 2022 Junior-Gruppenleiterin am Leibniz-Forschungsinstitut für Molekulare Pharmakologie (FMP), Berlin.
Rights and permissions
Dieser Artikel wird unter der Creative Commons Namensnennung 4.0 International Lizenz veröffentlicht, welche die Nutzung, Vervielfältigung, Bearbeitung, Verbreitung und Wiedergabe in jeglichem Medium und Format erlaubt, sofern Sie den/die ursprünglichen Autor(en) und die Quelle ordnungsgemäß nennen, einen Link zur Creative Commons Lizenz beifügen und angeben, ob Änderungen vorgenommen wurden. Die in diesem Artikel enthaltenen Bilder und sonstiges Drittmaterial unterliegen ebenfalls der genannten Creative Commons Lizenz, sofern sich aus der Abbildungslegende nichts anderes ergibt. Sofern das betreffende Material nicht unter der genannten Creative Commons Lizenz steht und die betreffende Handlung nicht nach gesetzlichen Vorschriften erlaubt ist, ist für die oben aufgeführten Weiterverwendungen des Materials die Einwilligung des jeweiligen Rechteinhabers einzuholen. Weitere Details zur Lizenz entnehmen Sie bitte der Lizenzinformation auf http://creativecommons.org/licenses/by/4.0/deed.de.
About this article
Cite this article
Milles, S. Die dynamische Funktion intrinsisch ungeordneter Proteine. Biospektrum 29, 351–353 (2023). https://doi.org/10.1007/s12268-023-1966-z
Published:
Issue Date:
DOI: https://doi.org/10.1007/s12268-023-1966-z