Abstract
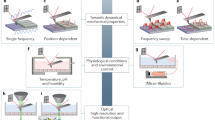
The ability of cells to sense and respond to extracellular forces is critical for cellular and tissue homeostasis. Tension or compression act on our body ubiquitously and cells respond to such mechanical cues by producing intracellular forces on their own. In this article, we briefly highlight the cellular and physical basis driving these phenomena and discuss our recent technical advance to stimulate and monitor the cellular mechanoresponse on a molecular scale.
Article PDF
Similar content being viewed by others
Avoid common mistakes on your manuscript.
Literatur
Orr AW, Helmke BP, Blackman BR et al. (2006) Mechanisms of mechanotransduction. Dev Cell 10: 11–20
Janmey PA, Miller RT (2011) Mechanisms of mechanical signaling in development and disease. J Cell Sci 124: 9–18
Choquet D, Felsenfeld DP, Sheetz MP (1997) Extracellular matrix rigidity causes strengthening of integrin-cytoskeleton linkages. Cell 88: 39–48
Brown AE, Discher DE (2009) Conformational changes and signaling in cell and matrix physics. Curr Biol 19: R781–789
Uhler C, Shivashankar GV (2017) Regulation of genome organization and gene expression by nuclear mechanotransduction. Nat Rev Mol Cell Biol 18: 717–727
Finer JT, Simmons RM, Spudich JA (1994) Single myosin molecule mechanics: piconewton forces and nanometre steps. Nature 368: 113–119
Balaban NQ, Schwarz US, Riveline D et al (2001) Force and focal adhesion assembly: a close relationship studied using elastic micropatterned substrates. Nat Cell Biol 3: 466–472
Kamble H, Barton MJ, Jun M et al. (2016) Cell stretching devices as research tools: engineering and biological considerations. Lab Chip 16: 3193–3203
Roca-Cusachs P, Conte V, Trepat X (2017) Quantifying forces in cell biology. Nat Cell Biol 19: 742–751
Hippler M, Weißenbruch K, Richler K et al. (2020) Mechanical stimulation of single cells by reversible host-guest interactions in 3D microscaffolds. Sci Adv 6: 1–13
Hahn C, Mayer F, Thiel M et al. (2019) 3-D Laser Nanoprinting. OPN 30: 28–35
Webster KD, Ng WP, Fletcher DA (2014) Tensional homeostasis in single fibroblasts. Biophys J 107: 146–155
Vicente-Manzanares M, Ma X, Adelstein RS et al. (2009) Non-muscle myosin II takes centre stage in cell adhesion and migration. Nat Rev Mol Cell Biol 10: 778–790
Funding
Funding note: Open Access funding enabled and organized by Projekt DEAL.
Author information
Authors and Affiliations
Corresponding authors
Additional information
Kai Weißenbruch 2010–2015 Studium der allgemeinen Biologie, KIT. 2016–2019 Promotion am Zoologischen Institut, Zell-und Neurobiologie, KIT. Seit 2020 Postdoc am Zoologischen Institut, Zell- und Neurobiologie, KIT, mit Schwerpunkten in Zellbiologie und Mechanobiologie.
Marc Hippler 2010–2016 Physikstudium am KIT. 2016–2020 Promotion am Institut für Angewandte Physik sowie am Zoologischen Institut, KIT. Seit 2021 wissenschaftlicher Mitarbeiter am Institut für Nanotechnologie, KIT. Forschungsschwerpunkt in der 3D-Laserlithografie für Anwendungen in den Biowissenschaften.
Martin Bastmeyer Studium der Biologe und Promotion. 1988–1994 Postdoc am Friedrich-Miescher-Labor in Tübingen und am Salk Institute in San Diego, CA, USA. 1990–1998 Wissenschaftlicher Mitarbeiter an der Universität Konstanz. 1998–2001 Heisenberg-Stipendium der DFG. 2001–2004 Professor für Neurobiologie an der Universität Jena. Seit 2004 Professor für Zell- und Neurobiologie am KIT und Leiter des Zoologischen Instituts.
Rights and permissions
Open Access: Dieser Artikel wird unter der Creative Commons Namensnennung 4.0 International Lizenz veröffentlicht, welche die Nutzung, Vervielfältigung, Bearbeitung, Verbreitung und Wiedergabe in jeglichem Medium und Format erlaubt, sofern Sie den/die ursprünglichen Autor(en) und die Quelle ordnungsgemäß nennen, einen Link zur Creative Commons Lizenz beifügen und angeben, ob Änderungen vorgenommen wurden. Die in diesem Artikel enthaltenen Bilder und sonstiges Drittmaterial unterliegen ebenfalls der genannten Creative Commons Lizenz, sofern sich aus der Abbildungslegende nichts anderes ergibt. Sofern das betreffende Material nicht unter der genannten Creative Commons Lizenz steht und die betreffende Handlung nicht nach gesetzlichen Vorschriften erlaubt ist, ist für die oben aufgeführten Weiterverwendungen des Materials die Einwilligung des jeweiligen Rechteinhabers einzuholen. Weitere Details zur Lizenz entnehmen Sie bitte der Lizenzinformation auf http://creativecommons.org/licenses/by/4.0/deed.de.
About this article
Cite this article
Weissenbruch, K., Hippler, M. & Bastmeyer, M. Zelluläres Tauziehen: Wie Zellen auf mechanischen Stress antworten. Biospektrum 27, 385–389 (2021). https://doi.org/10.1007/s12268-021-1598-0
Published:
Issue Date:
DOI: https://doi.org/10.1007/s12268-021-1598-0