Abstract
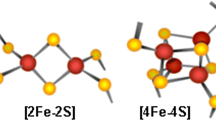
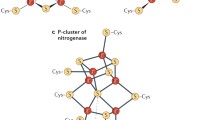
Iron-sulfur (FeS) clusters are versatile protein cofactors that fulfil numerous catalytic and regulatory functions in mitochondria, cytosol, and nucleus. Maturation of FeS proteins requires the mitochondrial iron-sulfur cluster assembly (ISC) and the cytosolic iron-sulfur protein assembly (CIA) machineries for de novo cluster synthesis on scaffold proteins, cluster trafficking via transfer proteins, and cluster integration into recipient apoproteins. Here, I provide a cursory overview of FeS protein function and maturation.
Article PDF
Similar content being viewed by others
Avoid common mistakes on your manuscript.
Literatur
Kispal G, Csere P, Prohl C et al. (1999) The mitochondrial proteins Atm1p and Nfs1p are essential for biogenesis of cytosolic Fe/S proteins. Embo J 18:3981–3989
Schilke B, Voisine C, Beinert H et al. (1999) Evidence for a conserved system for iron metabolism in the mitochondria of Saccharomyces cerevisiae. Proc Natl Acad Sci USA 96:10206–10211
Balk J, Schaedler TA (2014) Iron cofactor assembly in plants. Annu Rev Plant Biol 65:125–153
Braymer JJ, Lill R (2017) Iron-sulfur cluster biogenesis and trafficking in mitochondria. J Biol Chem 292:12754–12763
Ciofi-Baffoni S, Nasta V, Banci L (2018) Protein networks in the maturation of human iron-sulfur proteins. Metallomics 10:49–72
Lill R, Freibert SA (2020) Mechanisms of mitochondrial iron-sulfur protein biogenesis. Annu Rev Biochem, doi: https://doi.org/10.1146/annurev-biochem-013118-111540
Paul VD, Lill R (2015) Biogenesis of cytosolic and nuclear iron-sulfur proteins and their role in genome stability. Biochim Biophys Acta 1853:1528–1539
Barton JK, Silva RMB, O’Brien E (2019) Redox chemistry in the genome: emergence of the [4Fe4S] cofactor in repair and replication. Annu Rev Biochem 88:163–190
Boniecki MT, Freibert SA, Muhlenhoff U et al. (2017) Structure and functional dynamics of the mitochondrial Fe/S cluster synthesis complex. Nat Commun 8:1287
Fox NG, Yu X, Feng X et al. (2019) Structure of the human frataxin-bound iron-sulfur cluster assembly complex provides insight into its activation mechanism. Nat Commun 10:2210
Pandey AK, Pain J, Dancis A et al. (2019) Mitochondria export iron-sulfur and sulfur intermediates to the cytoplasm for iron-sulfur cluster assembly and tRNA thiolation in yeast. J Biol Chem 294:9489–9502
Srinivasan V, Pierik AJ, Lill R (2014) Crystal structures of nucleotide-free and glutathione-bound mitochondrial ABC transporter Atm1. Science 343:1137–1140
Stehling O, Jeoung JH, Freibert SA et al. (2018) Function and crystal structure of the dimeric P-loop ATPase CFD1 coordinating an exposed [4Fe-4S] cluster for transfer to apoproteins. Proc Natl Acad Sci USA 115:E9085–E9094
Stehling O, Wilbrecht C, Lill R (2014) Mitochondrial iron-sulfur protein biogenesis and human disease. Biochimie 100:61–77
Funding
Funding: Open Access funding provided by Projekt DEAL.
Author information
Authors and Affiliations
Corresponding author
Additional information
Danksagung
Unsere Arbeiten wurden unter anderem von DFG, EU, German-Israeli Foundation (GIF) und der Alexander-von-Humboldt-, Behring-Röntgen- und Volkswagen-Stiftung großzügig gefördert.
Roland Lill 1976–1981 Chemiestudium an den Universitäten Ulm und München. 1986 Promotion in Biochemie an der LMU München bei Prof. Dr. W. Wintermeyer. 1987–1989 DFG-Stipendiat an der University of California, Los Angeles, USA bei Prof. Dr. W. T. Wickner. 1990–1996 Gruppenleiter an der LMU München bei Prof. Dr. W. Neupert. Seit 1996 Professor für Zellbiologie am Institut für Zytobiologie, Universität Marburg; seit 2000 dessen Leiter. 2009–2014 Fellow der Max-PlanckGesellschaft.
Rights and permissions
Open Access: Dieser Artikel wird unter der Creative Commons Namensnennung 4.0 International Lizenz veröffentlicht, welche die Nutzung, Vervielfältigung, Bearbeitung, Verbreitung und Wiedergabe in jeglichem Medium und Format erlaubt, sofern Sie den/die ursprünglichen Autor(en) und die Quelle ordnungsgemäß nennen, einen Link zur Creative Commons Lizenz beifügen und angeben, ob Änderungen vorgenommen wurden. Die in diesem Artikel enthaltenen Bilder und sonstiges Drittmaterial unterliegen ebenfalls der genannten Creative Commons Lizenz, sofern sich aus der Abbildungslegende nichts anderes ergibt. Sofern das betreffende Material nicht unter der genannten Creative Commons Lizenz steht und die betreffende Handlung nicht nach gesetzlichen Vorschriften erlaubt ist, ist für die oben aufgeführten Weiterverwendungen des Materials die Einwilligung des jeweiligen Rechteinhabers einzuholen. Weitere Details zur Lizenz entnehmen Sie bitte der Lizenzinformation auf http://creativecommons.org/licenses/by/4.0/deed.de.
About this article
Cite this article
Lill, R. Funktion und Biogenese von Eisen-Schwefel-Proteinen in Eukaryoten. Biospektrum 26, 242–245 (2020). https://doi.org/10.1007/s12268-020-1372-8
Published:
Issue Date:
DOI: https://doi.org/10.1007/s12268-020-1372-8