Abstract
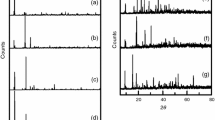
Thermogravimetry, differential thermal, X-ray diffraction and infrared spectroscopy analyses showed La(CH3COO)3·1.5H2O to decompose completely at 700°C yielding La2O3. The results revealed that the compound dehydrates in two steps at 130 and 180°C, and recrystallizes at 210°C. Water thus produced hydrolyzes surface acetates (at 310°C), releasing acetic acid into the gas phase. At 334°C, the anhydrous acetate releases gas phase CH3COCH3 to give La2(CO3)3 residue, which decomposes to La2O2(CO3) via the intermediate La2O(CO3)2. On further heating up to 700°C, La2O3 is formed. IR spectroscopy of the gaseous products indicated a chemical reactivity at gas/solid interfaces formed throughout the decomposition course. As a result, CH3COCH3 was involved in a surface-mediated, bimolecular reaction, releasing CH4 and C4H8 (isobutene) into the gas phase.
Non-isothermal kinetic parameters, the rate constantk, frequency factorA, and activation energy ΔE, were calculated on the basis of temperature shifts experienced in the thermal processes encountered, at various heating rates (2–20 deg·min−1).
Zusammenfassung
TG, DTA, Röntgendiffraktion und IR-Spektroskopie zeigen eine vollständige Zersetzung von La(CH3COO)3·1,5H2O zu La2O3 bei 700°C. Die Ergebnisse zeigen daß die Verbindung in zwei Schritten, bei 130 und bei 180°C dehydratiert und bei 210°C umkristallisiert wird. Das auf diese Weise entstehende Wasser hydrolisiert Oberflächenacetat (bei 310°C), wodurch Essigsäure in die Gasphase übergeht. Bei 334°C setzt das wasserfreie Acetat gasförmiges CH3COCH3 frei und ergibt La2(CO3)3 als Rückstand, der sich über das Zwischenprodukt La2O(CO3)2 zu La2O2(CO3) zersetzt. Durch weiteres Erhitzen auf 700°C wird La2O3 gebildet. IR-Spektroskopie der gasförmigen Produkte zeigt eine chemische Reaktivität an den wahrend des Zersetzungsweges gebildeten Gas/Feststoff-Phasengrenzen. Im Ergebnis wird Aceton in einer bimolekularen Oberflächenreaktion umgesetzt, wobei CH4 und C4H8 (Isobuten) in die Gasphase abgegeben wird.
Nichtisotherme kinetische Parameter, die Geschwindigkeitskonstantek, der FrequenzfaktorA und die Aktivierungsenergie ΔE wurden anhand der Temperaturverschiebungen im thermischen Prozeß für verschiedene Aufheizgeschwindigkeiten (2–20 deg·min−1) berechnet.
Similar content being viewed by others
References
M. E. Brown, D. Dollimore and A. K. Galwey, Reactions in the Solid State, Comprehensive Chemical Kinetics; C. H. Bamford and C. E. H. Tipper (Eds.) Vol. 22, Elsevier, Amsterdam 1980.
A. K. Galwey, S. G. Mckee, T. R. B. Mitchell, M. E. Brown and A. F. Bean, Reactivity of Solids, 6 (1988) 173.
S. A. A. Mansour, G. A. M. Hussein and M. I. Zaki, Reactivity of Solids, 8 (1990) 197.
M. A. Bernard and F. Busnott, Bull. Soc. Chim. Fr. 5 (1968) 2000.
B. Dlmon, P. Grange, P. A. Jacobs and G. Poncelet (Eds.) Preparation of Catalysts II, Elsevier, Amsterdam 1970.
G. A. M. Hussein, N. Sheppard, M. I. Zaki and R. B. Fahim, J. Chem. Soc. Faraday Trans. I 85 (1989) 1732.
C. H. K. D. Campbell, J. X. Wang and J. H. Lunsford, J. Phys. Chem., 90 (1986) 534.
M. P. Rosynek and D. T. Magnison, J. Catal., 46 (1977) 402.
W. Zuou, D. A. Jefferson and W. Y. Liang, Surf. Sci., 209 (1989) 444.
K. C. Patil, G. V. Chandraskar, M. V. George and C. N. R. Rao, Can. J. Chem., 46 (1968) 257.
R. C. Paul, M. S. Bains and J. S. Ghotra, Indian J. Chem., 7 (1969) 514.
J. V. Smith (Ed.), X-ray Powder Data File, American Society for Testing and Materials, Philadelphia 1980.
J. B. Peri and R. H. Hannan, J. Phys. Chem., 64 (1960) 1526.
J. H. Flynn, J. Thermal Anal., 27 (1983) 45.
A. W. Coats and J. P. Redfern, Nature, 201 (1964) 68.
K. Nakamoto, Infrared Spectra of Inorganic and Coordination Compounds, John Wiley and Sons, New York 1970 p. 253.
D. M. Griffiths and C. H. Rochester, J. Chem. Soc. Faraday Trans. I, 74 (1987) 403.
R. H. Pierson, A. M. Fletcher and E. St. Clair Gabtz, Anal. Chem., 28 (1956) 1218.
S. S. Moosath, J. Abraham and T. V. Swaminathan, Z. Anorg. Allg. Chem., 324 (1963) 30.
J. A. Goldsmith and S. D. Ross, Spectrochim. Acta, 23A (1967) 1909.
G. A. M. Hussein, Thermochim. Acta, 180 (1991) 187.
M. I. Zaki and N. Sheppard, J. Catal., 80 (1983) 114.
M. D. Judd, B. A. Plunkett and M. I. Pope, J. Thermal Anal., 6 (1974) 555.
Author information
Authors and Affiliations
Rights and permissions
About this article
Cite this article
Hussein, G.A.M. Spectrothermal investigation of the decomposition course of lanthanum acetate hydrate. Journal of Thermal Analysis 42, 1091–1102 (1994). https://doi.org/10.1007/BF02546919
Received:
Revised:
Issue Date:
DOI: https://doi.org/10.1007/BF02546919