Summary
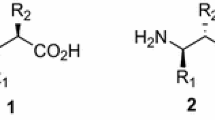
The synthesis of both enantiomers of norephedrine and norisoephedrine is described to present a method for the preparation of enantiomerically pure branched 1,2-aminoalcohols. In a one pot reaction enantiomerically pure cyanohydrins bearing an acetal protective group are subjected to Grignard-reaction followed by addition of lithium aluminum hydride. After deprotection the target compounds are obtained.
Similar content being viewed by others
Literatur und bemerkungen
Noe C. R., Knollmüller M., Kürner H., Steinbauer G. (1990) Öst. Pat. 390789, 25. 6. 1990 (Prior. 3. 11. 88, AT 2071/88);
Noe C. R., Knollmüller M., Kürner H. (1989) Eur. Pat. 0162235, 18. 1. 1989 (Prior. 4. 4. 84, AT 1136/84)
Noe C. R., Knollmüller M., Göstl G., Gärtner P. (1989) Öst. Pat. Anm. 958/89, 21. 4. 1989;
Noe C. R., Fleischhacker W., Gärtner P., Katikarides E. (1989) Arch. Pharm. Weinheim322: 171;
Noe C. R., Knollmüller M., Ettmayer P., Gärtner P., Letschnig M. (1990) Öst. Chem. Z.91: 36
Noe C. R., Knollmüller M., Steinbauer G., Jangg E., Völlenkle H. (1988) Chem. Ber.121: 1231. Das Reagens kann auch in seiner „dimeren“ Form (MBE)2O eingesetzt werden
Noe C. R. (1985) US. Patent 4,497,960, 5. 2. 1985 (Prior. 18. 12. 1981, AT 5453/88)
Noe C. R. (1982) Chem. Ber.115: 1591
Dungler K. (1988) Dissertation. TU-Wien
Becker W., Freund H., Pfeil E. (1965) Angew. Chem.77: 1139;
Brussee J., Jansen A. C. A., Kühn A. (1984) Vortrag, 8th Int. Symp. of Med. Chem., Uppsala;
Effenberger F., Ziegler T., Forster S. (1987) Angew. Chem. Int. Ed.26: 458;
Becker W., Pfeil E. (1966) J. Amer. Chem. Soc.88: 4299
Oku J., Ito N., Inoue S. (1982) Makromol. Chem.183: 579;
Asada S., Kobayashi Y., Inoue S. (1985) Makromol. Chem.186: 1755;
Stoutamire D. W., Tieman C. H., Dong W. (1984) EP 0109681 Shell Oil Co., 30. 5. 1984 (Prior. 22. 11. 82, US 443513);
Jackson W. R., Jayatilake G. S., Matthews B. R., Wilshire C. (1988) Aust. J. Chem.41: 203;
Matthews B. R., Jackson W. R., Jayatilake G. S., Wilshire C., Jacobs H. A. (1988) Aust. J. Chem.41: 1697;
Narasaka K., Yamada T., Minamikawa H. (1987) Chem. Lett.: 2073;
Kenji K., Mitsunori M., Satomi T., Tarumi-ku S., Takeshi O., Kiyoshi W. (1987) Kanegafu Chemical Industry Co., Ltd., EP Appl. 871185518
Bei üblicherweise durchgeführten 90 MHz-1H-NMR Routineaufnahmen liegt die Nachweisgrenze für das jeweils im Unterschuß vorliegende Diastereomer bei 1–3%; Ecker G., Fleischhacker W., Noe C. R. (1989) Sci. Pharm.57: 171
Jackson W. R., Jacobs H. A., Matthews B. R., Jayatilake G. S., Watson K. G. (1990) Tetrahedron Lett.31: 1447;
Brussee J., Dofferhoff F., Kruse C. G., van der Gen A. (1990) Tetrahedron46: 1653;
Brussee J., van Benthem R. A. T. M., Kruse C. G., van der Gen A. (1990) Tetrahedron Asym.1: 163
Zur Bezeichnung AA-Typ bzw. BB-Typ siehe: Noe C. R., Knollmüller M., Göstl G., Oberhauser B., Völlenkle H. (1987) Angew. Chem.99: 467. Für Systeme, in denen zwei gleichartige Liganden b bzw. pl auftreten, wird jeweils der kleinere Ligand mit b′ bzw. pl′ bezeichnet und ihm die niedrigere Priorität eingeräumt. Für das jeweilige Chiralitätszentrum ergibt sich dann für die Fälle b, b′, H bzw. pl, pl′, H in Analogie zur b, pl, H-Regel die Typenbezeichnung A′ bzw. B′
Nagai W. N., Kanao S. (1929) Justus Liebigs Ann. Chem.470: 157
Fles D., Markovac-Prpic A. (1957) Croat. Chem. Acta29: 183
Prelog V., Mutak S. (1983) Helv. Chim. Acta66: 2274
Author information
Authors and Affiliations
Additional information
Dr. Paul Löw-Beer zum 80. Geburtstag gewidmet
Rights and permissions
About this article
Cite this article
Noe, C.R., Knollmüller, M., Göstl, G. et al. Aminoalkohole, 1. Mitt.: Ein Verfahren zur Synthese enantiomerenreiner 1,2-Aminoalkohole miterythro-Konfiguration. Monatsh Chem 122, 283–290 (1991). https://doi.org/10.1007/BF00810829
Received:
Accepted:
Issue Date:
DOI: https://doi.org/10.1007/BF00810829