Summary
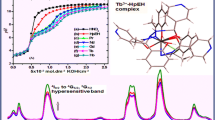
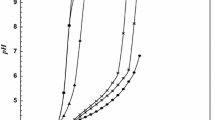
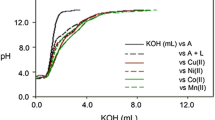
Equilibria between 2-hydroxy naphthaldehyde derivatives (semicarbazone and thiosemicarbazone) and proton or some bivalent metal ions have been investigated potentiometrically at a constant ionic strength and different compositions of the mixed solvent (dioxane: water). The method of Bjerrum and Calvin [1, 2], as modified by Irving and Rossotti [3], has been used to determine the values ofn andpL. The stability constants have been calculated following Sullivan et al. [4] to give β n values. The values ofS min=χ2 have also been calculated. The order of stability constants was found to be found to be UO 2+2 > Cu2+ > Ni2+ > Co2+ > Zn2+ > Pb2+ > Cd2+ > Mn2+ > Mg2+. The effect of varying the dielectric constant of the medium on the stability constants of the complexes has also been investigated at an ionic strength of 0.100M NaClO4 and a temperature of 20±0.5°C.
Zusammenfassung
Es wurden die Gleichgewichte zwischen 2-Hydroxynaphthaldehyd-Semicarbazonen und -Thiosemicarbazonen einerseits und Proton oder zweiwertigen Übergangsmetallionen andererseits potentiometrisch bei einer konstanten Ionenstärke und verschiedenen Zusammensetzungen von Dioxan und Wasser als gemischtem Lösungsmittel untersucht. Die Methode von Bjerrum und Calvin nach der Modifikation von Irving und Rossotti wurde zur Evaluierung der Werte fürn undpL verwendet. Die Stabilitätskonstanten und β n -Werte wurden nach Sullivan et al. berechnet. Die WerteS min=χ2 wurden ebenfalls bestimmt. Die Reihenfolge der Stabilitätskonstanten war UO 2+2 > Cu2+ > Ni2+ > Co2+ > Zn2+ > Pb2+ > Cd2+ > Mn2+ > Mg2+. Außerdem wurde der Effekt wechselnder Dielektrizitätskonstanten des Lösungsmittels auf die Stabilitätskonstanten der Komplexe bei einer Ionenstärke von 0.100M NaClO4 und einer Temperature von 20±0.5°C untersucht.
Similar content being viewed by others
References
Calvin M., Wilson K. W. (1945) J. Am. Chem. Soc.67: 2003
Bjerrum J. (1941) Metal Ammine Formation in Aqueous Solutions. Hasse, Copenhagen, p. 298
Irving H. M., Rossotti H. S. (1954) J. Chem. Soc.: 2904
Sullivan J., Rydberg J., Miller W. F. (1959) Acta Chem. Scand.13: 2023
Salinas F., Jimenez Sanchez J. C., Lozazo Ruiz M. M. (1987) Bull. Soc. Chim. Belg.96 (1: 73–74
Ting P. H., Wilson F. D., Chance B. (1970) Arch. Biochem. Biophys.141 (1: 141–146
Bareet P. A. (1965) Nature206: 1340
Doamaral J. R., Blanz E. J., French F. A. (1969) J. Med. Chem.12: 21
Bauer D. J., Vincent L. St., Kempe C. H., Downe A. W. (1963) Lancet2: 494
Petring H. G., Buskirk H. H., Underwood G. E. (1964) Cancer Res.64: 367
Orlova N. N., Aksevova V. A., Selidovkin D. A., Bogdanova N. S., Perslin G. N. (1968) Russ. Pharm. Toxical.348
Domagk G., Behnisch R., Mietzsch F., Schmidt H. (1946) Naturwissenschaften33: 315
Sahadev, Sharma R. K., Sindhwani S. K. (1988) Indian J. Chem.27 A: 643
Sahadev, Sharma R. K., Sindhwani S. K. (1988) Thermochimica Acta126: 1
Varshney A., Tandon J. P., Crowe A. J. (1986) Polyhedron5 (3: 739–742
Vogel A. I. (1956) A Text Book of Practical Organic Chemistry. Longmans, New York, p. 177
Van Uitert L. G., Hass C. G. (1953) J. Am. Chem. Soc.75: 451
Rao U. B., Mathur H. B. (1969) Indian J. Chem.7: 1234
Rydberg J., Sullivan J. C. (1959) Acta Chem. Scand.13: 2059
Mellor D. P., Maley L. (1947) Nature159: 370
Irving H., Williams R. J. P. (1948) Nature162: 746
Irving H., Williams R. J. P. (1952) Analyst77: 813
Stability constants of metal ion complexes, Part I, The Chemical Soc., London, p. 2, 3, 5, 10, 13 (1957)
Schin-ichi I., Oka Y., Ohtaki H. (1983) Bull. Chem. Soc.56: 2426
Gergely A., Kiss T. (1977) J. Inorg. Nucl. Chem.39: 109
Irving H. M., Rossotti H. S. (1956) Acta Chem. Scand.10: 72
Rorabacher D. B., Mackellar W. J., Shu F. R., Bonavita (1971) Anal. Chem.43: 561
Braude E. A., Stern E. S. (1948) J. Chem. Soc.1976
Hammet L. P. (1940) Physical Organic Chemistry. McGraw Hill, New York, p. 204
Author information
Authors and Affiliations
Rights and permissions
About this article
Cite this article
Sahadev, Sharma, R.K. & Sindhwani, S.K. Stabilities of some bivalent transition metal ions with 2-hydroxy naphthaldehyde semicarbazones and thiosemicarbazones in dioxane-water mixtures: A potentiometric study. Monatsh Chem 123, 1099–1105 (1992). https://doi.org/10.1007/BF00808272
Received:
Accepted:
Issue Date:
DOI: https://doi.org/10.1007/BF00808272