Summary
-
1.
Proteolytic enzymes ofCulex pipiens pipiens (autogenous) andC. p. fatigans (anautogenous) were investigated qualitatively and quantitatively in the larvae, pupae and adults.
-
2.
The use of synthetic substrates allowed identification of four distinct proteolytic enzymes, trypsin, chymotrypsin, leucine aminopeptidase and carboxypeptidase A. Chymotrypsin is present only in the larva, whereas the other proteases were observed in all developmental stages. TheCulex trypsin can be characterized as follows: 1. It has a distinct esterase specificity with a preference for arginine esters. 2. Its pH optimum is in the alkaline range (8.4). 3. The inhibition by diisopropylfluorophosphate suggests the presence of a serine residue in the active center. 4. There is neither an activating nor a stabilizing effect of calcium. 5. Like bovine trypsin, the enzyme is positively charged at neutral pH, but has a lower electrophoretic mobility.
-
3.
A comparison of proteolytic activities present in the midgut and in the whole animal demonstrates distinct differences in the relative distribution of the individual enzymes. Of the total trypsin activity, 95% is in the midgut, and the corresponding values are 187% for chymotrypsin, 78% for leucine aminopeptidase and 62% for carboxypeptidase A.
-
4.
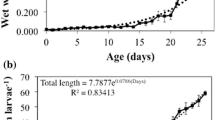
In the course of larval growth proteolytic activity increases rapidly. At the onset of puparium formation a rapid decrease occurs. Levels of proteolytic activity are low in the pupae, suggesting that these enzymes are not involved in the histolytic processes. Adults fed on sugar show still lower values.
-
5.
In sugar-fed females, the uptake of blood results in a sudden increase of the proteolytic activity. At 48 h, a maximal level is reached, representing a 30-fold increase over the initial activity. The rapid decrease of the proteolytic activity observed by day 4 after the blood meal indicates that digestion is complete.
-
6.
The present study shows that the proteolytic activities in the autogenous and anautogenous form are comparable.
Zusammenfassung
-
1.
Proteolytische Enzyme vonCulex pipiens pipiens (autogen) undC. p. fatigans (anautogen) wurden in Larven, Puppen und Imagines qualitativ und quantitativ untersucht.
-
2.
Mit synthetischen Substraten konnten vier proteolytische Komponenten identifiziert werden: Trypsin, Chymotrypsin, Leucinaminopeptidase und Carboxypeptidase A. Während Chymotrypsin nur in Larven vorkommt, lassen sich die anderen drei Proteasen in allen Entwicklungsstadien nachweisen. Die Charakterisierung desCulex-Trypsins ergibt: 1. Strikte Esterasespezifität mit deutlicher Bevorzugung von Argininestern. 2. pH-Optimum im basischen Bereich (8,4). 3. Hemmung durch Diisopropylfluorophosphat als Hinweis auf einen Serinrest im aktiven Zentrum. 4. Keine aktivierende oder stabilisierende Wirkung von Calcium. 5. Bei neutralem pH positive Ladung entsprechend Rindertrypsin, aber geringere elektrophoretische Beweglichkeit.
-
3.
Ein Vergleich zwischen den proteolytischen Aktivitäten im Mitteldarm und im Ganztier ergibt für die einzelnen Enzyme eine unterschiedliche prozentuale Verteilung. Der Anteil im Darm beträgt: Trypsin 95%, Chymotrypsin 187%, Leucinaminopeptidase 78%, Carboxypeptidase A 62%.
-
4.
Die proteolytische Aktivität steigt in Larven während des Wachstums rasch an. Mit Beginn der Verpuppung erfolgt ein steiler Abfall. Die Enzymtätigkeit in den Puppen ist gering und deutet nicht auf eine Beteiligung an histolytischen Prozessen. Noch tiefere Werte kennzeichnen die zuckergefütterten Imagines.
-
5.
Die Blutmahlzeit bewirkt einen sprunghaften Anstieg der niedrigen proteolytischen Aktivität in zuckergefütterten Weibchen. Nach 48 Std wird ein Maximum, das 30fache des Ausgangswertes, erreicht. Ein ebenso steiler Abfall weist auf eine abgeschlossene Verdauung nach 4 Tagen hin.
-
6.
Ein Vergleich der Proteasenaktivität zwischen der autogenen und der anautogenen Culexform ergibt eine weitgehende Übereinstimmung.
Similar content being viewed by others
Literatur
Applebaum, S. W., Birk, Y., Horpaz, J., Bondi, A.: Comparative studies on proteolytic enzymes ofTenebrio molitor L. Comp. Biochem. Physiol.11, 85–104 (1964)
Bernt, E., Bergmeyer, H. U.: Bestimmung der Leucinaminopeptidase. In: Bergmeyer, H. U., Methoden der enzymatischen Analysen, S. 833–835. Weinheim: Verlag Chemie 1962
Briegel, H.: Untersuchungen zum Aminosäuren- und Proteinstoffwechsel während der autogenen und anautogenen Eireifung vonCulex pipiens. J. Insect Physiol.15, 1137–1160 (1969)
Charney, J., Tomarelli, R. M.: A colorimetric method for the determination of the proteolytic activity of duodenal juice. J. biol. Chem.171, 501–505 (1947)
Chen, P. S.: Studies on the protein metabolism ofCulex pipiens L. I. Metabolic changes of free amino acids during larval and pupal development. J. Insect Physiol.2, 38–51 (1958)
Chen, P. S.: Studies on the protein metabolism ofCulex pipiens L. III. Comparative analysis of the protein contents in the larval haemolymph of autogenous and anautogenous forms. J. Insect Physiol.3, 335–344 (1959)
Chen, P. S.: Biochemical aspects of insect development. Basel: Karger 1971
Chen, P. S., Briegel, H.: Studies on the protein metabolism ofCulex pipiens L. V. Changes in free amino acids and peptides during embryonic development. Comp. Biochem. Physiol.14, 463–473 (1965)
Clements, A. N.: The physiology of mosquitoes. Oxford: Pergamon Press 1963
Combre, A., Beytout, D., Mouchet, J., Bastide, P.: Activités enzymatiques d'Aedes aegypti. J. Insect Physiol.17, 527–543 (1971)
Day, M. F.: The mechanism of food distribution to midgut or diverticula in the mosquito. Aust. J. biol. Sci.7, 515–524 (1954)
Day, M. F., Powning, R. F.: A study of the processes of digestion in certain insects. Aust. J. sci. Res. (B)2, 175–215 (1949)
Engelmann, F.: Food stimulated synthesis of intestinal proteolytic enzymes in the cockroachLeucophaea maderae. J. Insect Physiol.15, 217–235 (1969)
Erlanger, B., Edel, F., Cooper, A.: The action of Chymotrypsin on two new chromogenic substrates. Arch. Biochem. Biophys.115, 206–210 (1966)
Folk, J. E., Piez, K. A., Carrol, W. R., Gladner, J. A.: Carboxypeptidase B. IV. Purification and characterization of the porcine enzyme. J. biol. Chem.235, 2272–2279 (1960)
Fraser, A., Ring, R. A., Stewart, R. K.: Intestinal proteinases in an insect (Calliphora vomitoria). Nature (Lond.)192, 999–1000 (1961)
Gooding, R. H.: Physiological aspects of digestion of the blood meal byAedes aegypti andCulex fatigans Wiedemann. J. med. Ent.3, 53–60 (1966)
Gornall, A. G., Bardawill, C. J., David, M. M.: Determination of serum proteins by means of the biuret reaction. J. biol. Chem.177, 751–766 (1949)
Hosbach, H. A., Egg, A. H., Kubli, E.: Einfluß der Futterzusammensetzung auf Verdauungsenzym-Aktivitäten beiDrosophila melanogaster-Larven. Rev. Suisse Zool.79, 1049–1060 (1972)
Katzenellenbogen, B. S., Kafatos, F. C.: Proteinases of silkmoth moulting fluid: Physical and catalytic properties. J. Insect Physiol.17, 775–800 (1971)
Langley, P. A.: The control of the digestion in the tsetseflyGlossina morsitans. Enzyme activity in relation to the size and nature of the meal. J. Insect. Physiol.12, 439–448 (1966)
Lecadet, M., Dedonder, R.: Les protéases dePieris brassicae. I. Purification et propriétés. Bull. Soc. Chim. biol. (Paris)48, 631–660 (1966)
Lockshin, R. A., Williams, C. M.: Programmed cell death. V. Cytolytic enzymes in relation to the breakdown of the intersegmental muscles of silkmoths. J. Insect Physiol.11, 831–844 (1965)
Lowry, O. H., Rosenbrough, N. J., Farr, A. L., Randall, R. J.: Protein measurement with the folin phenol reagent. J. biol. Chem.193, 265–275 (1951)
Moser, J. G.: Reinigung und Charakterisierung einer Proteinase der Larve vonCalliphora erythrocephala Meigen. Biochem. Z.344, 337–352 (1966)
Persaud, C. E., Davey, K. G.: The control of protease synthesis in the intestine of adults ofRhodnius prolixus. J. Insect Physiol.17, 1429–1440 (1970)
Powning, R. F., Jrzykiewicz, H.: Studies on the digestive proteinase of clothes moth larvae (Tineola bisselliella). J. Insect Physiol.8, 267–274 (1962)
Reisfeld, R., Lewis, U., Williams, D.: Disk electrophoresis of basic proteins and peptides on polyacrylamide gels. Nature (Lond.)195, 281–283 (1962)
Schwert, G. W., Takenaka, Y.: A spectrometric determination of trypsin and chymotrypsin. Biochim. biophys. Acta (Amst.)16, 570–575 (1955)
Siegelmann, A. M., Carlson, A. S., Robertson, T.: Investigations of serum trypsin related substances. Arch. Biochem. Biophys.97, 159–163 (1962)
Snodgrass, R. E.: The anatomical life of the mosquito. Smithsonian misc. Collect.139, no. 8 (1959)
Srivastava, P. N., Auclair, J. L.: Characteristics and nature of proteases from the alimentary canal of the pea aphidAcrythosiphon pisum. J. Insect Physiol.9, 469–474 (1963)
Villez De, E. J.: Isolation of the proteolytic digestive enzymes from the gastric juice of the crayfishOrconectes virilis. Comp. Biochem. Physiol.14, 577–586 (1965)
Vithayathil, A. J., Buck, E., Bier, M., Nord, F. F.: On the mechanisms of enzyme action: LXXII. Comparative studies on trypsin of various origins. Arch. Biochem. Biophys.92, 532–540 (1961)
Waldner-Stiefelmeier, R. D.: Untersuchungen über die Proteasen im Wildtyp und in den Letalmutanten (lme undltr) vonDrosophila melanogaster. Z. vergl. Physiol.56, 268–289 (1967)
Yang, Y. J., Davies, D. M.: Trypsin and chymotrypsin during metamorphosis inAedes aegypti and properties of the chymotrypsin. J. Insect Physiol.17, 117–131 (1970)
Yang, Y. J., Davies, D. M.: Digestive enzymes in the excreta ofAedes aegypti larvae. J. Insect Physiol.17, 2119–2123 (1971)
Yang, Y. J., Davies, D. M.: A mosquito-chymotrypsin inhibitor in tissues of adultAedes aegypti. Comp. Biochem. Physiol.43B, 137–141 (1972)
Author information
Authors and Affiliations
Additional information
Die vorliegende Arbeit wurde teilweise mit Unterstützung durch den Schweizerischen Nationalfonds zur Förderung der wissenschaftlichen Forschung durchgeführt.
Meinem verehrten Lehrer, Herrn Prof. P. S. Chen, danke ich herzlich für Anregung und Leitung dieser Arbeit.
Rights and permissions
About this article
Cite this article
Spiro-Kern, A. Untersuchungen über die Proteasen beiCulex pipiens . J. Comp. Physiol. 90, 53–70 (1974). https://doi.org/10.1007/BF00698367
Received:
Issue Date:
DOI: https://doi.org/10.1007/BF00698367