Summary
The number and types of inclusions within bee retinula cells in the distal region of the ommatidium were investigated. Measurements were made in 416 histological sections of visual cells, representing five different conditions of adaptation, i.e. light adaptation to intensities of 1, 9000 and 54000 lux, total dark adaptation, and the transient state of adaptation to dark following light adaptation.
Four kinds of inclusions can be distinguished in the visual cells: multivesicular bodies (MVB) (Fig. 1a–c), lamellar bodies (Lb) (Fig. 1d), autophagic vacuoles (aut. V) (Fig. 2), and dense bodies (Db) (Fig. 3). Transitional forms combining two or even three characteristics of the types listed above point to close relationships (Fig. 4 and 5).
None of the types of inclusion found is in itself a criterion for any of the states of adaptation studied; it is necessary to consider all the inclusions and take account of the relative numbers of the various types.
The number of multivesicular bodies does not increase with the state of light adaptation (Table 1).
During transient dark adaptation, as the sensitivity of the receptor increases the number of dense bodies and autophagic vacuoles increases significantly in proportion to that of other inclusions.
It is the relative increase in the number of autophagic vacuoles that characterizes the rise in sensitivity of the visual cells; the increase of dense bodies is smaller than that of autophagic vacuoles, because the mean number of dense bodies is relatively high even during dark adaptation.
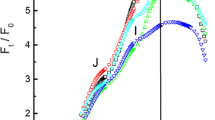
The transition from the light-adapted to the dark-adapted state (pigment migration and alteration of the perirhabdomeric system) after 1 1/2 hours of light adaptation at 54000 lux begins within about 10 min during subsequent dark adaptation. This means that the ultrastruetural alterations begin when the adaptation curve (Fig. 7), measured electrophysiclogically, rises only slightly.
Zusammenfassung
Art und Anzahl der Einschlüsse wurden in insgesamt 416 Schnitten von Retinulazellen der Biene im distalen Ommatidiumbereich während Helladaptation (HA) mit 1, 9000 und 54000 Lux, totaler Dunkeladaptation (DA) und Hell-Dunkel-Adaptation (HDA) registriert. Bei HDA wurde der Rezeptor noch während des Empfindlichkeitsanstiegs, d.h. in der Phase der DA, die auf HA folgt, geprüft. Vier Typen von Einschlußkörpern lassen sich in den Sehzellen unterscheiden: multivesikuläre Körper (MVB) (Abb. 1a–c), Lamellenkörper (Lb) (Abb. 1 d), autophage Vakuolen (aut. V) (Abb. 2) und Dichtekörper (Db) (Abb. 3). Zwischen diesen Einschlußkörpern besteht ein Zusammenhang. Übergangsformen können Merkmale von zwei oder sogar drei Binschlußtypen aufweisen (Abb. 4 und 5). Keiner der gefundenen Einschlußtypen stellt allein ein Kriterium für einen der genannten Adaptationszustände dar. Vielmehr muß stets das Zahlenverhältnis der Einschlußtypen und damit aller Einschlüsse berücksichtigt werden. Während der HA erfolgt auch mit steigender Belichtungsintensität keine Zunahme der Anzahl der MVB (Tabelle 1).
Während des Empfindlichkeitsanstiegs der Sehzellen (HDA) steigt die Zahl der Db und aut. V im Verhältnis zur Anzahl der anderen Einschlüsse signifikant an. — Dabei charakterisiert die relative Zunahme der aut. V den Empfindlichkeitsanstieg der Sehzellen; die Zunahme der Db ist in Relation zu der der aut. V geringer, weil der Mittelwert der Anzahl der Db schon bei DA verhältnismäßig hoch liegt und nicht wesentlich bei Empfindlichkeitsanstieg zunimmt.
Der Übergang von HA- in DA-Stellung (Pigmentwanderung und Veränderung des perirhabdomeren Systems) beginnt nach 1 1/2stündiger HA mit 54000 Lux in etwa 10 min der nachfolgenden DA. Das bedeutet, daß diese feinstrukturellen Veränderungen einsetzen, wenn die elektrophysiologisch gewonnene Adaptationskurve (Abb. 7) nur noch schwach ansteigt.
Similar content being viewed by others
Literatur
Autrum, H., Kolb, G.: The dark adaptation in single visual cells of the compound eye ofAeschna cyanea. J. comp. Physiol.79, 213–232 (1972)
Biberfeld, P.: Endocytosis and lysosome formation in blood lymphocytes transformed by phytohemagglutinin. J. Ultrastruct. Res.37, 41–68 (1971)
Brammer, J. D., White, R. H.: Vitamin A deficiency: effect on mosquito eye ultrastructure. Science163, 821–823 (1969)
Burton, P. R., Stockhammer, K. A.: Electron microscopic studies of the compound eye of the toadbug,Gelastocoris oculatus. J. Morph.127, 233–258 (1969)
Eguchi, E., Waterman, T. H.: Changes in retinal fine structure induced in the crabLibinia by light and dark adaptation. Z. Zellforsch.79, 209–229 (1967)
Esch, H.: Über die Körpertemperaturen und den Wärmehaushalt vonApis mellifica. Z. vergl. Physiol.43, 305–335 (1960)
Fahrenbach, W. H.: The morphology of the eye ofLimulus. II. Ommatidia of the compound eye. Z. Zellforsch.93, 451–483 (1969)
Fahrenbach, W. H.: The morphology of theLimulus visual system. III. The lateral rudimentary eye. Z. Zellforsch.105, 303–316 (1970)
Hamdorf, K., Kaschef, A. H.: Adaptation beim Fliegenauge. Z. vergl. Physiol.51, 67–95 (1965)
Kabuta, H., Tominaga, Y., Kuwabara, M.: The rhabdomeric microvilli of several arthropod compound eyes kept in darkness. Z. Zellforsch.85, 78–88 (1968)
Kolb, G., Autrum, H.: Die Feinstruktur im Auge der Biene bei Hell- und Dunkeladaptation. J. comp. Physiol.77, 113–125 (1972)
Melamed, J., Trujillo-Cenóz, O.: The fine structure of the visual system ofLycosa (Araneae: Lycosidae). Part I: Retina and optic nerve. Z. Zellforsch.74, 12–31 (1966)
Menzel, R.: Feinstruktur des Komplexauges der Roten Waldameise,Formica polyctena (Hymenoptera, Formicidae). Z. Zellforsch.127, 356–373 (1972)
Neese, V.: Die Altersabhängigkeit des Ommochromgehalts im Komplexauge der Bienen. Ein quantitativer Vergleich zwischen Wildtyp und der Augenmutante Chartreuse. J. Insect Physiol.18, 229–236 (1972)
Novikoff, A.B., Holtzman, E.: In: Cells and organelles, 129–135 Rioehart & Winston, Inc. 1970
Perrelet, A., Orci, L., Baumann, F.: Evidence for granulolysis in the retinula cells of a stomatopod crustacean,Squilla mantis. J. Cell Biol.48, 684–688 (1971)
Quatacker, J. R.: Formation of autophagic vacuoles during human corpus luteum involution. Z. Zellforsch.122, 479–487 (1971)
Seibt, U.: Der Einfluß der Temperatur auf die Dunkeladaptation vonApis mellifica. Z. vergl. Physiol.67, 77–102 (1967)
Smith, R. E., Farquhar, M. G.: Lysosome functions in the regulation of the secretory process in cells of the anterior pituitary gland. J. Cell Biol.31, 319–346 (1966)
Trujillo-Cenóz, O.: Some aspects of the structural organization of the arthropod eye. In: Sensory receptors. Cold Spr. Harb. Symp. quant. Biol.30, 371–382 (1965)
Tuurala, O., Lehtinen, A.: Über die Wandlungen in der Feinstruktur der Lichtsinneszellen bei der Hell- und Dunkeladaptation im Auge einer Asselart,Oniscus asellus L. Ann. Acad. Sci. fenni. A, IV. Biol.123, 3–8 (1967)
Varela, F. G., Porter, K. R.: Fine structure of the visual system of the honey bee (Apis mellifica). J. Ultrastruct. Res.29, 236–259 (1969)
Wachmann, E.: Multivesikuläre und andere Einschlußkörper in den Retinulazellen der SumpfgrillePteronemobius heydeni (Fischer). Z. Zellforsch.99, 263–276 (1969)
White, R. H.: The effect of light deprivation upon the ultrastructure of the larval mosquito eye. II. The rhabdom. J. exp. Zool.166, 405–426 (1967)
Author information
Authors and Affiliations
Additional information
Mit Unterstützung durch die Deutsche Forschungsgemeinschaft.
Herrn Prof. Dr. Dr. h. c. H. Autrum danke ich für anregende Diskussionen und kritische Durchsicht des Manuskripts, Herrn Dr. Smola für Ratschläge bei der statistischen Auswertung, Fräulein Hubalek für technische Mitarbeit in der Elektronenmikroskopie und Frau Lorenz bei der Durchführung der elektrophysiologischen Versuche. Den Herren Prof. Dr. Renner und Dr. Heinzeller danke ich für die Überlassung der Bienen auch während der Wintermonate.
Rights and permissions
About this article
Cite this article
Kolb, G. Einschlüsse in Retinulazellen der Biene während der Adaptation. J. Comp. Physiol. 91, 167–186 (1974). https://doi.org/10.1007/BF00694272
Received:
Issue Date:
DOI: https://doi.org/10.1007/BF00694272