Background:
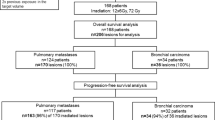
In the European Intergroup Cooperative Ewing's Sarcoma Study (EICESS) 92, whole lung irradiation (WLI) was performed in patients with primary lung metastases. This retrospective analysis evaluates the pulmonary function and the outcome of patients with exclusively pulmonary metastases.
Patients and Methods:
Between 1990 and 1999, 99 patients were registered into the EICESS-92-study trial with exclusively pulmonary metastases of Ewing tumors. The multimodal treatment regimen included polychemotherapy and local therapy to the primary tumor. WLI was performed with a dose between 12–21 Gy. 70 patients were treated with WLI, 13 of them received a further boost to their primary tumor in the thorax up to a cumulative dose of 54 Gy.
Results:
Pulmonary function tests were available for 37 patients treated with WLI (± boost). None, mild, moderate or severe pulmonary complications were seen in 43%, 29%, 21% and 7% of patients treated with WLI without further boost (median follow-up 25.2 months). Patients with an additional radiation boost or surgery to the thorax showed slightly higher rates of complications. Overall survival (OAS) showed a trend towards better results for patients with WLI (5-year-OAS: 0.61 for WLI vs. 0.49 for no WLI, p = 0.36).
Conclusion:
These data indicate a benefit and acceptable toxicity for WLI in the presented collective of patients. As long as there is no randomized prospective analysis, the present data confirm the indication for WLI in Ewing tumor patients with primary exclusively lung metastases.
Hintergrund:
In der European Intergroup Cooperative Ewing's Sarcoma Study (EICESS) 92 wurde bei Patienten mit primären Lungenmetastasen eine Ganzlungenbestrahlung durchgeführt. Für diese retrospektive Analyse wurden Lungenfunktion und Behandlungsergebnisse von Patienten mit ausschließlich pulmonaler Metastasierung analysiert.
Patienten und Methodik:
Von 1990 bis 1999 wurden 99 Patienten mit primären Lungenmetastasen ohne weitere Metastasierung von Ewing-Tumoren in der EICESS-92-Studie registriert. Das multimodale Therapieregime beinhaltete Polychemotherapie und Lokaltherapie für den Primarius. Die Ganzlungenbestrahlung wurde mit Dosen von 12 bis 21 Gy durchgeführt. 70 Patienten erhielten eine Ganzlungenbestrahlung, 13 davon mit einem weiteren Boost auf den Primarius im Thorax bis maximal kumulativ 54 Gy.
Ergebnisse:
Lungenfunktionsanalysen waren bei 37 Patienten mit Ganzlungenbestrahlung (± Boost) zu erheben. Keine, milde, moderate oder schwere pulmonale Einschränkungen waren in 43%, 29%, 21% und 7% der Patienten mit alleiniger Ganzlungenbestrahlung zu erheben (mediane Nachbeobachtungszeit 25,2 Monate) (Tabellen 2 und 3: Vergleich der Patientencharakteristika von Patienten mit/ohne Funktionseinschränkungen (Tabelle 2) bzw. mit/ohne Lungenfunktionsprüfung im Verlauf (Tabelle 3). Patienten mit einem zusätzlichen Boost oder einer Operation am Thorax (Tabelle 1) zeigten etwas höhere Komplikationsraten. Im Trend zeigte das Gesamtüberleben für die Patienten, die eine Ganzlungenbestrahlung erhalten hatten, bessere Ergebnisse (Abbildung 1: Gesamtüberleben bei Patienten mit und ohne Ganzlungenbestrahlung; 5-Jahres-Gesamtüberleben: 0,61 für Ganzlungenbestrahlung vs. 0,49 für Nicht-Ganzlungenbestrahlung, p = 0,36).
Schlussfolgerung:
Diese Daten weisen auf einen Vorteil und eine akzeptable Toxizität bei Ganzlungenbestrahlung im präsentierten Kollektiv hin. Solange keine Ergebnisse von prospektiven randomisierten Studien vorliegen, unterstützen die hier gezeigten Daten die Indikation zur Ganzlungenbestrahlung bei Patienten mit solitären primären Lungenmetastasen eines Ewing-Tumors.
Similar content being viewed by others
Author information
Authors and Affiliations
Corresponding author
Rights and permissions
About this article
Cite this article
Bölling, T., Schuck, A., Paulussen, M. et al. Whole Lung Irradiation in Patients with Exclusively Pulmonary Metastases of Ewing Tumors. Strahlenther Onkol 184, 193–197 (2008). https://doi.org/10.1007/s00066-008-1810-x
Received:
Accepted:
Issue Date:
DOI: https://doi.org/10.1007/s00066-008-1810-x