Abstract
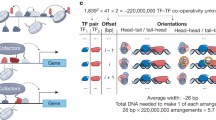
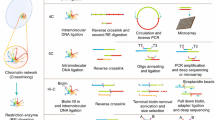
Transcription factories are dynamic structures located in the cell nucleus, which bring multiple genes and genomic control elements into proximity. Our research group explores these factories as inspiration for the design of high-performance DNA-based computer hardware. Potential applications range from innovative cell-based cancer therapy to advanced metabolic monitoring systems.
Article PDF
Similar content being viewed by others
Avoid common mistakes on your manuscript.
Literatur
Iborra FJ, Pombo A, Jackson DA, Cook PR (1996) Active RNA polymerases are localized within discrete transcription “factories” in human nuclei. J Cell Sci 109:1427–1436
Eskiw CH, Rapp A, Carter DRF, Cook PR (2008) RNA polymerase II activity is located on the surface of protein-rich transcription factories. J Cell Sci 121: 1999–2007
Cook PR (1999) The Organization of Replication and Transcription. Science 284: 1790–1795
Shin Y, Brangwynne CP (2017) Liquid phase condensation in cell physiology and disease. Science 357: eaaf4382
Cho WK, Spille JH, Hecht M et al. (2018) Mediator and RNA polymerase II clusters associate in transcription-dependent condensates. Science 361: 412–415
Lu H, Yu D, Hansen AS et al. (2018) Phase-separation mechanism for C-terminal hyperphosphorylation of RNA polymerase II. Nature 558: 318–323
Cho W K, Jayanth N, English BP et al. (2016) RNA Polymerase II cluster dynamics predict mRNA output in living cells. Elife 5: e13617
Morin JA, Wittmann S, Choubey S et al. (2022) Sequence-dependent surface condensation of a pioneer transcription factor on DNA. Nat Phys 18: 271–276
Pancholi A, Klingberg T, Zhang W et al. (2021) RNA polymerase II clusters form in line with surface condensation on regulatory chromatin. Mol Syst Biol 17: e10272
Kempfer R, Pombo A (2020) Methods for mapping 3D chromosome architecture. Nat Rev Genet 21: 207–226
Espinola SM, Götz M, Bellec M et al. (2021) Cisregulatory chromatin loops arise before TADs and gene activation, and are independent of cell fate during early Drosophila development. Nat Genet 53: 477–486
Hajiabadi H, Mamontova I, Prizak R et al. (2022) Deep-learning microscopy image reconstruction with quality control reveals second-scale rearrangements in RNA polymerase II clusters. PNAS Nexus 1: pgac065
Guo YE, Manteiga JC, Henninger JE et al. (2019) Pol II phosphorylation regulates a switch between transcriptional and splicing condensates. Nature 572: 543–548
Li J, Hsu A, Hua Y et al. (2020) Single-gene imaging links genome topology, promoter–enhancer communication and transcription control. Nat Struct Mol Biol 27: 1032–1040
Henninger JE, Oksuz O, Shrinivas K et al. (2021) RNA-Mediated Feedback Control of Transcriptional Condensates. Cell 184: 207–225.e24
Ghavi-Helm Y, Klein FA, Pakozdi T et al. (2014) Enhancer loops appear stable during development and are associated with paused polymerases. Nature 512: 96–100
Winick-Ng W, Kukalev A, Harabula I et al. (2021) Celltype specialization in the brain is encoded by specific longrange chromatin topologies. Nature 599: 684–691
Liu Q, Wang L, Frutos AG et al. (2000) DNA computing on surfaces. Nature 403: 175–179
Tang W, Liu DR (2018) Rewritable multi-event analog recording in bacterial and mammalian cells. Science 8992: eaap8992
Yang Q, Yang F, Dai W et al. (2021) DNA Logic Circuits for Multiple Tumor Cells Identification Using Intracellular MicroRNA Molecular Bispecific Recognition. Adv Healthc Mater 10: 1–8
Sato Y, Sakamoto T, Takinoue M (2020) Sequence-based engineering of dynamic functions of micrometer-sized DNA droplets. Sci Adv 6: eaba3471
Tran MP, Chatterjee R, Dreher Y et al. (2023) A DNA Segregation Module for Synthetic Cells. Small 19: e2202711
Tschurikow X, Gadzekpo A, Tran MP et al. (2023) Amphiphiles formed from synthetic DNA-nanomotifs mimic the dispersal of transcriptional clusters in the cell nucleus. Nano Lett 23: 7815–7824
Tschurikow X (2022) Mimicking subcellular cluster formation via surface condensation with synthetic DNA nanomotifs and surface structures. Bachelorarbeit, Karlsruher Institut für Technologie.
Funding
Funding note: Open Access funding enabled and organized by Projekt DEAL.
Author information
Authors and Affiliations
Corresponding author
Additional information
Danksagung
Abstract wurde im Dialog mit ChatGPT 3.5 erzeugt und erste Autorenrohfassung des Texts wurde mittels ChatGPT 3.5 gekürzt. Dank an Michael Hambsch für Kommentare
Lennart Hilbert
2005–2014 Physikstudium, wissenschaftliche Arbeit und Promotion. 2005–2014 Physikstudium an der Universität Bremen, wissenschaftliche Arbeit und Promotion in der Physiologie, McGill University, Montreal, Kanada. 2014–2018 PostDoc am Max-Planckhstitut für Molekulare Zellbiologie und Genetik und am Max-Planck-Institut für Physik komplexer Systeme. Seit 2018 Tenure-Track-Professor für Systembiologie/Bioinformatik, Zoologisches Institut & Institut für Biologische und Chemische Systeme, Karlsruher Institut für Technologie (KIT).
Rights and permissions
Open Access: Dieser Artikel wird unter der Creative Commons Namensnennung 4.0 International Lizenz veröffentlicht, welche die Nutzung, Vervielfältigung, Bearbeitung, Verbreitung und Wiedergabe in jeglichem Medium und Format erlaubt, sofern Sie den/die ursprünglichen Autor(en) und die Quelle ordnungsgemäß nennen, einen Link zur Creative Commons Lizenz beifügen und angeben, ob Änderungen vorgenommen wurden. Die in diesem Artikel enthaltenen Bilder und sonstiges Drittmaterial unterliegen ebenfalls der genannten Creative Commons Lizenz, sofern sich aus der Abbildungslegende nichts anderes ergibt. Sofern das betreffende Material nicht unter der genannten Creative Commons Lizenz steht und die betreffende Handlung nicht nach gesetzlichen Vorschriften erlaubt ist, ist für die oben aufgeführten Weiterverwendungen des Materials die Einwilligung des jeweiligen Rechteinhabers einzuholen. Weitere Details zur Lizenz entnehmen Sie bitte der Lizenzinformation auf http://creativecommons.org/licenses/by/4.0/deed.de.
About this article
Cite this article
Hilbert, L. Der Zellkern als Vorbild für zukünftige DNA-Computerchips?. Biospektrum 30, 19–22 (2024). https://doi.org/10.1007/s12268-024-2090-4
Published:
Issue Date:
DOI: https://doi.org/10.1007/s12268-024-2090-4