Abstract
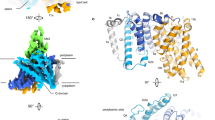
TRAP-transporters are widespread in bacteria and archaea and are often responsible for the transport of nutrients or virulence factors in pathogens. They consist of three domains, a substrate-binding protein and two membrane domains. Using cryo-EM, we have determined the structure of the membrane domains, revealing a monomeric elevator architecture. Further studies gave insights into the interaction between the domains of TRAP-transporters and how they can be specifically inhibited by using a VHH antibody.
Article PDF
Similar content being viewed by others
Avoid common mistakes on your manuscript.
Literatur
Forward JA, Behrendt MC, Wyborn NR et al. (1997) TRAP transporters: a new family of periplasmic solute transport systems encoded by the dctPQM genes of Rhodobacter capsulatus and by homologs in diverse gram-negative bacteria. J Bacteriol 179: 5482–5493
Müller A, Severi E, Mulligan C et al. (2006) Conservation of structure and mechanism in primary and secondary transporters exemplified by SiaP, a sialic acid binding virulence factor from Haemophilus influenzae. J Biol Chem 281: 22212–22222
Berntsson RPA, Smits SHJ, Schmitt L et al. (2010) A structural classification of substrate-binding proteins. FEBS Letters 584: 2606–2617
Peter MF, Ruland JA, Depping P et al. (2022) Structural and mechanistic analysis of a tripartite ATP-independent periplasmic TRAP transporter. Nat Commun 13: 4471
Mancusso R, Gregorio GG, Liu Q, Wang DN (2012) Structure and mechanism of a bacterial sodium-dependent dicarboxylate transporter. Nature 491: 622–626
Jumper J, Evans R, Pritzel A et al. (2021) Highly accurate protein structure prediction with AlphaFold. Nature 596: 583–589
Mulligan C, Fenollar-Ferrer C, Fitzgerald GA et al. (2016) The bacterial dicarboxylate transporter VcINDY uses a two-domain elevator-type mechanism. Nat Struct Mol Biol 23: 256–263
Funding
Open Access funding enabled and organized by Projekt DEAL.
Author information
Authors and Affiliations
Corresponding author
Additional information
Martin F. Peter, 2011–2016 Chemiestudium, Universität Bonn. 2021 Promotion mit Stipendium der Konrad-Adenauer-Stiftung bei PD Dr. G. Hagelueken, Universität Bonn. 2022 Postdoktorand bei Prof. Dr. C. Paulino, Membrane Enzymology, University of Groningen, Niederlande. Seit 2023 Postdoktorand bei Prof. Dr. C. Paulino, Universität Heidelberg.
Jan A. Ruland, 2011–2016 Chemiestudium, Universität Bonn. 2021 Promotion bei Prof. Dr. U. Kubitscheck, Universität Bonn. Seit 2021 Postdok bei Prof. Dr. U. Kubitscheck, Universität Bonn.
Gregor Hagelueken Bis 2004 Studium der Angewandten Naturwissenschaft, TU Freiberg. 2007 Promotion, HZI Braunschweig, Prof. Dr. D. Heinz, Prof. Dr. W.-D. Schubert. 2008–2012 Postdoc, Prof. Dr. J. Naismith, University of St Andrews, UK. 2012–2018 Habilitation in Biophysikalischer Chemie, Prof. Dr. O. Schiemann, Universität Bonn. Seit 2019 Gruppenleiter, Institut für Strukturbiologie der Universität Bonn.
Rights and permissions
Dieser Artikel wird unter der Creative Commons Namensnennung 4.0 International Lizenz veröffentlicht, welche die Nutzung, Vervielfältigung, Bearbeitung, Verbreitung und Wiedergabe in jeglichem Medium und Format erlaubt, sofern Sie den/die ursprünglichen Autor(en) und die Quelle ordnungsgemäß nennen, einen Link zur Creative Commons Lizenz beifügen und angeben, ob Änderungen vorgenommen wurden. Die in diesem Artikel enthaltenen Bilder und sonstiges Drittmaterial unterliegen ebenfalls der genannten Creative Commons Lizenz, sofern sich aus der Abbildungslegende nichts anderes ergibt. Sofern das betreffende Material nicht unter der genannten Creative Commons Lizenz steht und die betreffende Handlung nicht nach gesetzlichen Vorschriften erlaubt ist, ist für die oben aufgeführten Weiterverwendungen des Materials die Einwilligung des jeweiligen Rechteinhabers einzuholen. Weitere Details zur Lizenz entnehmen Sie bitte der Lizenzinformation auf http://creativecommons.org/licenses/by/4.0/deed.de.
About this article
Cite this article
Peter, M.F., Ruland, J.A. & Hagelueken, G. Wie sekundäre Transporter mit substratbindenden Proteinen interagieren. Biospektrum 29, 245–248 (2023). https://doi.org/10.1007/s12268-023-1934-7
Published:
Issue Date:
DOI: https://doi.org/10.1007/s12268-023-1934-7