Abstract
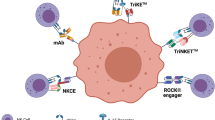
NK cells emerged as promising immune cells for cancer therapy. Beyond antibody-based approaches triggering NK cell activity via the FcγRIIIa, also multifunctional approaches are being exploited to redirect NK cell cytotoxicity against malignant cells. In this respect, immunoligands which are fusion proteins composed of an antibody-derived targeting arm and a natural ligand for an activating receptor on NK cells show great promise in inducing effector cell activation against tumor cells.
Article PDF
Similar content being viewed by others
Avoid common mistakes on your manuscript.
Literatur
Peipp M, Klausz K, Boje AS et al. (2022) Immunotherapeutic targeting of activating natural killer cell receptors and their ligands in cancer. Clin Exp Immunol, 209:22–32
Demaria O, Cornen S, Daëron M, Morel Y et al. (2019) Harnessing innate immunity in cancer therapy. Nature 574:45–56
Quatrini L, Della Chiesa M, Sivori S et al. (2021) Human NK cells, their receptors and function, Eur J Immunol 51:1566–1579
Schlecker E, Fiegler N, Arnold A et al. (2014) Metalloprotease-Mediated Tumor Cell Shedding of B7-H6, the Ligand of the Natural Killer Cell-Activating Receptor NKp30. Cancer Res 74:3429–3440
Demaria O, Gauthier L, Debroas G et al. (2021) Natural killer cell engagers in cancer immunotherapy: Next generation of immuno-oncology treatments. Eur. J. Immunol 51:1934–1942
Gauthier L, Vivier E (2020) Boosting Cytotoxic Antibodies against Cancer. Cell 180:822–824
Crinier A, Narni-Mancinelli E, Ugolini S et al. (2020) SnapShot: Natural Killer Cells. Cell 180:1280–1280
Kellner C, Gramatzki M, Peipp M (2013) Promoting natural killer cell functions by recombinant immunoligands mimicking an induced self phenotype. Oncoimmunology 2:e24481
von Strandmann EP, Hansen HP, Reiners KS et al. (2006) A novel bispecific protein (ULBP2-BB4) targeting the NKG2D receptor on natural killer (NK) cells and CD138 activates NK cells and has potent antitumor activity against human multiple myeloma in vitro and in vivo. Blood 107:1955–1962
Kellner C, Günther, A, Humpe A et al. (2016) Enhancing natural killer cell-mediated lysis of lymphoma cells by combining therapeutic antibodies with CD20-specific immunoligands engaging NKG2D or NKp30. Oncoimmunology 5:e1058459
Pekar L, Klausz K, Busch M et al. (2021) Affinity Maturation of B7-H6 Translates into Enhanced NK Cell-Mediated Tumor Cell Lysis and Improved Proinflammatory Cytokine Release of Bispecific Immunoligands via NKp30 Engagement. J Immunol 206:225–236
Funding
Funding note: Open Access funding enabled and organized by Projekt DEAL.
Author information
Authors and Affiliations
Corresponding authors
Additional information
Danksagung
Wir bedanken uns bei allen Kollegen und Kolleginnen, welche an der Generierung und am Engineering von bi- und multifunktionellen Molekülen für die Effektorzellrekrutierung beteiligt sind und waren: Britta Lipinski, Jasmin Zimmermann, Paul Arras, Simon Krah, Daniel Klewinghaus, Brian Rabinovich, Harald Kolmar, Han Byul Yoo, Tushar Gupta, Bernhard Valldorf, Sven Poetzsch, Rinat Zaynagetdinov, Yanping Xiao, Daniela Wesch, Hans-Heinrich Oberg, Steffen Krohn, Carina Lynn Gehlert, Britta von Below sowie Anja Muskulus und viele andere.
Ammelie Svea Boje, Katja Klausz, Lukas Pekar (oben), Christian Kellner, Stefan Zielonka und Matthias Peipp (unten, v. l. n. r.)
Die Abteilung von Matthias Peipp beschäftigt sich mit der Generierung und den Effektormechanismen optimierter Antikörper und Antikörperderivate zur Verbesserung der Immuntherapie von Autoimmun- und Tumorerkrankungen.
Die Arbeitsgruppe von Stefan Zielonka bei Merck Healthcare KGaA beschäftigt sich mit der Generierung und dem Engineering von mono- und multifunktionellen Antikörperderivaten für unterschiedliche Indikationen u.a. im Bereich der Immunonkologie.
Rights and permissions
Open Access: Dieser Artikel wird unter der Creative Commons Namensnennung 4.0 International Lizenz veröffentlicht, welche die Nutzung, Vervielfältigung, Bearbeitung, Verbreitung und Wiedergabe in jeglichem Medium und Format erlaubt, sofern Sie den/die ursprünglichen Autor(en) und die Quelle ordnungsgemäß nennen, einen Link zur Creative Commons Lizenz beifügen und angeben, ob Änderungen vorgenommen wurden. Die in diesem Artikel enthaltenen Bilder und sonstiges Drittmaterial unterliegen ebenfalls der genannten Creative Commons Lizenz, sofern sich aus der Abbildungslegende nichts anderes ergibt. Sofern das betreffende Material nicht unter der genannten Creative Commons Lizenz steht und die betreffende Handlung nicht nach gesetzlichen Vorschriften erlaubt ist, ist für die oben aufgeführten Weiterverwendungen des Materials die Einwilligung des jeweiligen Rechteinhabers einzuholen. Weitere Details zur Lizenz entnehmen Sie bitte der Lizenzinformation auf http://creativecommons.org/licenses/by/4.0/deed.de.
About this article
Cite this article
Boje, A.S., Klausz, K., Pekar, L. et al. Rekrutierung von Natürlichen Killerzellen durch optimierte Immunliganden. Biospektrum 28, 601–604 (2022). https://doi.org/10.1007/s12268-022-1836-0
Published:
Issue Date:
DOI: https://doi.org/10.1007/s12268-022-1836-0