Abstract
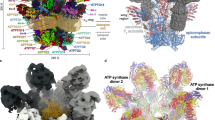
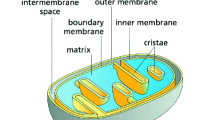
Mitochondrial energy conversion depends on an intricately folded membrane structure, generated by oligomerisation of ATP synthase dimers. However, morphology of cristae membranes varies greatly between different organisms. Recent studies have revealed the unique ATP synthase assemblies of the causative agents of toxoplasmosis and sleeping sickness, giving insight into the role of parasite-specific sub-units in complex assembly, mitochondrial function and parasite fitness.
Article PDF
Similar content being viewed by others
Avoid common mistakes on your manuscript.
Literatur
Kühlbrandt W (2019) Structure and mechanisms of F-type ATP synthases. Annu Rev Biochem 88:515–549
Sheffield HG, Melton ML (1968) The fine structure and reproduction of Toxoplasma gondii. J Parasitol 54: 209–226
Mühleip AW, Dewar CE, Schnaufer A et al. (2017) In situ structure of trypanosomal ATP synthase dimer reveals a unique arrangement of catalytic subunits. Proc Natl Acad Sci USA 114:992997
Zikova A, Schnaufer A, Dalley RA et al. (2009) The F0F1-ATP synthase complex contains novel subunits and is essential for procyclic Trypanosoma brucei. PLoS Pathog 5: e1000436
Huet D, Rajendran E, van Dooren GG, Lourido S (2018) Identification of cryptic subunits from an apicomplexan ATP synthase. eLife 7:e38097
Mühleip A, Kock Flygaard R, Ovciarikova J et al. (2021) ATP synthase hexamer assemblies shape cristae of Toxoplasma mitochondria. Nat Commun 12:120
Gahura O, Mühleip A, Hierro-Yap C et al. (2022) An ancestral interaction module promotes oligomerization in divergent mitochondrial ATP synthases. bioRxiv, DOI: https://doi.org/10.1101/2021.10.10.463820
Guo H, Bueler SA, Rubinstein JL (2017) Atomic model for the dimeric FO region of mitochondrial ATP synthase. Science 358:936–940
Gu J, Zhang L, Zong S et al. (2019) Cryo-EM structure of the mammalian ATP synthase tetramer bound with inhibitory protein IF1. Science 364:1068–1075
Watt IN, Montgomery MG, Runswick MJ et al. (2010) Bioenergetic cost of making an adenosine triphosphate molecule in animal mitochondria. Proc Natl Acad Sci USA 107:16823–16827
Wolf DM, Segawa M, Kondadi AK et al. (2019) Individual cristae within the same mitochondrion display different membrane potentials and are functionally independent. EMBO J: e101056
Funding
Funding note: Open Access funding enabled and organized by Stockholm University.
Author information
Authors and Affiliations
Corresponding author
Additional information
Danksagung
Ich danke dem Personal der schwedischen Kryo-EM Infrastruktur-Plattform am SciLifeLab für die Unterstützung bei der Datenaufnahme.
Alexander Mühleip 2007–2012 Studium der Biochemie an der Goethe-Universität Frankfurt a. M. Danach bis 2017 Promotion am Max-Planck-Institut für Biophysik, Frankfurt a. M. Seitdem Postdoktorand in der Abteilung für Biochemie und Biophysik der Universität Stockholm, Schweden.
Rights and permissions
Open Access: Dieser Artikel wird unter der Creative Commons Namensnennung 4.0 International Lizenz veröffentlicht, welche die Nutzung, Vervielfältigung, Bearbeitung, Verbreitung und Wiedergabe in jeglichem Medium und Format erlaubt, sofern Sie den/die ursprünglichen Autor(en) und die Quelle ordnungsgemäß nennen, einen Link zur Creative Commons Lizenz beifügen und angeben, ob Änderungen vorgenommen wurden. Die in diesem Artikel enthaltenen Bilder und sonstiges Drittmaterial unterliegen ebenfalls der genannten Creative Commons Lizenz, sofern sich aus der Abbildungslegende nichts anderes ergibt. Sofern das betreffende Material nicht unter der genannten Creative Commons Lizenz steht und die betreffende Handlung nicht nach gesetzlichen Vorschriften erlaubt ist, ist für die oben aufgeführten Weiterverwendungen des Materials die Einwilligung des jeweiligen Rechteinhabers einzuholen. Weitere Details zur Lizenz entnehmen Sie bitte der Lizenzinformation auf http://creativecommons.org/licenses/by/4.0/deed.de.
About this article
Cite this article
Mühleip, A. Mechanismen der Cristae-Biogenese in Humanparasiten. Biospektrum 28, 590–593 (2022). https://doi.org/10.1007/s12268-022-1831-5
Published:
Issue Date:
DOI: https://doi.org/10.1007/s12268-022-1831-5