Abstract
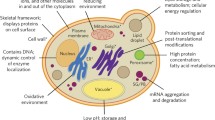
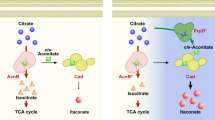
Microbial production of chemicals is a sustainable alternative to conventional industrial processes. However, the implementation of exogenous metabolic pathways is hampered by slow diffusion rates, competing pathways, or secretion of intermediates. Pre-existing organelles have been harnessed to overcome these problems, but these approaches suffer from interference with endogenous pathways. We have developed a new concept for the compartmentalization of enzymatic pathways in ER-derived vesicles.
Article PDF
Similar content being viewed by others
Avoid common mistakes on your manuscript.
Literatur
Borodina I, Nielsen J (2014) Advances in metabolic engineering of yeast Saccharomyces cerevisiae for production of chemicals. Biotechnol J 5: 609–620
Avalos JL, Fink GR, Stephanopoulos G (2013) Compartmentalization of metabolic pathways in yeast mitochondria improves production of branched chain alcohols. Nat Biotechnol 31: 335–341
Grewal PS, Samson JA, Baker JJ et al. (2021) Peroxisome compartmentalization of a toxic enzyme improves alkaloid production. Nat Chem Biol 17: 96–103
Kulagina N, Besseau S, Papon N et al. (2021) Peroxisomes: a new hub for metabolic engineering in yeast. Front Bioeng Biotechnol 9: 659431
Llop-Tous I, Madurga S, Giralt E et al. (2010) Relevant elements of a maize gamma-zein domain involved in protein body biogenesis. J Biol Chem 285: 35633–35644
Llop-Tous I, Ortiz M, Torrent M et al. (2011) The expression of a xylanase targeted to ER-protein bodies provides a simple strategy to produce active insoluble enzyme polymers in tobacco plants. PLoS One 6: e19474
Reifenrath M, Oreb M, Boles E et al. (2020) Artificial ER-derived vesicles as synthetic organelles for in vivo compartmentalization of biochemical pathways. ACS Synth Biol 9: 2909–2916
Bruckner C, Oreb M, Kunze G et al. (2018) An expanded enzyme toolbox for production of cis, cis-muconic acid and other shikimate pathway derivatives in Saccharomyces cerevisiae. FEMS Yeast Res 2: foy017
Funding
Funding note: Open Access funding enabled and organized by Projekt DEAL.
Author information
Authors and Affiliations
Corresponding author
Additional information
Danksagung
Die Autoren danken dem Bundesministerium für Bildung und Forschung (FKZ: 031A542 und 031B0218) für die finanzielle Unterstützung ihrer Arbeiten zur künstlichen Kompartimentierung.
Joanna Tripp, Mislav Oreb und Eckhard Boles (v. l. n. r.) arbeiten am Institut für Molekulare Biowissenschaften der Universität Frankfurt a. M. am Metabolic Engineering von Bäckerhefe und an neuen Ansätzen zur Kompartimentierung biotechnologisch interessanter Stoffwechselwege.
Rights and permissions
Open Access: Dieser Artikel wird unter der Creative Commons Namensnennung 4.0 International Lizenz veröffentlicht, welche die Nutzung, Vervielfältigung, Bearbeitung, Verbreitung und Wiedergabe in jeglichem Medium und Format erlaubt, sofern Sie den/die ursprünglichen Autor(en) und die Quelle ordnungsgemäß nennen, einen Link zur Creative Commons Lizenz beifügen und angeben, ob Änderungen vorgenommen wurden. Die in diesem Artikel enthaltenen Bilder und sonstiges Drittmaterial unterliegen ebenfalls der genannten Creative Commons Lizenz, sofern sich aus der Abbildungslegende nichts anderes ergibt. Sofern das betreffende Material nicht unter der genannten Creative Commons Lizenz steht und die betreffende Handlung nicht nach gesetzlichen Vorschriften erlaubt ist, ist für die oben aufgeführten Weiterverwendungen des Materials die Einwilligung des jeweiligen Rechteinhabers einzuholen. Weitere Details zur Lizenz entnehmen Sie bitte der Lizenzinformation auf http://creativecommons.org/licenses/by/4.0/deed.de.
About this article
Cite this article
Tripp, J., Oreb, M. & Boles, E. Neuartige, metabolisch aktive Organellen in eukaryotischen Zellen. Biospektrum 28, 397–399 (2022). https://doi.org/10.1007/s12268-022-1777-7
Published:
Issue Date:
DOI: https://doi.org/10.1007/s12268-022-1777-7