Summary
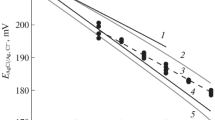
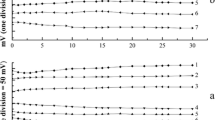
Coulometric titrations of small amounts of chloride with electrogenerated silver ions in mixed aqueous solvents containing 50 and 90% of ethanol, acetone or acetic acid have been compared. The end-points were detected with zero-current potentiometry, potentiometry with indicator electrode polarized to the end-point potential, potentiometry with two polarized electrodes and amperometry with two polarized electrodes. Best results were obtained in 90% ethanol medium by zero-current potentiometry. At the level of 0.18μg of chloride (in 50 ml) the error was approximately 10%. Although the solubility products indicating that the solubility is lowest in 90% acetic acid and 90% acetone media, the response in these media is too slow for practical purposes.
Zusammenfassung
Die coulometrische Titration kleiner Mengen Chlorid mit galvanisch gebildeten Silberionen in gemischt-wäßrigen Lösungsmitteln mit 50 bzw. 90% Ethanol, Aceton oder Essigsäure wurde verglichen. Der jeweilige Endpunkt wurde mit Null-Strom-Potentiometrie, potentiometrisch mit einer polarisierten Indikator-Elektrode, potentiometrisch mit zwei polarisierten Elektroden bzw. amperometrisch mit zwei polarisierten Elektroden bestimmt. Die besten Ergebnisse wurden in 90% ethanolischem Medium mit Null-Strom-Potentiometrie erhalten Bei der Bestimmung von 0,18μg Chlorid in 50 ml betrug der Fehler etwa 10% Wiewohl die Löslichkeitsprodukte in 90%iger Essigsäure bzw. 90%igem Aceton am kleinsten sind, verläuft die Endpunkteinstellung in diesen Medien für praktische Zwecke zu langsam.
Similar content being viewed by others
References
E. Bishop and R. G. Dhaneshwar, Analyt. Chemistry36, 726 (1964).
E. Jacobsen and G. Tandberg, Analyt. Chim. Acta64, 280 (1973).
W. Selig, Microchem. J.20, 388 (1975).
J. S. Hetman, Bull, centre rech. Pau3, 193 (1969).
A. Cedergren and G. Johansson, Talanta18, 917 (1971).
J. S. Hetman, Bull, centre rech. Pau7, 83 (1973).
D. E. Oh and F. A. Gunther, Bull. Environment. Contam. Toxic.12, 161 (1974).
W. J. Van Oort, G. Veenendael, and E. Buijsman, Analyt Chemistry2, 284 (1977)
W D. Cooke, C. N. Reilley, and N. H. Furman, Analyt. Chemistry23, 1662 (1951).
J. Tencheva, G. Velinov, and O. Budevsky, J. Electroanal. Chem.68, 65 (1976).
P. Zikolov, A. Astrug, and O. Budevsky, Talanta22, 511 (1975).
Author information
Authors and Affiliations
Rights and permissions
About this article
Cite this article
Hulanicki, A., Jędral, W., Piotrowska, J. et al. Coulometric titration of small amounts of chloride. Mikrochim Acta 77, 203–212 (1982). https://doi.org/10.1007/BF01237808
Received:
Issue Date:
DOI: https://doi.org/10.1007/BF01237808