Abstract
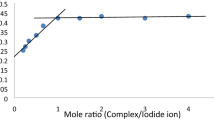
The kinetics of oxidation of quinol by mercuric nitrate in presence ofAcOH-H2O-HNO3 mixture has been investigated in order to find the active species of mercuric nitrate involved in the oxidation in this medium. The order of reaction both with respect to quinol and Hg(II) is found to be one. The reaction rate slightly increases with the increase in [HNO3] and the decrease of the dielectric constant of the medium. The reaction rate retards on addition of KNO3. There is no evidence for complex formation between quinol and Hg(II). These results suggest that HgNO 3+ might be the active species in this medium. A probable mechanism involving a two electron transfer in the rate determining step has been suggested. The producedp-benzoquinone does not exist in free state but forms a stable (1 : 1) complex with mercuric nitrate which has been characterized by TLC and IR studies.
Zusammenfassung
Es wurde die Kinetik der Oxidation von Chinol mit Quecksilbernitrat in Gegenwart einer Mischung ausAcOH-H2O-HNO3 untersucht, um die aktive Species bei der Oxidation in diesem Medium aufzuklären. Die Reaktionsordnung ist sowohl bezüglich des Chinols als auch des Hg(II)-Ions erster Ordnung. Die Reaktionsgeschwindigkeit erhöht sich leicht mit der HNO3-Konzentration und auch mit abfallender Dielektrizitätskonstante des Mediums. Die Reaktionsgeschwindigkeit sinkt mit dem Zusatz von KNO3. Es ist keinerlei Hinweis auf eine Komplexbildung zwischen Chinol und Hg(II) festzustellen. Die Resultate der Untersuchungen legen HgNO 3+ als aktive Spezies nahe. Es wird ein möglicher Mechanismus mit einem Zweielektronen-Transfer im geschwindigkeitsbestimmenden Schritt vorgeschlagen. Das dabei produziertep-Benzochinon existiert nicht in freier Form, sondern es bildet einen stabilen 1 : 1-Komplex mit Quecksilbernitrat; dieser Komplex wurde mittels TLC und IR charakterisiert.
Similar content being viewed by others
References
Sidwick N. V., The Chemical Elements and their Compounds, 296. Oxford University Press. 1950.
Zappi E. V., Manini A., Anales asoc. quim. argentina26, 89 (1938).
Topham A. R.,White A. G., J. Chem. Soc.1952, 105.
Halpern J., Taylor S. M., Discussion Faraday Soc.29, 174 (1960).
Littler J. S., J. Chem. Soc. London1962, 827.
Miano R. R., Plane R. A., Inorg. Chem.3, 987 (1964).
Patai S.,Shenfeld I., J. Chem. Soc. (B)1966, 366.
Fielding B. C.,Robberts H. L., J. Chem. Soc.1966, 1627.
Surender Rao V., Sethuram B., Navaneeth Rao T., Indian J. Chem.13, 1291 (1975).
Gupta K. C., Sharma Anita K., Indian J. Chem.20 A, 88 (1981).
Gupta K. C., Sharma Anita K., Misra V. D., Tetrahedron37, 2887 (1981).
Ayres G. H., Quantitative Chemical Analysis, 318. New York-Evanston-London: Harper & Row, and Tokyo: John Weatherhill, Inc. 1964.
Ouellette R. J., Robbins R. D., South A., jr., J. Amer. Chem. Soc.90, 1619 (1968).
Hinshelwood, J. Chem. Soc.1919, 1180.
Srinivasan V. S., Venkatasubramanian N., Indian J. Chem.8, 57 (1970).
Bailar J. C.,jr.,Emeléus H. J.,Nyholm Sir Ronald,Trotman-Dickenson A. F., Comprehensive Inorganic Chemistry, Vol. 3, 279, 316. Pergamon Press. 1973.
Amis E. S., Solvent Effects on Reaction Rates and Mechanisms, 34. London: Academic Press. 1966.
Grdenić D., Quart. Revs. (London)19, 318 (1965).
McKillop A., Swann B. P., Taylor E. C., Tetrahedron26, 4031 (1970).
Moeller T., Inorganic Chemistry, 300, 853. New York: J. Wiley. 1952.
Bartlett J. N., Curitis G. W., Anal. Chem.34, 80 (1962).
Stahl E., Thin Layer Chromatography, 494. London: Academic Press. 1965.
Addison C. C., Logan N., Quart. Chem. Rev.25, 289 (1971).
Brill T. B., Hugus Z. Z., jr., Inorg. Chem.9, 984 (1970).
Author information
Authors and Affiliations
Rights and permissions
About this article
Cite this article
Gupta, K.C., Misra, V.D. & Gupta, K. Kinetics and mechanism of oxidation of quinol by mercuric nitrate inAcOH-H2O-HNO3 medium. Monatsh Chem 115, 405–414 (1984). https://doi.org/10.1007/BF00810000
Received:
Revised:
Accepted:
Issue Date:
DOI: https://doi.org/10.1007/BF00810000