Summary
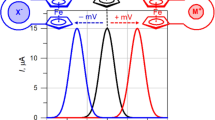
The UV/Vis spectra of the conjugated bases (NH deprotonation) of biliverdin IX α (BV), mesobiliverdin IX α (MBV), biliverdin IX α dimethyl ester (BV -DME) and mesobiliverdin IX α dimethyl ester (MBV - DME) are shown. They resemble those obtained for the reaction products of these biliverdins with superoxide anion (\(o_2^{\underset{\raise0.3em\hbox{$\smash{\scriptscriptstyle\cdot}$}}{ - } } \)). These results confirm that the bile pigments react with\(o_2^{\underset{\raise0.3em\hbox{$\smash{\scriptscriptstyle\cdot}$}}{ - } } \) giving the lactam NH deprotonated conjugated bases and inducing\(o_2^{\underset{\raise0.3em\hbox{$\smash{\scriptscriptstyle\cdot}$}}{ - } } \) dismutation. The spectrometric titrations ofBV, MBV and their dimehyl esters show that the lactam NH of the vinyl substituted biliverdins is more acidic (ΔpK a ℞0.5). The spectra of the lactam NH bisdeprotonated conjugated bases of the bilatrienes-abc studied (BV 4− andMBV 4−) can be obtained inDMSO/H2O/OH− systems of high basicity function (H−℞23).
Because of the low oxidation potentials ofBV 3− and of the corresponding trianion of bilirubin IX α (studied by voltammetry) an alternative metabolic degradative pathway is suggested for bilirubin, involving the interaction in lipophilic media with\(o_2^{\underset{\raise0.3em\hbox{$\smash{\scriptscriptstyle\cdot}$}}{ - } } \) and oxidation of the conjugated base generated by NH deprotonation.
Zusammenfassung
Es wurden die UV/Vis-Spektren der konjugierten Basen (NH-Deprotonierung) von Biliverdin IX α (BV), Mesobiliverdin IX α (MBV), Biliverdin-IX α-dimethylester (BV - DME) und Mesobiliverdin-IX α-dimethylester (MBV - DME) bestimmt. Sie ähneln denen der Reaktionsprodukte, die man bei der Umsetzung dieser Biliverdinverbindungen mit Superoxydanion (\(o_2^{\underset{\raise0.3em\hbox{$\smash{\scriptscriptstyle\cdot}$}}{ - } } \)) erhält. Damit wird bewiesen, daß die Reaktion über eine N-Deprotonierung der Lactamgruppe verläuft, an die sich eine\(o_2^{\underset{\raise0.3em\hbox{$\smash{\scriptscriptstyle\cdot}$}}{ - } } \)-Dismutation anschließt. Die spektrometrische Titration vonBV, MBV und ihrer Dimethylester zeigt, daß der Lactamstickstoff in den vinylsubstituierten Biliverdinderivaten eine höhere Azidität aufweist (ΔpK a ℞0.5). Die Spektren der bis-deprotonierten konjugierten Basen der Bilatriene-abc (BV 4− undMBV 4−) wurden inDMSO/H2O/OH−-Systemen (H−℞23) erhalten.
Unter Berücksichtigung der geringen Redoxpotentiale vonBV 3− und des entsprechenden Trianions von Bilirubin IX α (voltammetrische Bestimmung) wird ein neuer metabolischer Abbau für Bilirubin IX α vorgeschlagen: primäre Deprotonierung in lipophilem Medium mit\(o_2^{\underset{\raise0.3em\hbox{$\smash{\scriptscriptstyle\cdot}$}}{ - } } \) und nachfolgender Oxydation.
Similar content being viewed by others
References
Part XII: Claret J., Farrera J. A., Ribó J. M. (1990) Tetrahedron46: 1039
Ribó J. M., Farrera J. A., Claret J. (1989) Experientia46: 63
Sawyer D. T., Valentine J. S. (1981) Acc. Chem. Res.14: 393
Galliani G., Monti D., Speranza G., Manitto P. (1984) Tetrahedron Lett.25: 6037
Galliani G., Monti D., Speranza G., Manitto P. (1985) Experientia41: 1559
Land E. J., Sloper R. W., Truscott T. G. (1983) Radiat. Res.96: 450
Bowden K. (1966) Chem. Rev.66: 119
Cox R. A., Steward R. (1976) J. Am. Chem. Soc.98: 488
Reichardt Ch. (1988) In: Solvents and Solvents Effects in Organic Chemistry. Verlag Chemie, Weinheim
McDonagh A. F. (1979) In: Dolphin D. (ed.) The Porphyrins, Vol. 6, part A. Academic Press, New York, pp. 389–391
Falk H., Zruneck U. (1983) Monatsh. Chem.114: 1107
Scheer H. (1976) Z. Naturforsch.31 c: 413
Scheer H., Linsenmeier U., Krauss C. (1977) Z. Physiol. Chem.358: 185
Lightner D. A., Trull F. R. (1983) Spectroscopy Lett.16: 785
Burke M. J., Pratt D. C., Moscowitz A. (1972) Biochem.11: 4025
Wagniere G., Blauer G. (1976) J. Am. Chem. Soc.98: 7806
Falk H., Leodolter A. (1978) Monatsh. Chem.109: 883
Van Norman J. D., Szentirmay R. (1974) Anal. Chem.46: 1456
Petryka Z. J., Howe R. B. (1979) In: Dolphin D. (ed.) The Porphyrins, Vol. 6, part A. Academic Press, New York, pp. 805–837
Cardenas-Vazquez R., Yokosura O., Billing B. H. (1986) Biochem. J.236: 625
Yokosuka O., Billing B.H. (1987) Biochim. Biophys. Acta923: 268
de Matteis F., Trenti T., Gibbs A. H., Greig J. B. (1989) Mol. Pharmacol.35, 831
Kapitulnik J., Hardwick J. P., Ostrow J. D. (1987) Biochem. J.242: 297
McDonagh A. F., Palma L. A. (1980) Biochem. J.189: 193
Landen D. G., Park Y.-T., Lightner D. A. (1983) Tetrahedron39: 1893
Ribó J. M., Masip M. D., Vallès A. (1981) Monatsh. Chem.112: 359
Author information
Authors and Affiliations
Rights and permissions
About this article
Cite this article
Anglada, C., Claret, J., Crusats, J. et al. Reactivity of pyrrole pigments, part 13: Identification of the reaction product generated from bile pigments by the superoxide anion. Monatsh Chem 121, 653–663 (1990). https://doi.org/10.1007/BF00809769
Received:
Accepted:
Issue Date:
DOI: https://doi.org/10.1007/BF00809769