Summary
Muscle fibres of the red and slow contracting soleus of rat, rabbit and cat and of the red however fast contracting thyreoarytenoid of rabbit are compared with different fibre types in the anterior tibial muscle of rat and in the gastrocnemius of rabbit and cat. With respect to fibre types soleus and thyreoarytenoid (including m. vocalis) are homogeneous and both being rich in mitochondria. The fast thyreoarytenoid shows a narrow Z-line (50–60 nm) and a well developed sarcoplasmic reticulum. The pattern of reticulum and mitochondria resembles more that of heart muscle cells than of skeletal muscle fibres. Like many slow contracting muscles of different animals the soleus fibres display a wide Z-line (100–120 nm), few triads, little reticulum and irregularly shaped areas of myofilaments instead of fibrils. In that soleus fibres equal fibres of type C (rich in mitochondria) in a corresponding heterogeneous muscle, whereas intermediate (type B) fibres reveal narrow Z-lines (50–70 nm), isodiametrically shaped myofibrils and more triads than C-fibres. Therefore it is far more likely that the slow motor units of a mixed muscle consist of C-fibres than of B-fibres. This is at variance with the histochemical designation of soleus fibres as type B and thyreoarytenoid fibres as type C.
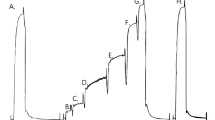
In some muscles in C-fibres the sarcomeres are longer than in B-(and A-)fibres. In the anterior tibial muscle of rat this difference is 8.5% at a mean sarcomere length of 2.6 μm, and disappears at a mean length of 2.8 μm, probably due to the steeper slope of the length tension diagram at rest. Since the isometric extratension in a tetanus is highest at 120% resting length (corresponding to about 2.7 μm sarcomere length), the force of C-fibres exceeds that of B-fibres at 2.6 μm but not at 2.8 μm sarcomere length.
Red and white muscle differ with respect to vascularisation. The relation between the densities of capillaries in soleus and gastrocnemius of cat is 2.7∶:1 and equals the relation between the blood flows through these muscles during rest and maximum vasodilatation.
Zusammenfassung
Die Fasern des roten und langsamen M. soleus von Ratte, Kaninchen und Katze und des roten, jedoch schnellen, M. vocalis des Kaninchens wurden licht- und elektronenmikroskopisch untersucht und mit den verschiedenen Fasertypen aus dem M. tibialis anterior der Ratte und dem M. gastrocnemius des Kaninchens und der Katze verglichen. M. soleus und M. vocalis (einschließlich M. thyreoarytenoideus) enthalten nur einen mitochondrienreichen Fasertyp. Im schnellen M. vocalis ist der Z-Streifen schmal (50–60 nm), das sarcoplasmatische Reticulum ist gut entwickelt. Die Anordnung von Reticulum und Mitochondrion ist ähnlich wie in Herzmuskelzellen. Wie auch in anderen langsamen Muskeln verschiedener Tiere ist im M. soleus der Z-Streifen breit (100–120 nm), Triaden und Reticulum sind selten, und die Filamente bilden unregelmäßige Areale anstelle von Fibrillen. Hierin gleichen die Fasern des M. soleus den (mitochondrienreichen) C-Fasern eines entsprechenden gemischten Muskels; dagegen zeigen die Zwischentyp-(B-)Fasern schmale Z-Linien (50–70 nm), isodiametrische Fibrillen und mehr Triaden als die C-Fasern. Entgegen der bisherigen Vermutung, die auf der histochemischen Zuordnung der SoleusFasern zum Typ B und der Vocalis-Fasern zum Typ C beruht, ist daher anzunehmen, daß die langsamen motorischen Einheiten eines gemischten Muskels aus C- und nicht aus B-Fasern bestehen.
In einigen Muskeln sind die Sarcomere der C-Fasern länger als die der B-(und A-) Fasern. Im M. tibialis anterior der Ratte verschwindet der Unterschied von 8,5% bei 2,6 μm Sarcomerlänge bei der Dehnung auf 2,8 μm mittlere Sarcomerlänge; vermutlich weil die Ruhedehnungskurve zunehmend steiler wird. Die isometrische Extraspannung im Tetanus ist bei 120% der Ruhelänge, d.h. bei 2,7 μm Sarcomerlänge. am größten. Daher muß bei 2,6 μm mittlerer Sarcomerlänge die Kraft der C-Fasern die der B-Fasern übertreffen.
Rote Muskeln sind besser vaskularisiert als weiße Muskeln. Für die Mm. soleus und gastrocnemius der Katze verhalten sich die Kapillardichten (Kapillaren/mm2 Muskelfaserquerschnitt) wie 2,7∶:1. Dieser Wert entspricht dem Verhältnis zwischen den Größen für die Durchblutung (ml/min × 100 g) in Ruhe und bei maximaler Gefäßerweiterung.
Similar content being viewed by others
Literatur
Bubenzer, H. J.: Die dünnen und die dicken Muskelfasern des Zwerchfells der Ratte. Z. Zellforsch. 69, 520–550 (1966).
Buchthal, F., Schmalbruch, H.: Spectrum of contraction times of different fibre bundles in the brachial biceps and triceps muscles of man. Nature (Lond.) 222, 89 (1969).
—: Contraction times and fibre types in intact human muscle. Acta physiol. scand. 79. 435–452 (1970).
—, Kamieniecka, Z.: Contraction times and fiber types in neurogenic paresis. Neurology (Minneap.) 21, 58–67 (1971).
—: Contraction times and fiber types in patients with progressive muscular dystrophy Neurology (Minneap.) 21, 131–139 (1971).
Bullard, H. H.: Histological as related to physiological and chemical differences in certain muscles of the cat. Johns Hopk. Hosp. Rep. 18, 323–328 (1919).
Close, R.: Properties of motor units in fast and slow skeletal muscles of the rat. J. Physiol. (Lond.) 193, 45–55 (1967).
Edgerton, V. R., Simpson, D. R.: The intermediate muscle fiber of rats and guinea pigs. J. Histochem. Cytochem. 17, 828–838 (1969).
Edström, L., Kugelberg, K.: Histochemical composition, distribution of fibres and fatiguability of single motor units. Anterior tibial muscle of the rat. J. Neurol. Neurosurg. Psychiat. 31, 424–433 (1968).
Engel, W. K.: Diseases of the neuromuscular junction and muscle. In: Adams, C. W. M. (ed.), Neurohistochemistry, pp. 622–672. Amsterdam: Elsevier Publ. 1965.
Fawcett, D. W., McNutt, N. S.: The ultrastructure of the cat myocardium. I. Ventricular papillary muscle. J. Cell Biol. 42, 1–45 (1969).
Folkow, B., Halicka, H. D.: A comparison between “red” and “white” muscle with respect to blood supply, capillary surface area and oxygen uptake during rest and exercise. Microvascular Res. 1, 1–14 (1968).
Gauthier, G. F.: On the relationship of ultrastructural and cytochemical features to color in mammalian skeletal muscle. Z. Zellforsch. 95, 462–482 (1969).
—: Padykula, H. A.: Cytological studies of fiber types in skeletal muscle. A comparative study of the mammalian diaphragm. J. Cell Biol. 28, 333–354 (1966).
Geigy, J. R., Geigy AG, (Hrsg.): Documenta Geigy, Wissenschaftliche Tabellen, 6. Aufl. Basel: J. R. Geigy 1960.
Goldspink, G.: Sarcomere length during post-natal growth of mammalian muscle fibres. J. Cell Sci. 3, 539–548 (1968).
Guth, L.: Trophic influences of nerve on muscle. Physiol. Rev. 48, 645–687 (1968).
Hall-Craggs, E. C.: The contraction times and enzyme activity of two rabbit laryngeal muscles. J. Anat. (Lond.) 102, 241–255 (1968).
Handbook of Circulation. Dittmer, D. S., Grebe, R. M. (ed.), pp. 34–37. Philadelphia and London: W. B. Saunders 1959.
Henneman, E., Olson, C. B.: Relations between structure and function in the design of skeletal muscle. J. Neurophysiol. 28, 581–598 (1965).
Hess, A.: Structural differences of fast and slow extrafusal muscle fibers and their nerve endings in chickens. J. Physiol. (Lond.) 157, 221–231 (1961).
Høncke,P.: Investigations on the structure and function of living, isolated, cross striated muscle fibres of mammals. Acta physiol. scand. 15, Suppl. 48 (1947).
Hoyle, G.: Comparative aspects of muscle. Ann. Rev. Physiol. 31, 43–84 (1969).
Kaczmarski, F.: The fine structure of extraocular muscles of the tree sparrow, Passer montanus L. Z. mikr.-anat. Forsch. 82, 523–536 (1970).
Krüger, P.: Über einen möglichen Zusammenhang zwischen Struktur, Funktion und chemischer Beschaffenheit der Muskeln. Biol. Zbl. 49, 616–622 (1929).
—: Tetanus und Tonus der quergestreiften Skeletmuskeln der Wirbeltiere und des Menschen. Leipzig: Akad.-Verlags.-Anst. Geest and Portig 1952.
Kugelberg, E., Edström, L., Abbruzzese, M.: Mapping of motor units in experimentally reinnervated rat muscle. J. Neurol. Neurosurg. Psychiat. 33, 319–329 (1970).
Landon, D. N.: The influence of fixation upon the fine structure of the Z-disk of rat striated muscle. J. Cell Sci. 6, 257–276 (1970).
McPhedran, A. M., Wuerker, R. B., Heneman, E.: Properties of motor units in a homo-geneous red muscle (soleus) of the cat. J. Neurophysiol. 28, 71–84 (1965).
Muralt, A. v.: Einführung in die Praktische Physiologie. Berlin-Göttingen-Heidelberg: Springer 1948.
Page, S. G.: A comparison of the fine structure of frog slow and twitch muscle fibers. J. Cell Biol. 26, 477–497 (1965).
—: Structure and some contractile properties of fast and slow muscles of the chicken. J. Physiol. (Lond.) 205, 131–145 (1969).
Peachey, L. D.: The sarcoplasmic reticulum and transverse tubules of the frog's sartorius. J. Cell Biol. 25, 209–231 (1965).
—, Huxley, A. F.: Structural identification of twitch and slow striated muscle fibers of the frog. J. Cell Biol. 13, 177–180 (1962).
Ranvier, L.: Propriétés et structures différentes des muscles rouges et des muscles blanc chez les lapins et chez les raies. C. R. Acad. Sci. (Paris) 77, 1030–1034 (1873).
Reis, D. J., Moorhead, D., Wooten, G. F., Hollenberg, M.: Some dynamic aspects of blood flow in red and white skeletal muscle in cat. In: Locke, S. (ed.) Modern neurology, Papers in tribute to Derek Denny-Brown, pp. 187–201. Boston: Little, Brown and Co. (Inc.) 1969.
Reynolds, E. S.: The use of lead citrate at high pH as an electron-opaque stain in electron microscopy. J. Cell Biol. 17, 208–212 (1963).
Romanul, F. C. A.: Enzymes in muscle. I. Histochemical studies of enzymes in individual muscle fibers. Arch. Neurol. (Chic.) 11, 355–368 (1964).
—: Capillary supply and metabolism of muscle fibers. Arch. Neurol. (Chic.) 12, 497–50 (1965).
Romeis, B.: Mikroskopische Technik. München und Wien: Oldenbourg 1968.
Sandow, A.: Skeletal muscle. Ann. Rev. Physiol. 32, 87–138 (1970).
Schmalbruch, H.: Die quergestreiften Muskelfasern des Menschen. Ergebn. Anat. Entwickl.-Gesch. 43, 1–75 (1970).
Stein, J. M., Padykula, H. A.: Histochemical classification of individual skeletal muscle fibres of the rat. Amer. J. Anat. 110, 103–124 (1962).
Wuerker, R. B., McPhedran, A. M., Henneman, E.: Properties of motor units in a hetero-geneous pale muscle (m. gastrocnemius) of the cat. J. Neurophysiol. 28, 85–99 (1965).
Author information
Authors and Affiliations
Additional information
Herrn Prof. Dr. Bargmann nachträglich zum 65. Geburtstag.
Rights and permissions
About this article
Cite this article
Schmalbruch, H. „Rote“ Muskelfasern. Z. Zellforsch. 119, 120–146 (1971). https://doi.org/10.1007/BF00330543
Received:
Issue Date:
DOI: https://doi.org/10.1007/BF00330543