Abstract
Purpose
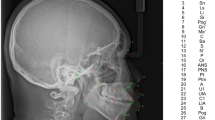
The aim of this investigation was to create an automated cephalometric X‑ray analysis using a specialized artificial intelligence (AI) algorithm. We compared the accuracy of this analysis to the current gold standard (analyses performed by human experts) to evaluate precision and clinical application of such an approach in orthodontic routine.
Methods
For training of the network, 12 experienced examiners identified 18 landmarks on a total of 1792 cephalometric X‑rays. To evaluate quality of the predictions of the AI, both AI and each examiner analyzed 12 commonly used orthodontic parameters on a basis of 50 cephalometric X‑rays that were not part of the training data for the AI. Median values of the 12 examiners for each parameter were defined as humans’ gold standard and compared to the AI’s predictions.
Results
There were almost no statistically significant differences between humans’ gold standard and the AI’s predictions. Differences between the two analyses do not seem to be clinically relevant.
Conclusions
We created an AI algorithm able to analyze unknown cephalometric X‑rays at almost the same quality level as experienced human examiners (current gold standard). This study is one of the first to successfully enable implementation of AI into dentistry, in particular orthodontics, satisfying medical requirements.
Zusammenfassung
Ziel
Ziel der vorliegenden Untersuchung war, eine vollständig automatisierte Fernröntgenseitenanalyse auf Basis eines spezialisierten künstlichen neuronalen Netzwerkes zu entwickeln. Die Genauigkeit dieser Analyse wurde mit der Auswertung menschlicher Experten, dem aktuellem Goldstandard, verglichen, um die Eignung eines solchen Systems zur Verwendung im klinischen Alltag zu überprüfen.
Patienten und Methodik
Für das Training des Netzwerkes wurden auf insgesamt 1792 Fernröntgenseitenbildern jeweils 18 kieferorthopädische Bezugspunkte durch 12 erfahrene Untersucher markiert. Zur Beurteilung der Auswertungsqualität des trainierten Netzwerkes wurden an 50 weiteren Fernröntgenseitenbildern, die nicht Teil der Trainingsdaten waren, sowohl durch die Künstliche Intelligenz (KI) als auch durch jeden der Untersucher 12 gängige kephalometrische Messungen durchgeführt. Als Goldstandard wurde für jeden Parameter der Medianwert der Untersucher definiert, welcher dann mit den Auswertungen der KI verglichen wurde.
Ergebnisse
Zwischen den Auswertungen der KI und dem menschlichen Goldstandard konnten nahezu keine statistisch signifikanten Unterschiede festgestellt werden. Sofern Unterschiede zwischen beiden Auswertungsmethoden bestanden, konnten diese als klinisch irrelevant betrachtet werden.
Schlussfolgerungen
Im Rahmen der vorliegenden Untersuchung war es möglich, ein künstliches neuronales Netzwerk darauf zu trainieren, unbekannte Fernröntgenseitenbilder in annähernd derselben Qualität wie der eines erfahrenen Klinikers auszuwerten. Diese Studie ist einer der ersten erfolgreichen Ansätze, künstliche neuronale Netzwerke in der Zahnmedizin, speziell in der Kieferorthopädie, zu integrieren.






Similar content being viewed by others
References
Arik SO, Ibragimov B, Xing L (2017) Fully automated quantitative cephalometry using convolutional neural networks. J Med Imaging 4:14501
Bland JM, Altman DG (1999) Measuring agreement in method comparison studies. Stat Methods Med Res 8:135–160
Bland JM, Altman DG (2003) Applying the right statistics: analyses of measurement studies. Ultrasound Obstet Gynecol 22:85–93
Broadbent B (1931) A new X‑ray technique and its application to orthodontia. Angle Orthod 1:45–66
Cardillo J, Sid-Ahmed MA (1994) An image processing system for locating craniofacial landmarks. IEEE Trans Med Imaging 13:275–289
Ciresan DC, Meier U, Masci J, Gambardella LM, Schmidhuber J (2011) Flexible, high performance convolutional neural networks for image classification. Paper presented at the Proceedings of the Twenty-Second international joint conference on Artificial Intelligence, Barcelona. vol 2
Desvignes M, Romaniuk B, Clouard R, Demoment R, Revenu M, Deshayes MJ (2000) First steps toward automatic location of landmarks on X‑ray images. In: Proceedings 15th International Conference on Pattern Recognition ICPR-2000, 3–7 Sept. 2000, pp 275–278
Ding Y, Sohn JH, Kawczynski MG, Trivedi H, Harnish R, Jenkins NW, Lituiev D, Copeland TP, Aboian MS, Aparici CM, Behr SC, Flavell RR, Huang S‑Y, Zalocusky KA, Nardo L, Seo Y, Hawkins RA, Pampaloni MH, Hadley D, Franc BL (2019) A deep learning model to predict a diagnosis of alzheimer disease by using 18F-FDG PET of the brain. Radiology 290:456–464
Dreyer KJ, Geis JR (2017) When machines think: radiology’s next frontier. Radiology 285:713–718
El-Feghi I, Sid-Ahmed MA, Ahmadi M (2004) Automatic localization of craniofacial landmarks for assisted cephalometry. Pattern Recognit 37:609–621
Forsyth DB, Davis DN (1996) Assessment of an automated cephalometric analysis system. Eur J Orthod 18:471–478
Fu Jie H, LeCun Y (2006) Large-scale learning with SVM and convolutional for generic object categorization. In: 2006 IEEE Computer Society Conference on Computer Vision and Pattern Recognition (CVPR′06) 17–22 June 2006, pp 284–291
Fukushima K (1975) Cognitron: a self-organizing multilayered neural network. Biol Cybern 20:121–136
Gonçalves FA, Schiavon L, Pereira Neto JS, Nouer DF (2006) Comparison of cephalometric measurements from three radiological clinics. Braz Oral Res 20:162–166
Hinton G, Sejnowski TJ (1999) Unsupervised learning: foundations of neural computation. MIT Press, Cambridge, MA
Kahn CE Jr. (2017) From images to actions: opportunities for artificial intelligence in radiology. Radiology 285:719–720
Kamoen A, Dermaut L, Verbeeck R (2001) The clinical significance of error measurement in the interpretation of treatment results. Eur J Orthod 23:569–578
Kaur A, Singh C (2013) Automatic cephalometric landmark detection using Zernike moments and template matching vol 9
Krizhevsky A, Sutskever I, Hinton G (2012) ImageNet classification with deep convolutional neural networks. Paper presented at the Proceedings of the 25th International Conference on Neural Information Processing Systems, Lake Tahoe. vol 1
LeCun Y, Bengio Y, Hinton G (2015) Deep learning. Nature 521:436–444
Lee JH, Kim DH, Jeong SN, Choi SH (2018) Detection and diagnosis of dental caries using a deep learning-based convolutional neural network algorithm. J Dent 77:106–111
Levy-Mandel AD, Venetsanopoulos AN, Tsotsos JK (1986) Knowledge-based landmarking of cephalograms. Comput Biomed Res 19:282–309
Liu JK, Chen YT, Cheng KS (2000) Accuracy of computerized automatic identification of cephalometric landmarks. Am J Orthod Dentofacial Orthop 118:535–540
Mohri M, Rostamizadeh A, Talwalkar A (2012) Foundations of machine learning. MIT Press, Cambridge, MA
Nebauer C (1998) Evaluation of convolutional neural networks for visual recognition. IEEE Trans Neural Netw 9:685–696
Nishimoto S, Sotsuka Y, Kawai K, Ishise H, Kakibuchi M (2019) Personal computer-based cephalometric landmark detection with deep learning, using cephalograms on the internet. J Craniofac Surg 30:91–95
Parthasarathy S, Nugent ST, Gregson PG, Fay DF (1989) Automatic landmarking of cephalograms. Comput Biomed Res 22:248–269
Ronneberger O, Fischer P, Brox T (2015) U‑net: convolutional networks for biomedical image segmentation. In: Medical image computing and computer-assisted intervention MICCAI 2015. Springer, Cham, pp 234–241
Russell S, Norvig P (2010) Artificial intelligence: a modern approach, 3rd edn. Prentice Hall, Upper Saddle River, NJ
Srivastava N, Hinton G, Krizhevsky A, Sutskever I, Salakhutdinov R (2014) Dropout: a simple way to prevent neural networks from overfitting vol 15
Tong W, Nugent ST, Jensen GM, Fay DF (1989) An algorithm for locating landmarks on dental X‑rays. IEEE, 552–554, https://doi.org/10.1109/IEMBS.1989.95869
Vial A, Stirling D, Field M, Ros M, Ritz C, Carolan M, Holloway L, Miller AA (2018) The role of deep learning and radiomic feature extraction in cancer-specific predictive modelling: a review. Transl Cancer Res 7:803–816
Wang CW, Huang CT, Hsieh MC, Li CH, Chang SW, Li WC, Vandaele R, Maree R, Jodogne S, Geurts P, Chen C, Zheng G, Chu C, Mirzaalian H, Hamarneh G, Vrtovec T, Ibragimov B (2015) Evaluation and comparison of anatomical landmark detection methods for cephalometric X‑Ray images: a grand challenge. IEEE Trans Med Imaging 34:1890–1900
Yang X, Wu N, Cheng G, Zhou Z, Yu DS, Beitler JJ, Curran WJ, Liu T (2014) Automated segmentation of the parotid gland based on atlas registration and machine learning: a longitudinal MRI study in head-and-neck radiation therapy. Int J Radiat Oncol Biol Phys 90:1225–1233
Yasaka K, Akai H, Kunimatsu A, Kiryu S, Abe O (2018) Deep learning with convolutional neural network in radiology. Jpn J Radiol 36:257–272
Author information
Authors and Affiliations
Corresponding author
Ethics declarations
Conflict of interest
F. Kunz, A. Stellzig-Eisenhauer, F. Zeman and J. Boldt declare that they have no competing interests.
Additional information
This paper received the Arnold-Biber Research Award of the German Orthodontic Society for the year 2019.
Rights and permissions
About this article
Cite this article
Kunz, F., Stellzig-Eisenhauer, A., Zeman, F. et al. Artificial intelligence in orthodontics. J Orofac Orthop 81, 52–68 (2020). https://doi.org/10.1007/s00056-019-00203-8
Received:
Accepted:
Published:
Issue Date:
DOI: https://doi.org/10.1007/s00056-019-00203-8