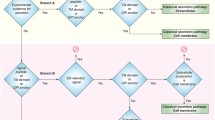
Abstract
Aspergillus fumigatus is a medically important human pathogenic fungus. It can cause various diseases such as serious allergic reactions and life-threatening, invasive infections. Proteome analyses massively contribute to elucidating host-pathogen interactions. Here, we describe challenges to analyze host-pathogen interactions using mass spectrometry-based proetomics; we provide insights into our research findings and current understanding about the role of proteins from both the fungus and human immune cells during infections.
Article PDF
Similar content being viewed by others
Avoid common mistakes on your manuscript.
Literatur
Brown GD, Denning DW, Gow NA et al. (2012) Hidden killers: human fungal infections. Sci Transl Med 4: 165rv13
Bongomin F, Gago S, Oladele RO et al. (2017) Global and multi-national prevalence of fungal diseases-estimate precision. J Fungi 3: 1–29
Thywissen A, Heinekamp T, Dahse HM et al. (2011) Conidial dihydroxynaphthalene melanin of the human pathogenic fungus Aspergillus fumigatus interferes with the host endocytosis pathway. Front Microbiol 2: 96
Schmidt F, Thywißen A, Goldmann M et al. (2020) Flotillin-dependent membrane microdomains are required for functional phagolysosomes against fungal infections. Cell Reports 32: 108017
Brakhage AA, Zimmermann A-K, Rivieccio F et al. (2021) Host-derived extracellular vesicles for antimicrobial defense. microLife 2: uqab003
Shopova IA, Belyaev I, Dasari P et al. (2020) Human neutrophils produce antifungal extracellular vesicles against Aspergillus fumigatus. mBio 11: e00596–20
Voltersen V, Blango MG, Herrmann S et al. (2018) Proteome analysis reveals the conidial surface protein CcpA essential for virulence of the pathogenic fungus Aspergillus fumigatus. mBio 9: e01557–18
Jia LJ, Krüger T, Blango MG et al. (2020) Biotinylated surfome profiling identifies potential biomarkers for diagnosis and therapy of Aspergillus fumigatus infection. mSphere 5: e00535–20
Schmidt H, Vlaic S, Krüger T et al. (2018) Proteomics of Aspergillus fumigatus conidia-containing phagolysosomes identifies processes governing immune evasion. Mol Cell Proteomics 17: 1084–1096
Goldmann M, Schmidt F, Kyrmizi I et al. (2021) Isolation and immunofluorescence staining of Aspergillus fumigatus conidia-containing phagolysosomes. STAR Protoc 2: 100328
Rafiq M, Rivieccio F, Zimmermann AK et al. (2022) PLB-985 neutrophil-like cells as a model to study Aspergillus fumigatus pathogenesis. mSphere 7: e00940–21
Blango MG, Pschibul A, Rivieccio F et al. (2020) Dynamic surface proteomes of allergenic fungal conidia. J Proteome Res 19: 2092–2104
Rodríguez-Ortega MJ, Norais N, Bensi G et al. (2006) Characterization and identification of vaccine candidate proteins through analysis of the group A Streptococcus surface proteome. Nat Biotechnol 24: 191–197
Jahn B, Langfelder K, Schneider U et al. (2002) PKSP-dependent reduction of phagolysosome fusion and intracellular kill of Aspergillus fumigatus conidia by human monocyte-derived macrophages. Cell Microbiol 4: 793–803
Jia LJ, Rafiq M, Radosa L et al. (2023) Aspergillus fumigatus hijacks human p11 to redirect fungal-containing phagosomes to non-degradative pathway. Cell Host Microbe 31: 373–388
Marin-Esteban V, Turbica I, Dufour G et al. (2012) Afa/ Dr diffusely adhering Escherichia coli strain C1845 induces neutrophil extracellular traps that kill bacteria and damage human enterocyte-like cells. Infect Immun 80: 1891–1899
Lane RE, Korbie D, Trau M et al. (2019) Optimizing size exclusion chromatography for extracellular vesicle enrichment and proteomic analysis from clinically relevant samples. Proteomics 19: e1800156
Timar CI, Lorincz AM, Csepanyi-Komi R et al. (2013) Antibacterial effect of microvesicles released from human neutrophilic granulocytes. Blood 121: 510–518
Funding
Open Access funding enabled and organized by Projekt DEAL.
Author information
Authors and Affiliations
Corresponding author
Additional information
Danksagung
Wir danken allen aktuellen und ehemaligen Mitgliedern der Arbeitsgruppe sowie allen Kooperationspartnern, die an der Konzeption, Erhebung und Analyse der vorgestellten Daten beteiligt waren. Ein besonderer Dank gilt allen Blutspendern, ohne die die Untersuchungen nicht möglich wären. Die Autoren danken der DFG (SFB/Transregio 124 – FungiNet) und dem BMBF (Leibniz-Zentrum für Photonik in der Infektionsforschung) für ihre finanzielle Unterstützung.
Lei-Jie Jia, Arite Bigalke, Olaf Kniemeyer, Axel Brakhage (Abteilungsleiter) und Thomas Krüger (v. l. n. r.).
Arite Bigalke, 2008–2014 Studium der Ernährungswissenschaften, Universität Jena (FSU). 2014–2019 Promotion (FSU Jena, Prof. Dr. G. Pohnert). 2019–2021 Postdoc (PD Dr. Dr. M. Kiehntopf). Seit 2021 wissenschaftliche Mitarbeiterin am Leibniz-HKI (Prof. Dr. A. A. Brakhage) mit Schwerpunkten in der Wirkmechanismusforschung von antifungalen Substanzen sowie im Aufbau einer LC-MS-basierten Analyseplattform für Targetproteomanalysen.
Thomas Krüger, 2000–2006 Studium der Ernährungswissenschaften, Universität Jena (FSU). 2006–2010 Promotion. 2010–2012 Postdoc. Seit 2013 wissenschaftlicher Mitarbeiter am Leibniz-HKI (Prof. Dr. A. A. Brakhage) verantwortlich für LC-MS-basierte Proteomanalysen mit infektionsbiologischem Schwerpunkt (Interaktion von humanpathogenen Pilzen mit dem menschlichen Wirt).
Lei-Jie Jia, 2005–2009 Biologiestudium (Pädagogische Universität Shandong, Jinan, China). 2009–2016 Promotion am Shanghai Institut für Biowissenschaften, Chinesische Akademie der Wissenschaften, Shanghai, China. Seit 2017 Postdoc am Leibniz HKI (Prof. Dr. A. A. Brakhage) mit Schwerpunkten Infektionsbiologie von A. fumigatus, intrazelluläre Prozessierung.
Olaf Kniemeyer, 1991–1998 Studium der Biologie. 1998–2001 Promotion. 2002–2005 Postdoc. Seit 2005 wissenschaftlicher Mitarbeiter am Leibniz-Institut für Naturstoff-Forschung und Infektionsbiologie (Leibniz-HKI) (Abt. Molekulare und Angewandte Mikrobiologie, A. Brakhage). Seit 2009 stellvertretender Abteilungsleiter. Schwerpunkte: Pathobiologie von A. fumigatus und neue Therapiestrategien.
Axel Brakhage Seit 2004 Leiter Lehrstuhl für Mikrobiologie und Molekularbiologie, Institut für Mikrobiologie, Universität Jena. Seit 2005 Direktor, Leibniz-Institut für Naturstoff-Forschung und Infektionsbiologie (Leibniz-HKI) und Leiter der Abteilung Molekulare und Angewandte Mikrobiologie. Sprecher des BMBF-Konsortiums InfectControl sowie des SFB/TR Humanpathogene Pilze und ihr menschlicher Wirt–Netzwerke der Interaktion (FungiNet).
Rights and permissions
Dieser Artikel wird unter der Creative Commons Namensnennung 4.0 International Lizenz veröffentlicht, welche die Nutzung, Vervielfältigung, Bearbeitung, Verbreitung und Wiedergabe in jeglichem Medium und Format erlaubt, sofern Sie den/die ursprünglichen Autor(en) und die Quelle ordnungsgemäß nennen, einen Link zur Creative Commons Lizenz beifügen und angeben, ob Änderungen vorgenommen wurden. Die in diesem Artikel enthaltenen Bilder und sonstiges Drittmaterial unterliegen ebenfalls der genannten Creative Commons Lizenz, sofern sich aus der Abbildungslegende nichts anderes ergibt. Sofern das betreffende Material nicht unter der genannten Creative Commons Lizenz steht und die betreffende Handlung nicht nach gesetzlichen Vorschriften erlaubt ist, ist für die oben aufgeführten Weiterverwendungen des Materials die Einwilligung des jeweiligen Rechteinhabers einzuholen. Weitere Details zur Lizenz entnehmen Sie bitte der Lizenzinformation auf http://creativecommons.org/licenses/by/4.0/deed.de.
About this article
Cite this article
Bigalke, A., Krüger, T., Jia, LJ. et al. Pathoproteomik des humanpathogenen Pilzes Aspergillus fumigatus. Biospektrum 29, 269–272 (2023). https://doi.org/10.1007/s12268-023-1932-9
Published:
Issue Date:
DOI: https://doi.org/10.1007/s12268-023-1932-9