Abstract
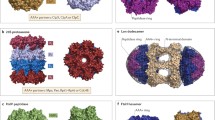
Bacterial AAA+ proteins play crucial roles in proteostasis networks and ensure protein homeostasis during stress conditions. They function as ATP-dependent components of proteolytic complexes degrading misfolded proteins or as disaggregases reactivating aggregated proteins. AAA+ proteins generate an ATP-fueled threading force driving substrate unfolding and translocation. Their central functions in protein quality control qualify them as antibacterial drug target.
Article PDF
Similar content being viewed by others
Avoid common mistakes on your manuscript.
Literatur
Puchades C, Sandate CR, Lander GC (2020) The molecular principles governing the activity and functional diversity of AAA+ proteins. Nat Rev Mol Cell Biol 21: 43–58
Olivares AO, Baker TA, Sauer RT (2018) Mechanical protein unfolding and degradation. Annu Rev Physiol 80: 413–429
Mogk A, Kummer E, Bukau B (2015) Cooperation of Hsp70 and Hsp100 chaperone machines in protein disaggregation. Front Mol Biosci 2: 22
Lee C, Franke KB, Kamal SM et al. (2018) Stand-alone ClpG disaggregase confers superior heat tolerance to bacteria. Proc Natl Acad Sci U S A 115: E273–E282
Katikaridis P, Meins L, Kamal SM et al. (2019) ClpG Provides Increased Heat Resistance by Acting as Superior Disaggregase. Biomolecules 9: 815
Deville C, Franke K, Mogk A et al. (2019) Two-step activation mechanism of the ClpB disaggregase for sequential substrate threading by the main ATPase motor. Cell Rep 27: 3433–3446
Avellaneda MJ, Franke KB, Sunderlikova V et al. (2020) Processive extrusion of polypeptide loops by a Hsp100 disaggregase. Nature 578: 317–320
Carroni M, Franke KB, Maurer M et al. (2017) Regulatory coiled-coil domains promote head-to-head assemblies of AAA+ chaperones essential for tunable activity control. eLife 6: e30120
Maurer M, Linder D, Franke KB et al. (2019) Toxic activation of an AAA+ protease by the antibacterial drug cyclomarin A. Cell Chem Biol 26: 1169–1179
Funding
Open Access funding enabled and organized by Projekt DEAL.
Author information
Authors and Affiliations
Corresponding author
Additional information
Axel Mogk Jahrgang 1968. Biochemiestudium an der Universität Bayreuth. 1997 Promotion. 1998–2006 Postdoc und wiss. Assistent am Institut für Biochemie, Universität Freiburg und am Zentrum für Molekulare Biologie der Universität Heidelberg (ZMBH) in der Arbeitsgruppe Prof. Dr. B. Bukau. Seit 2007 akademischer Rat und Privatdozent am ZMBH
Rights and permissions
Dieser Artikel wird unter der Creative Commons Namensnennung 4.0 International Lizenz veröffentlicht, welche die Nutzung, Vervielfältigung, Bearbeitung, Verbreitung und Wiedergabe in jeglichem Medium und Format erlaubt, sofern Sie den/die ursprünglichen Autor(en) und die Quelle ordnungsgemäß nennen, einen Link zur Creative Commons Lizenz beifügen und angeben, ob Änderungen vorgenommen wurden. Die in diesem Artikel enthaltenen Bilder und sonstiges Drittmaterial unterliegen ebenfalls der genannten Creative Commons Lizenz, sofern sich aus der Abbildungslegende nichts anderes ergibt. Sofern das betreffende Material nicht unter der genannten Creative Commons Lizenz steht und die betreffende Handlung nicht nach gesetzlichen Vorschriften erlaubt ist, ist für die oben aufgeführten Weiterverwendungen des Materials die Einwilligung des jeweiligen Rechteinhabers einzuholen. Weitere Details zur Lizenz entnehmen Sie bitte der Lizenzinformation auf http://creativecommons.org/licenses/by/4.0/deed.de.
About this article
Cite this article
Mogk, A. Mechanismen und Funktionen von bakteriellen AAA+Entfaltungsmaschinen. Biospektrum 27, 22–24 (2021). https://doi.org/10.1007/s12268-021-1515-7
Published:
Issue Date:
DOI: https://doi.org/10.1007/s12268-021-1515-7